Comparaison et analyse des produits des procédés d'extraction par hydrolyse alcaline et par hydrolyse acide de Lycium barbarum combiné à des polyphénols
Les substances phénoliques sont largement répandues dans le règne végétal, y compris les flavonoïdes, les anthocyanes, les catéchines, etc., et constituent l'un des métabolites secondaires les plus abondants dans les plantes. En raison de leurs puissantes propriétés antioxydantes et de leurs effets significatifs sur la prévention de diverses maladies liées au stress oxydatif, tels que les effets antioxydants, anti-inflammatoires, antitumoraux, hypotenseurs, hypoglycémiques et hypolipidémiants, les substances phénoliques dans l'alimentation et la médecine naturelle/traditionnelle chinoise font l'objet d'une attention croissante. Dans les plantes, les phénols existent à la fois sous forme libre et sous forme liée, à savoir les substances phénoliques solubles qui peuvent être extraites par des solvants et les composés phénoliques non extractibles (CPNE) qui ne peuvent pas être directement extraits par des solvants. Ces derniers se lient aux macromolécules telles que les sucres, l'hémicellulose, la pectine et les protéines par des liaisons covalentes telles que les liaisons ester et les liaisons glycosidiques, et constituent la principale forme de composants phénoliques dans les plantes. Les recherches sur les substances phénoliques dans les aliments ont montré que les CPNE présentent une meilleure activité biologique que les substances phénoliques libres. Par exemple, par rapport aux phénols libres, la CPNE présente dans les céréales une capacité de piégeage du radical peroxyde et une activité antioxydante cellulaire plus élevées. On pense généralement que l'activité biologique des substances phénoliques dans les plantes est étroitement liée à leur biodisponibilité. Les recherches sur le métabolisme des médicaments ont montré que les phénols libres peuvent être dégradés par les sucs digestifs, alors que la CPNE n'est pas digérée en raison de son association avec de grosses molécules. Après avoir pénétré dans l'intestin, il est hydrolysé par le microbiote intestinal pour exercer une activité biologique et même présenter des effets similaires à ceux des formulations à libération prolongée. En outre, certains NEPC peuvent être convertis en d'autres composés qui affectent le corps humain. Par conséquent, une analyse approfondie des CPNE dans les aliments et la médecine naturelle/traditionnelle chinoise peut contribuer à une évaluation complète de l'activité biologique des substances phénoliques.
Lycium barbarum L. est un fruit séché et mûr de Lycium barbarum L., une plante de la famille des Solanacées. Les études pharmacologiques modernes ont montré que Lycium barbarum possède de multiples activités biologiques potentielles, dont la plupart sont liées à l'activité antioxydante, qui est l'effet synergique des polysaccharides et des composés phénoliques de Lycium barbarum. Notre groupe de recherche a découvert dans des études antérieures que l'acide gallique et l'acide férulique peuvent être détectés dans les produits d'hydrolyse alcaline des polysaccharides de Lycium barbarum, ce qui indique la présence de NEPC. Les résultats pertinents de l'analyse suggèrent que les CPNE de Lycium barbarum jouent un rôle important dans son activité antioxydante. À l'heure actuelle, les recherches sur les composés phénoliques des baies de goji se concentrent principalement sur les phénols solubles. En négligeant le NEPC, on risque de sous-estimer la teneur totale, la capacité antioxydante et l'impact positif des composés phénoliques des baies de goji sur la santé humaine.
Pour analyser les CPNE, il faut d'abord utiliser des méthodes d'hydrolyse appropriées afin de rompre les liaisons ester et glycosidiques et de libérer les composants phénoliques. À l'heure actuelle, les méthodes d'hydrolyse les plus couramment utilisées dans la littérature sont l'hydrolyse acide et l'hydrolyse alcaline. Environ 30% des études utilisent l'acide (généralement l'acide chlorhydrique ou l'acide sulfurique) pour hydrolyser les liaisons covalentes entre les CPNE et les macromolécules. Par rapport à l'hydrolyse alcaline, l'hydrolyse acide peut libérer davantage de composants phénoliques, mais la température élevée, les conditions d'acidité élevée et l'hydrolyse prolongée requises pour l'hydrolyse acide peuvent souvent conduire à la dégradation des composants phénoliques. Les composés phénoliques courants dans les plantes, tels que l'acide férulique, se lient souvent aux parois cellulaires par des liaisons ester. La plupart des études utilisent l'hydrolyse alcaline pour analyser la NEPC dans les plantes. Lors de l'hydrolyse de la NEPC avec des bases inorganiques telles que l'hydroxyde de sodium, des températures élevées ne sont pas nécessaires, mais la réaction doit souvent être effectuée en l'absence de lumière sous protection d'azote afin d'éviter la dégradation des composants phénoliques.
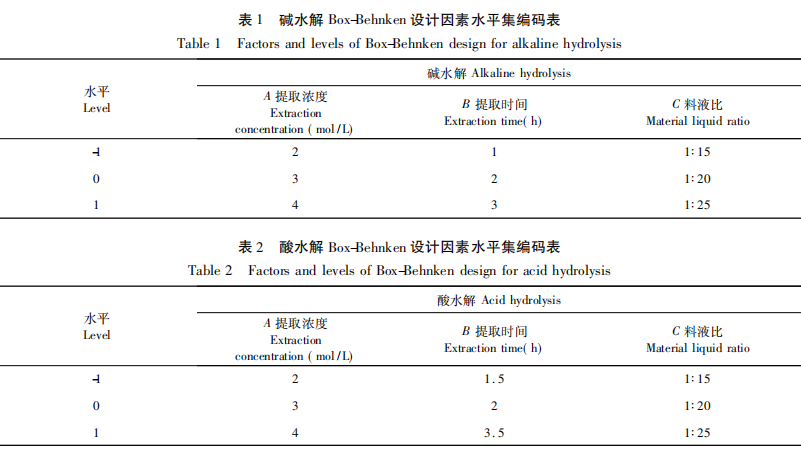
Afin d'évaluer de manière exhaustive les composants phénoliques des baies de goji, cette étude a utilisé l'hydrolyse acide et l'hydrolyse alcaline pour éliminer les composants phénoliques libres des baies de goji. Le rendement des composants phénoliques a été utilisé comme indice d'évaluation, et des expériences à facteur unique ainsi que la méthodologie de la surface de réponse ont été utilisées pour évaluer les effets de la concentration acide-base, de la durée de l'hydrolyse et du rapport solide-liquide sur l'indice d'évaluation. Les conditions de traitement pour l'hydrolyse alcaline et l'hydrolyse acide ont été optimisées ; et l'UPLC-Q-TOF-MS a été utilisée pour comparer les composants phénoliques dans les échantillons obtenus par différentes méthodes d'hydrolyse, fournissant une référence pour la sélection de méthodes d'hydrolyse appropriées pour différents composants phénoliques.












Les composés phénoliques sont les métabolites secondaires les plus abondants dans les plantes et également l'une des substances bioactives les plus concernées. Les composés phénoliques des plantes existent à la fois sous forme libre et sous forme liée, la NEPC étant le principal composant des substances phénoliques dans les plantes. La plupart des études antérieures se sont concentrées sur la composition et l'activité biologique des phénols libres, en accordant moins d'attention à la NEPC. Actuellement, un nombre croissant d'études suggèrent que la CPNE pourrait être une substance active importante dans l'alimentation et la médecine naturelle/traditionnelle chinoise. De même, les recherches sur les composants phénoliques libres des baies de goji ont été très approfondies, mais aucun rapport n'a été publié sur la CPNE. Les recherches préliminaires de l'équipe de recherche ont montré que les polysaccharides de Lycium barbarum peuvent être hydrolysés avec de l'hydroxyde de sodium faible (0,2mol/L) pour obtenir des substances phénoliques, ce qui indique la présence possible de substances phénoliques liées par des liaisons ester. On pense généralement que la CPNE interagit avec des macromolécules telles que la cellulose, les protéines et la lignine sous forme de liaisons covalentes, ou qu'elle se lie aux fibres végétales ou s'incorpore dans les cellules par des liaisons ioniques ou des interactions physiques. La NEPC des baies de goji est liée à des polysaccharides ou à des substrats végétaux, et une confirmation supplémentaire est nécessaire.
La CPNE ne peut pas être extraite directement à l'aide d'eau ou de solvants alcooliques. Pour analyser les CPNE dans les baies de goji, il faut utiliser des méthodes d'hydrolyse alcaline ou d'hydrolyse acide pour préparer les CPNE. L'alcali peut rompre les liaisons ester entre les composants phénoliques et des substances telles que les sucres, les protéines, la pectine, les fibres, etc. L'hydroxyde de sodium est le composé d'hydrolyse alcaline le plus couramment utilisé. Au cours du processus d'hydrolyse alcaline, les composants phénoliques subissent souvent une dégradation dans des conditions telles que l'oxygène, les températures élevées et la lumière. C'est pourquoi ils sont souvent hydrolysés à basse température, en l'absence de lumière et sous protection d'azote. Dans cette étude, l'hydrolyse à basse température a également été réalisée sous protection d'azote en utilisant de l'hydroxyde de sodium comme catalyseur d'hydrolyse. L'hydrolyse acide utilise généralement des acides forts tels que l'acide chlorhydrique. L'acide chlorhydrique peut non seulement hydrolyser les liaisons ester, mais aussi hydrolyser les liaisons glycosidiques, libérant ainsi efficacement les monomères ou les oligomères de la NEPC. Dans cette étude, le NEPC dans les baies de goji mesuré par hydrolyse alcaline était de 0,65 ± 0,05mg/100g, alors qu'il était de 0,52 ± 0,03mg/100g dans les produits d'hydrolyse acide. La différence entre les deux peut être due aux mécanismes différents de l'hydrolyse acide et de l'hydrolyse alcaline. Les expériences à facteur unique et les expériences de surface de réponse ont montré que le temps optimal requis pour l'hydrolyse alcaline était le même que pour l'hydrolyse acide. Cependant, le rendement de la NEPC préparée par hydrolyse alcaline était plus élevé, ce qui peut s'expliquer par le fait que l'hydrolyse alcaline interrompt davantage la liaison de la NEPC avec les protéines structurelles, les fibres alimentaires, etc. Le traitement acide rompt les liaisons glycosidiques et dissout les sucres. Dans des conditions acides, les groupes hydroxyles des molécules de polyphénols sont facilement protonés, ce qui entraîne la rupture des molécules de polyphénols et la libération de monomères ou d'oligomères. En conditions alcalines, les groupes hydroxyles des molécules de polyphénol sont plus facilement déprotonés qu'en conditions d'hydrolyse acide, ce qui se traduit par des rendements d'hydrolyse alcaline légèrement plus élevés et des pertes réduites.
Des études antérieures ont mis en évidence des différences entre les CPNE obtenus par hydrolyse alcaline et par hydrolyse acide. L'acide caféique, les catéchines et les dérivés de l'acide gallique peuvent être détectés dans les produits de l'hydrolyse acide de la farine, tandis que l'acide férulique n'existe que dans les produits de l'hydrolyse alcaline, ce qui indique qu'il pourrait y avoir plus de types de substances phénoliques obtenues par l'hydrolyse acide. Cette étude a utilisé l'UPLC-Q-TOF-MS pour analyser la composition des substances dans les produits d'hydrolyse NEPC des baies de goji. Le chromatogramme des ions totaux (voir figure 6) a montré qu'il n'y avait pas de différence dans les types de composés entre les produits de l'hydrolyse alcaline et ceux de l'hydrolyse acide, mais que le nombre de produits de l'hydrolyse acide était significativement plus élevé que celui des produits de l'hydrolyse alcaline. Ce phénomène peut être dû à la déprotonation et à la destruction faciles des groupes hydroxyles phénoliques dans les environnements alcalins forts, ce qui les rend indétectables par spectrométrie de masse, alors que les substances phénoliques sont plus stables et plus faciles à détecter dans les environnements acides ; d'autre part, l'hydrolyse alcaline ne peut rompre que les liaisons ester entre les phénols et les macromolécules, alors que les acides peuvent hydrolyser non seulement les liaisons ester mais aussi les liaisons glycosidiques, de sorte qu'il existe davantage de types de substances phénoliques pouvant être détectées. Du point de vue des produits, les principaux sont les dérivés phénylpropanoïdes. Parmi les 11 composés identifiés, il y a 8 phénylpropanoïdes, 1 coumarine, 1 dérivé phénylpropanoïde et 1 benzophénone. Dans le produit d'hydrolyse alcaline, seuls quatre composés peuvent être identifiés, l'acide férulique étant la substance principale ; et les 11 composés identifiés peuvent être détectés dans les produits d'hydrolyse acide. Il convient de noter que parmi les 8 acides phénoliques, 2 composés peuvent être les produits de l'ouverture du cycle coumarinique lactone au cours de l'hydrolyse du NEPC, plutôt que les substances natives des baies de goji. Cela peut être lié à la forte concentration d'acides utilisés dans le processus d'hydrolyse. À un stade ultérieur, la concentration d'acides ou de bases peut être réduite pour obtenir une structure moléculaire plus complète. En outre, le NEPC contenu dans les baies de goji est principalement constitué d'acides phénylpropanoïdes et de composants coumariniques. La présence d'autres composants doit encore faire l'objet d'une analyse plus approfondie des produits d'hydrolyse. Afin d'effectuer une analyse approfondie de la NEPC dans les baies de goji, la détection par spectrométrie de masse devrait être utilisée comme guide à un stade ultérieur, et la concentration d'acide/alcali pendant l'hydrolyse devrait être ajustée pour obtenir la véritable NEPC native appartenant aux baies de goji.
