Comparación y análisis de productos de los procesos de extracción por hidrólisis alcalina e hidrólisis ácida de Lycium barbarum combinados con polifenoles
Las sustancias fenólicas están ampliamente distribuidas en el reino vegetal, incluyendo flavonoides, flavonoides, antocianinas, catequinas, etc., y son uno de los metabolitos secundarios más abundantes en las plantas. Debido a sus potentes propiedades antioxidantes y a sus importantes efectos en la prevención de diversas enfermedades relacionadas con el estrés oxidativo, como efectos antioxidantes, antiinflamatorios, antitumorales, hipotensores, hipoglucémicos y reductores de lípidos, las sustancias fenólicas en los alimentos y en la medicina natural/tradicional china están recibiendo cada vez más atención. En las plantas, los fenoles existen tanto en forma libre como ligada, a saber, sustancias fenólicas solubles que pueden extraerse con disolventes y compuestos fenólicos no extraíbles (CPNE) que no pueden extraerse directamente con disolventes. Estos últimos se unen a macromoléculas como azúcares, hemicelulosa, pectina y proteínas mediante enlaces covalentes como los enlaces éster y los enlaces glicosídicos, y constituyen la principal forma de componentes fenólicos en las plantas. La investigación sobre las sustancias fenólicas en los alimentos ha descubierto que el NEPC presenta una mejor actividad biológica que las sustancias fenólicas libres. Por ejemplo, en comparación con los fenoles libres, el NEPC de los cereales muestra una mayor capacidad de eliminación de radicales de peróxido y una mayor actividad antioxidante celular. En general, se cree que la actividad biológica de las sustancias fenólicas en las plantas está estrechamente relacionada con su biodisponibilidad. La investigación sobre el metabolismo de los fármacos ha descubierto que los fenoles libres pueden ser degradados por los jugos digestivos, mientras que el NEPC no se digiere debido a su asociación con moléculas grandes. Tras entrar en el intestino, es hidrolizado por la microbiota intestinal para ejercer actividad biológica e incluso mostrar efectos similares a las formulaciones de liberación sostenida. Además, algunos NEPC pueden convertirse en otros compuestos que afectan al cuerpo humano. Por lo tanto, el análisis en profundidad del NEPC en los alimentos y la medicina natural/tradicional china puede ayudar a evaluar exhaustivamente la actividad biológica de las sustancias fenólicas.
Lycium barbarum L. es un fruto seco y maduro de Lycium barbarum L., una planta de la familia de las solanáceas. Estudios farmacológicos modernos han demostrado que Lycium barbarum tiene múltiples actividades biológicas potenciales, la mayoría de las cuales están relacionadas con la actividad antioxidante, que es el efecto sinérgico de los polisacáridos y los compuestos fenólicos de Lycium barbarum. Nuestro grupo de investigación descubrió en estudios anteriores que el ácido gálico y el ácido ferúlico pueden detectarse en los productos de hidrólisis alcalina de los polisacáridos de Lycium barbarum, lo que indica la presencia de NEPC. Los resultados de los análisis pertinentes sugieren que el NEPC en Lycium barbarum desempeña un papel importante en su actividad antioxidante. En la actualidad, la investigación sobre los compuestos fenólicos de las bayas de goji se centra principalmente en los fenoles solubles. Descuidar el NEPC puede subestimar el contenido total, la capacidad antioxidante y el impacto positivo de los compuestos fenólicos de las bayas de goji en la salud humana.
Para analizar el NEPC, deben utilizarse primero métodos de hidrólisis adecuados para romper los enlaces éster y glicosídicos y liberar los componentes fenólicos. En la actualidad, los métodos de hidrólisis más utilizados en la literatura son la hidrólisis ácida y la hidrólisis alcalina. Aproximadamente 30% de los estudios utilizan ácido (normalmente ácido clorhídrico o ácido sulfúrico) para hidrolizar los enlaces covalentes entre el NEPC y las macromoléculas. En comparación con la hidrólisis alcalina, la hidrólisis ácida puede liberar más componentes fenólicos, pero la alta temperatura, las condiciones de alta acidez y la hidrólisis prolongada requeridas para la hidrólisis ácida pueden conducir a menudo a la degradación de los componentes fenólicos. Los compuestos fenólicos comunes en las plantas, como el ácido ferúlico, suelen unirse a las paredes celulares a través de enlaces éster. La mayoría de los estudios utilizan la hidrólisis alcalina para analizar el NEPC en las plantas. Cuando se hidroliza NEPC con bases inorgánicas como hidróxido de sodio, no se requieren altas temperaturas, pero la reacción a menudo debe llevarse a cabo en ausencia de luz bajo protección de nitrógeno para evitar la degradación de los componentes fenólicos.
Con el fin de evaluar exhaustivamente los componentes fenólicos de las bayas de goji, este estudio utilizó la hidrólisis ácida y la hidrólisis alcalina para eliminar los componentes fenólicos libres de las bayas de goji. El rendimiento de los componentes fenólicos se utilizó como índice de evaluación, y se emplearon experimentos de un solo factor y la metodología de superficie de respuesta para evaluar los efectos de la concentración ácido-base, el tiempo de hidrólisis y la relación sólido-líquido sobre el índice de evaluación. Se optimizaron las condiciones de proceso para la hidrólisis alcalina y la hidrólisis ácida; y se utilizó UPLC-Q-TOF-MS para comparar los componentes fenólicos en muestras obtenidas por diferentes métodos de hidrólisis, proporcionando una referencia para seleccionar métodos de hidrólisis apropiados para diferentes componentes fenólicos.
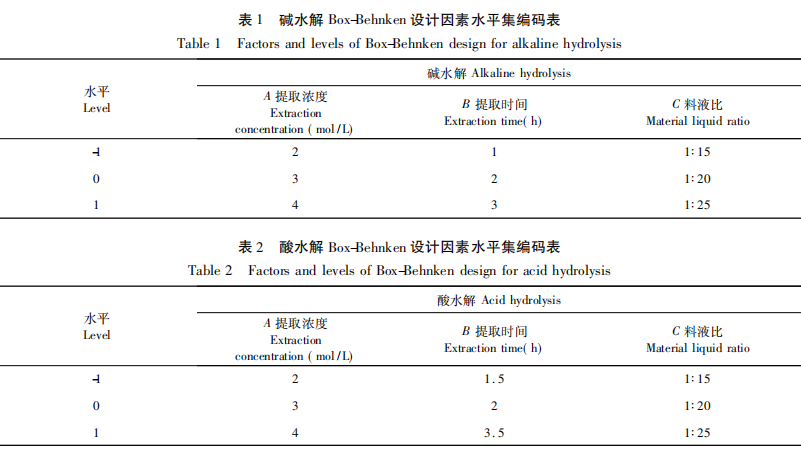






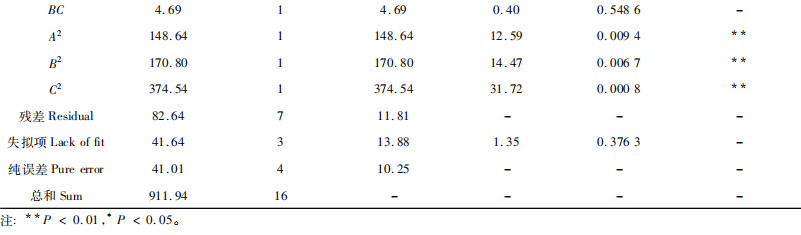






Los compuestos fenólicos son los metabolitos secundarios más abundantes en las plantas y también una de las sustancias bioactivas más preocupantes. Los compuestos fenólicos de las plantas existen tanto en forma libre como ligada, siendo el NEPC el principal componente de las sustancias fenólicas de las plantas. La mayoría de los estudios anteriores se han centrado en la composición y la actividad biológica de los fenoles libres, prestando menos atención al NEPC. En la actualidad, un número creciente de estudios sugiere que el NEPC puede ser una sustancia activa importante en los alimentos y en la medicina natural/tradicional china. Del mismo modo, la investigación sobre los componentes fenólicos libres en las bayas de goji ha sido muy profunda, pero no ha habido informes sobre el NEPC. La investigación preliminar del equipo de investigación descubrió que los polisacáridos de Lycium barbarum pueden hidrolizarse con hidróxido de sodio débil (0,2mol/L) para obtener sustancias fenólicas, lo que indica la posible presencia de sustancias fenólicas unidas por enlaces éster. Generalmente se cree que el NEPC interactúa con macromoléculas como la celulosa, las proteínas y la lignina en forma de enlaces covalentes, o se une a las fibras vegetales o se incrusta en las células mediante enlaces iónicos o interacciones físicas. El NEPC de las bayas de goji está unido a polisacáridos o sustratos vegetales, por lo que se necesita una mayor confirmación.
El NEPC no puede extraerse directamente utilizando agua o disolventes alcohólicos. Para analizar el NEPC en las bayas de goji, deben utilizarse métodos de hidrólisis alcalina o hidrólisis ácida para preparar el NEPC. El álcali puede romper los enlaces éster entre los componentes fenólicos y sustancias como azúcares, proteínas, pectina, fibras, etc., liberando así los fenoles y pudiendo ser detectados. El hidróxido de sodio es el compuesto de hidrólisis alcalina más utilizado. Durante el proceso de hidrólisis alcalina, los componentes fenólicos suelen sufrir degradación en condiciones como el oxígeno, las altas temperaturas y la luz. Por lo tanto, a menudo se hidrolizan a bajas temperaturas en ausencia de luz bajo protección de nitrógeno. En este estudio, la hidrólisis a baja temperatura también se llevó a cabo bajo protección de nitrógeno utilizando hidróxido de sodio como catalizador de hidrólisis. La hidrólisis ácida suele utilizar ácidos fuertes como el ácido clorhídrico. El ácido clorhídrico no sólo puede hidrolizar los enlaces éster, sino también los enlaces glicosídicos, liberando eficazmente monómeros u oligómeros de NEPC. En este estudio, el NEPC en las bayas de goji medido por hidrólisis alcalina fue de 0,65 ± 0,05mg/100g, mientras que fue de 0,52 ± 0,03mg/100g en los productos de hidrólisis ácida. La diferencia entre ambos puede deberse a los distintos mecanismos de la hidrólisis ácida y la hidrólisis alcalina. Tanto los experimentos de factor único como los experimentos de superficie de respuesta mostraron que el tiempo óptimo requerido para la hidrólisis alcalina era el mismo que para la hidrólisis ácida. Sin embargo, el rendimiento del NEPC preparado por hidrólisis alcalina fue mayor, lo que puede deberse a que la hidrólisis alcalina interrumpió más la unión del NEPC con las proteínas estructurales, la fibra dietética, etc. El tratamiento ácido rompe los enlaces glicosídicos y disuelve los azúcares. En condiciones ácidas, los grupos hidroxilo de las moléculas de polifenol se protonan fácilmente, lo que hace que las moléculas de polifenol se rompan y liberen monómeros u oligómeros. La hidrólisis ácida a altas temperaturas puede provocar la pérdida de algunas sustancias fenólicas; en condiciones alcalinas, los grupos hidroxilo de las moléculas de polifenol se desprotonan más fácilmente que en condiciones de hidrólisis ácida, lo que da lugar a rendimientos de hidrólisis alcalina ligeramente superiores y a una reducción de las pérdidas.
Estudios anteriores han encontrado diferencias en el NEPC obtenido mediante hidrólisis alcalina e hidrólisis ácida. El ácido cafeico, las catequinas y los derivados del ácido gálico pueden detectarse en los productos de hidrólisis ácida de la harina, mientras que el ácido ferúlico sólo existe en los productos de hidrólisis alcalina, lo que indica que puede haber más tipos de sustancias fenólicas obtenidas por hidrólisis ácida. Este estudio utilizó UPLC-Q-TOF-MS para analizar la composición de sustancias en los productos de hidrólisis NEPC de las bayas de goji. El cromatograma de iones totales (véase la figura 6) mostró que no había diferencias en los tipos de compuestos entre los productos de hidrólisis alcalina y los de hidrólisis ácida, pero el número de productos de hidrólisis ácida era significativamente mayor que el de los productos de hidrólisis alcalina. Este fenómeno puede deberse a la fácil desprotonación y destrucción de los grupos hidroxilo fenólicos en medios alcalinos fuertes, lo que los hace indetectables por espectrometría de masas, mientras que las sustancias fenólicas son más estables y fáciles de detectar en medios ácidos; por otra parte, la hidrólisis alcalina sólo puede romper los enlaces éster entre los fenoles y las macromoléculas, mientras que los ácidos pueden hidrolizar no sólo los enlaces éster sino también los enlaces glucosídicos, por lo que hay más tipos de sustancias fenólicas que pueden detectarse. Desde el punto de vista de los productos, los principales son los derivados fenilpropanoides. Entre los 11 compuestos identificados, hay 8 fenilpropanoides, 1 cumarina, 1 derivado fenilpropanoide y 1 benzofenona. En el producto de hidrólisis alcalina, sólo pueden identificarse cuatro compuestos, siendo el ácido ferúlico la sustancia principal; Y los 11 compuestos identificados pueden detectarse en los productos de hidrólisis ácida. Cabe destacar que entre los 8 ácidos fenólicos, 2 compuestos pueden ser los productos de la apertura del anillo de lactona de cumarina durante la hidrólisis del NEPC, en lugar de las sustancias nativas de las bayas de goji. Esto puede estar relacionado con la alta concentración de ácidos utilizados en el proceso de hidrólisis. En una fase posterior, la concentración de ácidos o bases puede reducirse para obtener una estructura molecular más completa. Además, el NEPC contenido en las bayas de goji consiste principalmente en ácido fenilpropanoide y componentes cumarínicos. Para saber si existen otros componentes, es necesario analizar más a fondo los productos de la hidrólisis. Para llevar a cabo un análisis en profundidad del NEPC en las bayas de goji, la detección por espectrometría de masas debe utilizarse como guía en la fase posterior, y la concentración de ácido/álcali durante la hidrólisis debe ajustarse para obtener el verdadero NEPC nativo perteneciente a las bayas de goji.
