Exploration du mécanisme d'action potentiel des gélules Bufei Huoxue dans le traitement de la fibrose pulmonaire sur la base de la pharmacologie de réseau
La fibrose pulmonaire (FP) est une maladie pulmonaire interstitielle chronique et irréversible caractérisée par l'activation des fibroblastes pulmonaires en myofibroblastes et la sécrétion de matrice extracellulaire. Cette maladie est la manifestation terminale de diverses maladies pulmonaires, où la structure normale du tissu pulmonaire est perturbée et remplacée par un tissu cicatriciel anormalement réparé. Il existe plusieurs sous-types cliniques de PF, qui se présentent sous la forme d'attaques progressives, parmi lesquels la PF idiopathique est le type le plus courant. La cause de cette maladie est actuellement inconnue, la période de survie est courte et il n'existe pas de traitement spécifique. Le taux d'incidence et la mortalité de la FP augmentent d'année en année, notamment en raison de l'infection répétée de l'interstitium pulmonaire par divers virus respiratoires, ce qui rend la maladie plus jeune. À l'heure actuelle, les connaissances cliniques sur cette maladie sont encore très lacunaires. Bien que deux médicaments, la pirfénidone et le nintedanib, soient largement acceptés dans la pratique clinique, leur efficacité clinique n'est pas satisfaisante.
La PF appartient à la catégorie des maladies de la médecine traditionnelle chinoise telles que l'"obstruction pulmonaire" ou l'"impotence pulmonaire". Au début de la maladie, une toux prolongée entraîne une déficience, qui se manifeste principalement par une "obstruction pulmonaire" due à une déficience du qi ; la maladie continue à se développer et, au stade avancé, il y a une déficience à la fois du qi et du yin, ce qui entraîne un dysfonctionnement des poumons. Une maladie de longue durée entraîne une toux et une respiration sifflante, ce qui épuise le yin des poumons et provoque une chaleur pulmonaire. Le liquide yin peut alors être refoulé, ce qui entraîne la sécheresse et l'assèchement des poumons, la perte de nourriture et, en fin de compte, l'impotence pulmonaire. C'est ce qui est dit dans l'"Essai sur l'impuissance" de Su Wen : "Si les poumons sont chauds et les feuilles brûlées, l'impuissance survient. Cette maladie est d'abord causée par une déficience du qi, ce qui entraîne des diarrhées, des sueurs et un manque de fluides corporels pour nourrir les organes. C'est pourquoi, dans la pratique clinique, la nutrition des poumons et la thérapie du yin sont utilisées pour traiter l'impuissance pulmonaire tout en complétant le qi. Les poumons font face aux cent méridiens et ont pour fonction de transporter l'eau, les grains et l'essence. Lorsque les agents pathogènes de la chaleur endommagent les poumons et que le qi épuise le yin, le transport est perdu et les organes sont privés de nourriture, ce qui entraîne le syndrome d'impuissance.
La capsule Bufei Huoxue (BHC) est fabriquée à partir de principes actifs extraits de l'Astragalus membranaceus, du Paeonia lactiflora et du Fructus Psorale, et est largement utilisée dans la pratique clinique pour les maladies pulmonaires. Le Huangqi a une nature douce et légèrement chaude, qui peut réguler les méridiens de la rate et des poumons. Il a pour fonction de nourrir le corps, de renforcer l'extérieur et de tonifier la rate et le milieu. La pivoine rouge a une nature amère et légèrement froide et appartient au méridien du foie. Elle a pour effet d'éliminer la chaleur, de refroidir le sang, de disperser la stase sanguine et de soulager la douleur ; la psoralea est de nature chaude et appartient aux méridiens des reins et de la rate. Elle a pour fonction de réguler le qi, de soulager l'asthme, de tonifier les reins et de renforcer le yang. Les trois médicaments agissent ensemble pour nourrir les poumons, renforcer les reins, favoriser la circulation sanguine et éliminer la stase sanguine. Cette étude prédit le mécanisme potentiel de l'effet anti-PF du BHC par des méthodes de pharmacologie de réseau et vérifie les résultats de la pharmacologie de réseau par des expériences sur les animaux, enrichissant ainsi la base théorique de la prévention et du traitement de la PF par la médecine traditionnelle chinoise et fournissant une base de recherche pour l'application clinique du BHC.
En tant que maladie, le dysfonctionnement pulmonaire doit être causé par une toux chronique et une respiration sifflante, une déficience du qi du poumon, un dysfonctionnement des organes et le contrôle du qi du corps par les poumons. La circulation des vaisseaux sanguins est défavorable, associée à une insuffisance de la rate et à un excès d'humidité, ce qui conduit finalement à la coagulation des mucosités et à la stase du sang, qui exacerbe à son tour le syndrome de l'insuffisance pulmonaire et forme un cercle vicieux. Il s'agit de la pathogenèse irréversible de la progression clinique de la PF selon la MTC. L'insuffisance du Qi est le facteur déclenchant de l'apparition de la PF et, à mesure que la maladie progresse, la congestion est inévitable aux derniers stades de la maladie. Le Canon intérieur énonce clairement ce qui suit : Lorsque le sang est abondant, il faut le déterminer ; lorsque le qi est déficient, il faut le contrôler et l'induire". Le BHC s'appuie précisément sur cette méthode comme principale méthode de traitement et base théorique pour développer des formulations de médicaments latents.
L'étude susmentionnée a révélé que le BHC exerce une fonction anti-FP en intervenant dans la voie de signalisation du TNF par l'intermédiaire des cibles p38, MMP9 et TNF-α. Le facteur de nécrose tumorale (TNF) a été mis au point dans les années 1970 par E. A. Carswell et son équipe de recherche, qui ont découvert que le TNF, synthétisé et sécrété par les macrophages mononucléaires, n'avait pas été spécifiquement défini avant 1958. Par la suite, les scientifiques ont progressivement découvert que d'autres cellules, dont les cellules NK et les lymphocytes T, pouvaient également produire du TNF. La recherche a montré que le TNF-α est étroitement impliqué dans la réponse inflammatoire des tissus locaux, principalement parce qu'il peut promouvoir la production de substances inflammatoires représentées par les corps NLRP3, induire l'activation des fibroblastes pulmonaires et sécréter la matrice extracellulaire. Parallèlement, le TNF-α peut également exacerber les lésions inflammatoires, ce qui se manifeste par sa capacité à agir seul ou en conjonction avec les compléments C3A et C5A, en exerçant des effets cytotoxiques. En résumé, le TNF-α joue un rôle crucial dans la formation et le développement de la FP. Les MMP sont des protéases dépendantes du zinc dont la fonction principale est de dégrader l'ECM. Après leur première découverte en 1961, de nombreuses protéases de la même famille ont été découvertes. Dans des conditions normales, l'activité de la MMP9 est très faible. Après activation de la protéine, elle est principalement responsable de la dégradation de la MEC. Il a été confirmé que l'activité de la MMP9 est significativement augmentée dans le tissu pulmonaire des patients atteints de PF, et que son contenu est significativement augmenté dans le liquide de lavage broncho-alvéolaire. La raison principale est l'élimination adaptative des effets néfastes de la sécrétion de la MEC. Ces dernières années, on a découvert que divers processus biologiques étaient associés à la formation de la maladie de la FP, parmi lesquels la protéine p38, qui est étroitement liée à l'apoptose et au cycle cellulaire, a fait l'objet d'une attention croissante. Synthétisée dans les cellules épithéliales alvéolaires de type II, les macrophages pulmonaires mononucléaires et les cellules endothéliales, la protéine p38 participe à de multiples étapes de la formation de la FP en jouant un rôle de médiateur dans l'infiltration des cellules inflammatoires, la différenciation des fibroblastes et d'autres processus. En lisant la littérature pertinente de ces dernières années, on a découvert que le processus de la FP médiée par p38 implique principalement les points suivants : premièrement, il est bien connu que le TGF-β est une molécule clé dans la formation de la FP. p38 favorise la synthèse du TGF-β, induit la transition épithélio-mésenchymateuse (EMT) dans les cellules épithéliales alvéolaires, et participe à la formation de la FP en activant les fibroblastes. Deuxièmement, p38 régule l'activité de la protéine NF - κ B et participe à la pathogenèse de la FP. NF - κ B est une protéine de liaison à l'ADN composée des sous-unités p65 et p50 de la famille des protéines Rel. C'est un régulateur de transcription important dans les cellules eucaryotes et il peut participer à la régulation de la réponse immunitaire dans l'inflammation alvéolaire pulmonaire précoce (PF) en favorisant la transcription des gènes inflammatoires et des gènes TGF-β. Troisièmement, p38 joue un rôle crucial dans la prolifération et la différenciation des fibroblastes, ainsi que dans le dépôt de la matrice extracellulaire. Dans les myofibroblastes survivants, p38 participe à la dégradation de la matrice extracellulaire PF en favorisant la transcription de l'ARNm des MMP.
L'analyse ci-dessus montre que les trois protéines exprimées de manière différentielle (TNF-α, MMP-9, p38) dans cette étude sont toutes situées en amont et en aval de la voie de signalisation du TNF, et que leur expression est étroitement liée à l'apparition et au développement de la polyarthrite rhumatoïde. De multiples aspects et voies de signalisation sont impliqués dans les changements de biologie moléculaire de la fibrose kystique. Il ressort de ce qui précède que les interventions de la médecine traditionnelle chinoise se caractérisent par des effets multi-cibles et multi-voies. Dans le même temps, les différentes voies sont étroitement liées, s'influençant et se régulant mutuellement. Cela reflète également le concept global des effets de la médecine traditionnelle chinoise. Cette étude a révélé que les changements de trois protéines (TNF-α, MMP-9, p38) présentaient une expression élevée significative dans le groupe modèle. Avec les changements de dose, l'expression des protéines a également montré des changements de gradient et une dépendance à la concentration. La partie expérimentale a non seulement indiqué la direction à suivre pour nos recherches ultérieures, mais a également vérifié la validité scientifique des résultats de l'analyse d'enrichissement dans notre section précédente sur la pharmacologie des réseaux.


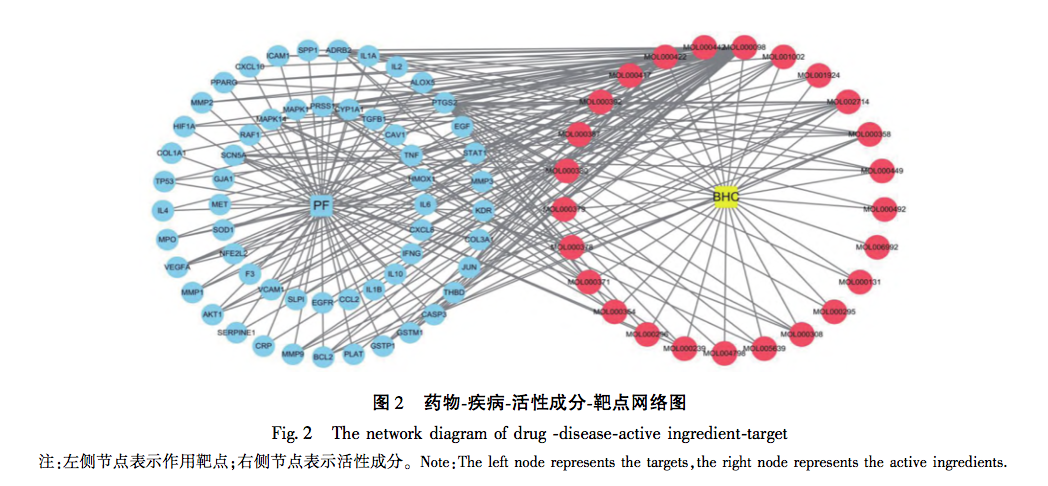
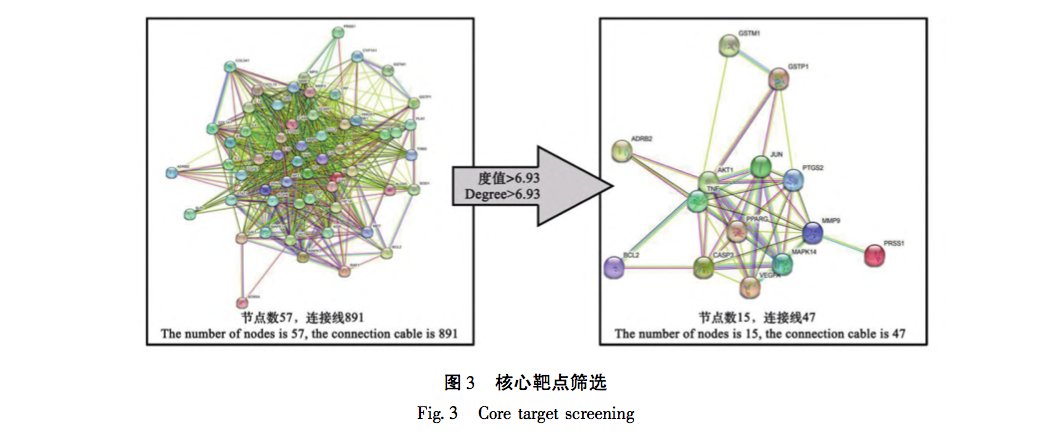
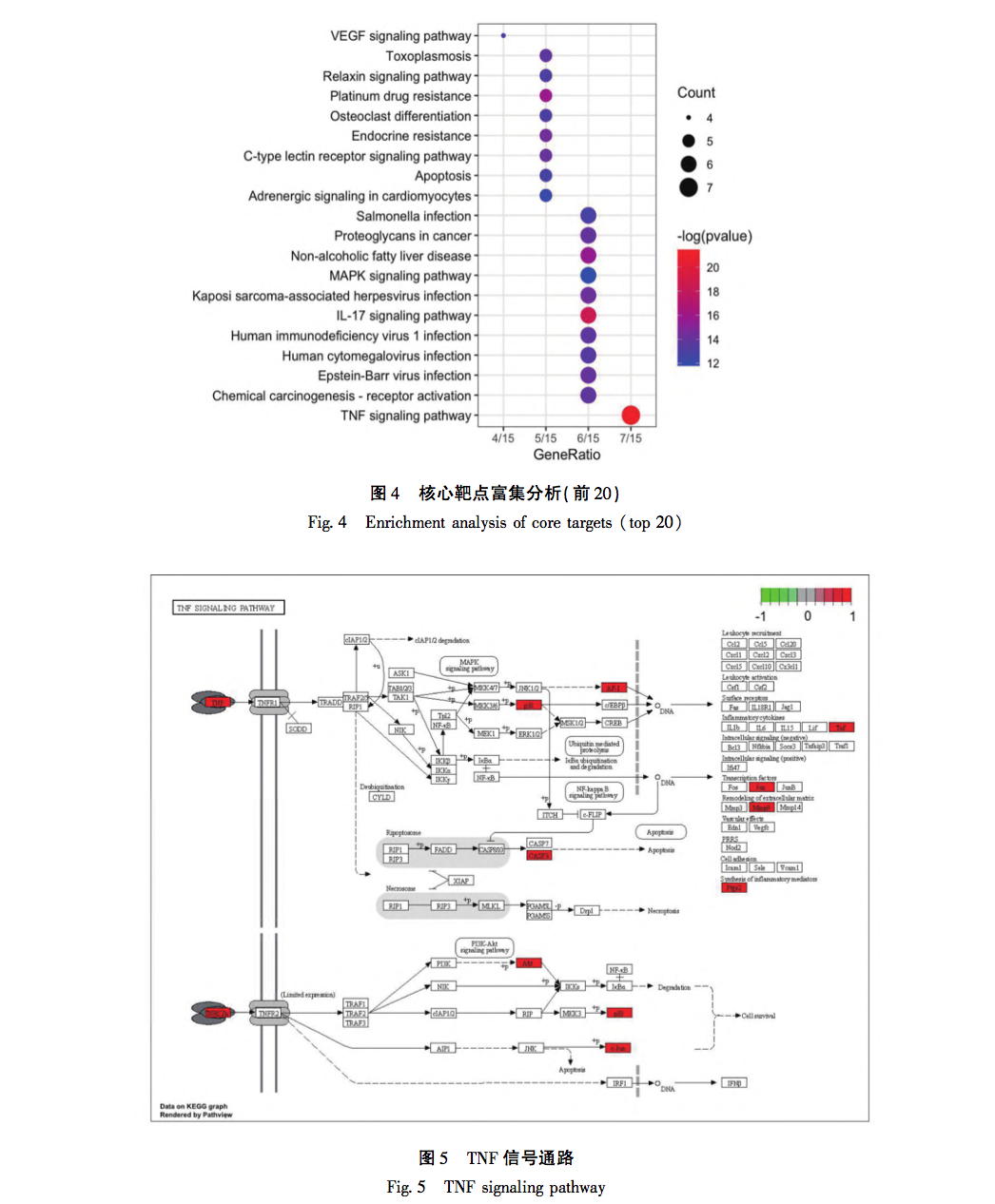
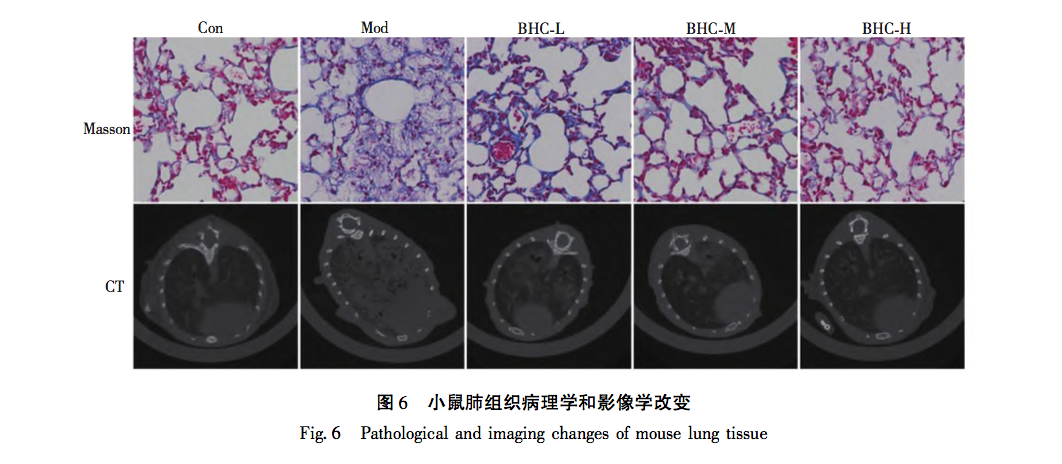
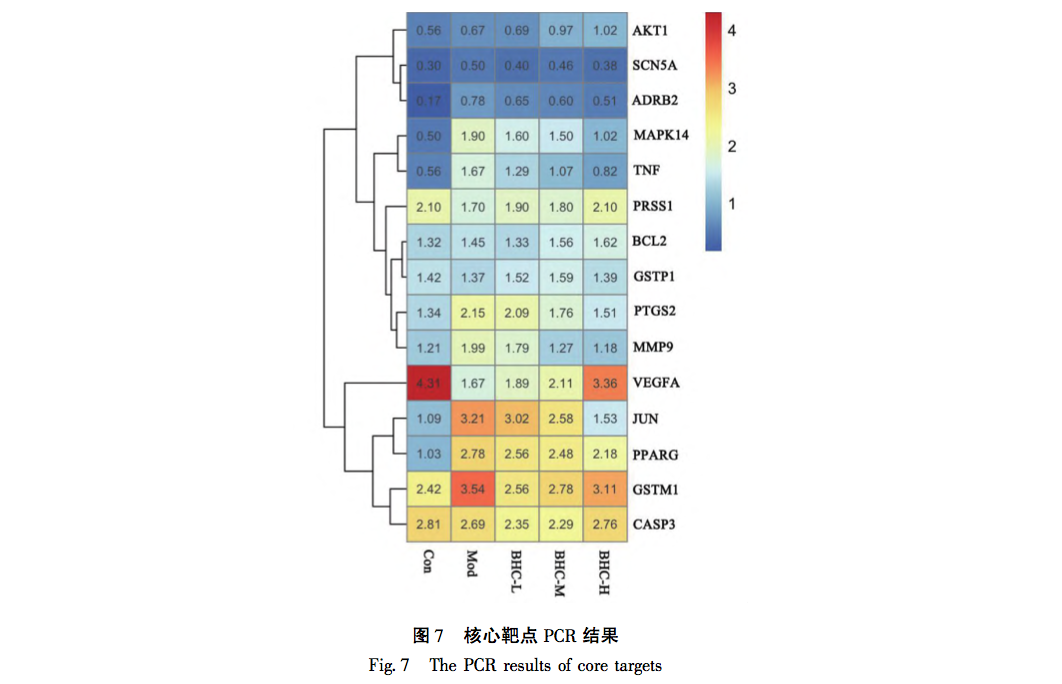
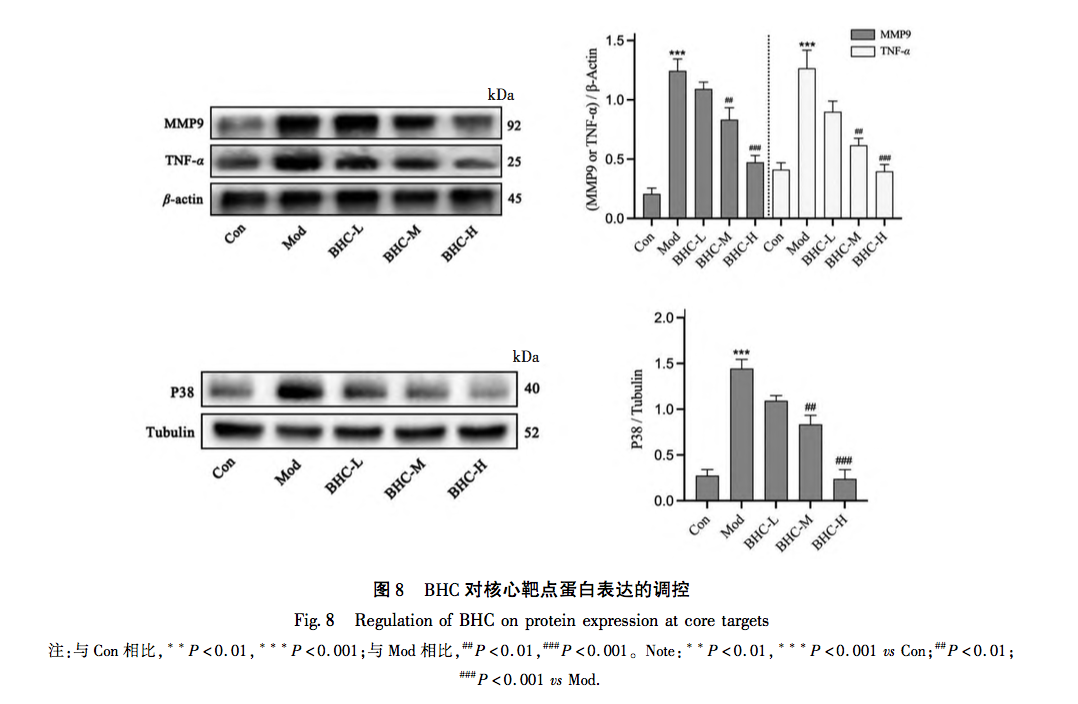 Le BHC concerné par cette étude est principalement traité par la méthode de promotion de la circulation sanguine et d'élimination de la stase sanguine. En raison de la rareté de la maladie et de la complexité de son étiologie, il existe actuellement relativement peu de données épidémiologiques actualisées sur la PF. Cependant, sur le plan clinique, son taux d'incidence augmente de manière significative, ce qui peut être dû à l'existence à long terme d'un nouveau coronavirus, à des infections répétées et à d'autres facteurs, qui stimulent de manière répétée l'interstitium pulmonaire. Bien que des progrès significatifs aient été réalisés dans le traitement du COVID-19, il reste encore de nombreux problèmes à résoudre pour les séquelles à long terme de ces patients, en particulier pour le traitement de la PF. Comme on le sait, la FP est le résultat final de la lente progression de nombreuses maladies pulmonaires, notamment la broncho-pneumopathie chronique obstructive (BPCO), la bronchectasie et l'emphysème. Aux premiers stades de la FP, elle est principalement due à la stagnation du qi et du sang, à une mauvaise circulation du qi et du sang et à un manque d'alimentation des poumons. Les caractéristiques de ce stade sont une apparition rapide, un cycle court et un contrôle facile. Par conséquent, le traitement précoce doit se concentrer sur la promotion de la circulation sanguine et l'élimination de la stase sanguine, complétées par la nutrition du qi et du yin. Chez les patients atteints d'une PF en phase terminale, l'insuffisance du qi et l'essoufflement, la faiblesse des défenses superficielles et la fragilité des poumons sont plus susceptibles d'être envahis par des agents pathogènes externes. Les caractéristiques de ce stade sont une progression lente de la maladie, un cycle long et une inversion difficile. À ce stade, la stratégie de traitement doit principalement se concentrer sur l'alimentation du qi et du yin, complétée par la promotion de la circulation sanguine et l'élimination de la stase sanguine. Le modèle animal utilisé dans cette étude correspond au stade d'apparition précoce et aiguë de la PF, et le traitement doit principalement se concentrer sur la promotion de la circulation sanguine et l'élimination de la stase sanguine, ce qui est conforme à l'efficacité du BHC. Cette étude révèle indirectement l'efficacité et la scientificité du BHC et fournit également une orientation pour les recherches futures de notre groupe de recherche.
Le BHC concerné par cette étude est principalement traité par la méthode de promotion de la circulation sanguine et d'élimination de la stase sanguine. En raison de la rareté de la maladie et de la complexité de son étiologie, il existe actuellement relativement peu de données épidémiologiques actualisées sur la PF. Cependant, sur le plan clinique, son taux d'incidence augmente de manière significative, ce qui peut être dû à l'existence à long terme d'un nouveau coronavirus, à des infections répétées et à d'autres facteurs, qui stimulent de manière répétée l'interstitium pulmonaire. Bien que des progrès significatifs aient été réalisés dans le traitement du COVID-19, il reste encore de nombreux problèmes à résoudre pour les séquelles à long terme de ces patients, en particulier pour le traitement de la PF. Comme on le sait, la FP est le résultat final de la lente progression de nombreuses maladies pulmonaires, notamment la broncho-pneumopathie chronique obstructive (BPCO), la bronchectasie et l'emphysème. Aux premiers stades de la FP, elle est principalement due à la stagnation du qi et du sang, à une mauvaise circulation du qi et du sang et à un manque d'alimentation des poumons. Les caractéristiques de ce stade sont une apparition rapide, un cycle court et un contrôle facile. Par conséquent, le traitement précoce doit se concentrer sur la promotion de la circulation sanguine et l'élimination de la stase sanguine, complétées par la nutrition du qi et du yin. Chez les patients atteints d'une PF en phase terminale, l'insuffisance du qi et l'essoufflement, la faiblesse des défenses superficielles et la fragilité des poumons sont plus susceptibles d'être envahis par des agents pathogènes externes. Les caractéristiques de ce stade sont une progression lente de la maladie, un cycle long et une inversion difficile. À ce stade, la stratégie de traitement doit principalement se concentrer sur l'alimentation du qi et du yin, complétée par la promotion de la circulation sanguine et l'élimination de la stase sanguine. Le modèle animal utilisé dans cette étude correspond au stade d'apparition précoce et aiguë de la PF, et le traitement doit principalement se concentrer sur la promotion de la circulation sanguine et l'élimination de la stase sanguine, ce qui est conforme à l'efficacité du BHC. Cette étude révèle indirectement l'efficacité et la scientificité du BHC et fournit également une orientation pour les recherches futures de notre groupe de recherche.
