Undersøgelse af den potentielle virkningsmekanisme for Bufei Huoxue Capsules i behandlingen af lungefibrose baseret på netværksfarmakologi
Lungefibrose (PF) er en kronisk, irreversibel interstitiel lungesygdom, der er kendetegnet ved aktivering af lungefibroblaster til myofibroblaster og udskillelse af ekstracellulær matrix. Denne sygdom er slutstadiet af forskellige lungesygdomme, hvor den normale lungevævsstruktur forstyrres og erstattes af unormalt repareret arvæv. Der findes forskellige kliniske undertyper af PF, der viser sig som progressive angreb, hvoraf idiopatisk PF er den mest almindelige type. Årsagen til denne sygdom er i øjeblikket ukendt, med en kort overlevelsesperiode og ingen specifikke behandlingsmidler til rådighed. Forekomsten og dødeligheden af PF stiger år for år, især den gentagne infektion af pulmonale interstitielle af forskellige respiratoriske vira, hvilket gør sygdommen mere ung. På nuværende tidspunkt er der stadig en stor mangel på viden om sygdommen i klinikken. Selv om to lægemidler, pirfenidon og nintedanib, er bredt accepteret i klinisk praksis, er deres kliniske effekt ikke tilfredsstillende.
PF hører til kategorien af traditionelle kinesiske medicinsygdomme som "lungeobstruktion" eller "lungeimpotens". Ved sygdommens begyndelse fører langvarig hoste til mangel, hovedsageligt manifesteret som "lungeobstruktion" på grund af qi-mangel; Sygdommen fortsætter med at udvikle sig, og i det sene stadium er der en mangel på både qi og yin, hvilket resulterer i lungedysfunktion. Langvarig sygdom fører til hoste og hvæsende vejrtrækning, som udtømmer lungernes yin og forårsager lungevarme. Det kan få yin-væsken til at løbe tilbage, hvilket resulterer i tørhed og tørhed i lungerne, tab af næring og i sidste ende fører til lungeimpotens. Dette er, hvad der siges i Su Wens "Essay om impotens": "Hvis lungerne er varme, og bladene er brændte, ... så vil der opstå impotens." Denne sygdom skyldes først og fremmest qi-mangel, som fører til diarré, svedtendens og mangel på kropsvæsker, der kan give næring til organerne. Derfor bruger man i klinisk praksis næring til lungerne og yin-terapi til at behandle pulmonal impotens, samtidig med at man supplerer qi. Lungerne vender ud mod de hundrede meridianer og har til opgave at transportere vand, korn og essens. Når varmepatogener skader lungerne, og qi udtømmer yin, går transporten tabt, og organerne får ikke næring, hvilket resulterer i impotenssyndrom.
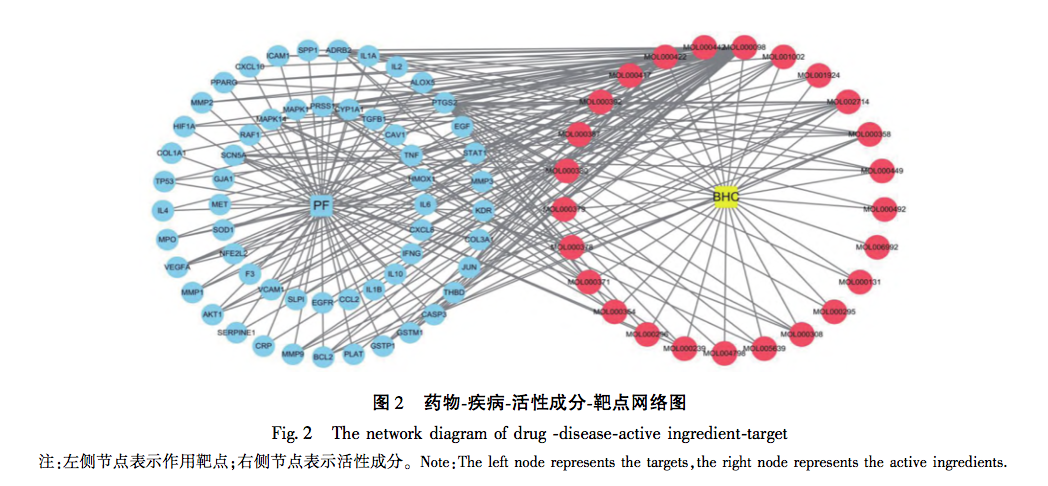
Bufei Huoxue Capsule (BHC) er fremstillet af aktive ingredienser udvundet af Astragalus membranaceus, Paeonia lactiflora og Fructus Psorale og anvendes i vid udstrækning i klinisk praksis til behandling af lungesygdomme. Huangqi har en sød og lidt varm karakter, som kan regulere milt- og lungemeridianerne. Den nærer kroppen, styrker det ydre og tonificerer milten og midten; rød pæon har en bitter og lidt kold natur og hører til levermeridianen. Den fjerner varme, køler blodet, opløser blodstasis og lindrer smerter; Psoralea har en varm natur og vender tilbage til nyre- og miltmeridianerne. Den har til formål at regulere qi, lindre astma, tonificere nyrerne og styrke yang. De tre lægemidler arbejder sammen om at give næring til lungerne, styrke nyrerne, fremme blodcirkulationen og fjerne blodstasis. Denne undersøgelse forudsiger den potentielle mekanisme for BHC's anti-PF-effekt gennem netværksfarmakologiske metoder og verificerer resultaterne af netværksfarmakologi gennem dyreforsøg, hvilket beriger det teoretiske grundlag for traditionel kinesisk medicins forebyggelse og behandling af PF og giver forskningsgrundlag for den kliniske anvendelse af BHC.
Som en sygdom skal lungedysfunktion være forårsaget af kronisk hoste og hvæsende vejrtrækning, lunge qi-mangel, dysfunktion af organer og lungerne, der kontrollerer kroppens qi. Cirkulationen af blodkar er ugunstig, kombineret med miltmangel og overdreven fugt, hvilket i sidste ende fører til slimkoagulation og blodstase, hvilket igen forværrer syndromet med lungemangel og danner en ond cirkel. Dette er den irreversible TCM-patogenese af den kliniske udvikling af PF. Qi-mangel er den udløsende faktor for udbruddet af PF, og efterhånden som sygdommen skrider frem, er overbelastning uundgåelig i de sidste stadier af sygdommen. Den indre kanon siger det klart: "Når der er rigeligt med blod, skal det bestemmes; når der er mangel på qi, skal det kontrolleres og induceres.". BHC er netop baseret på denne metode som den vigtigste behandlingsmetode og det teoretiske grundlag for udvikling af latente lægemiddelformuleringer.
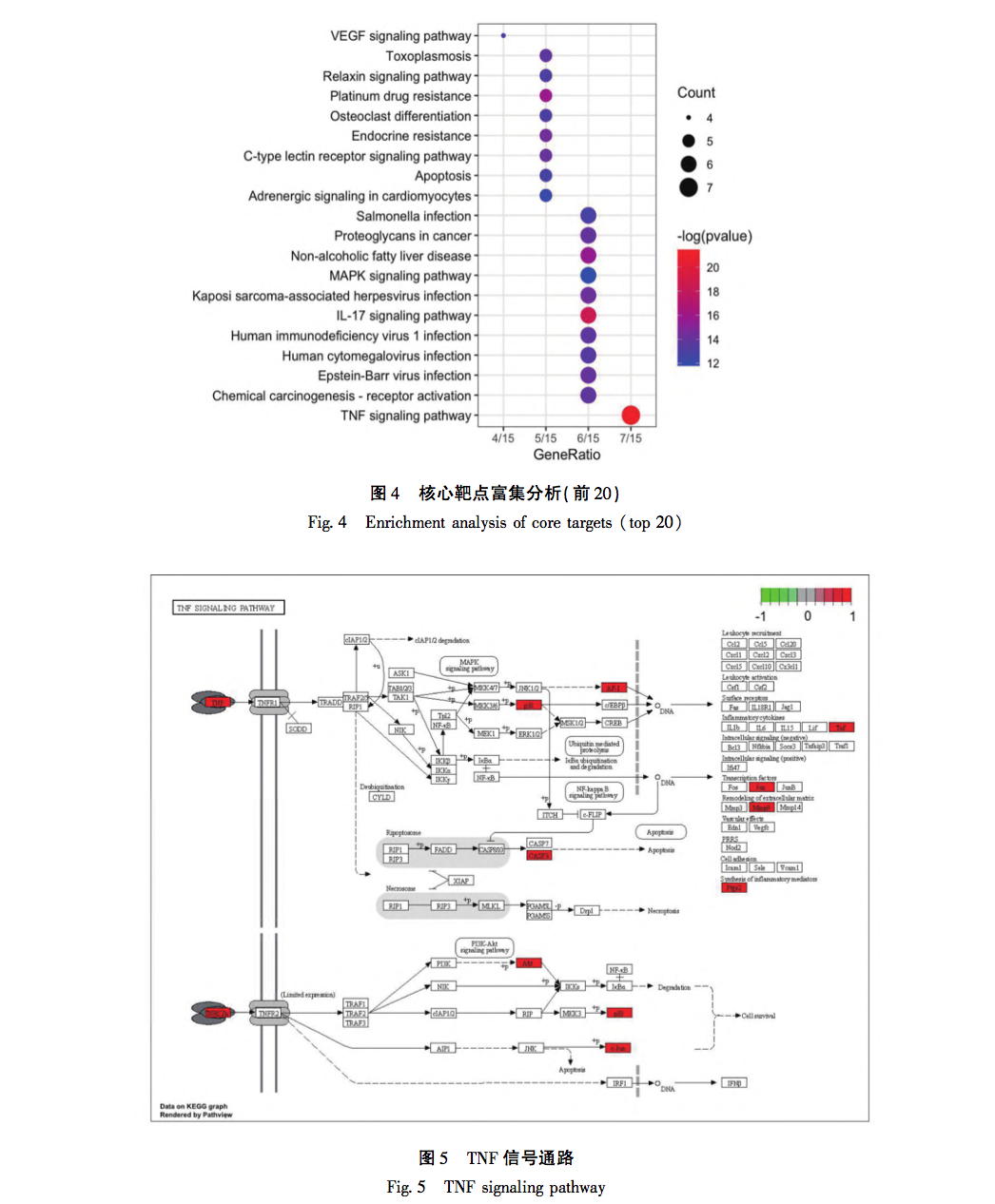
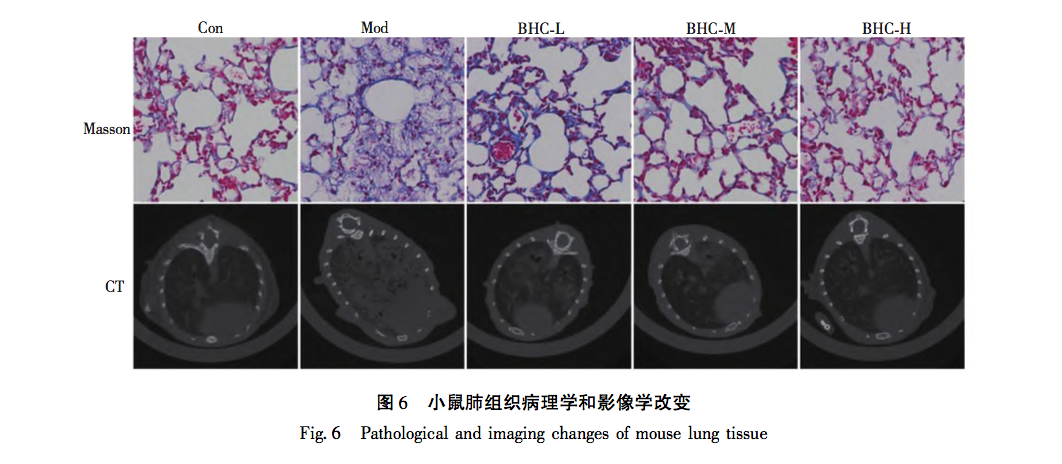
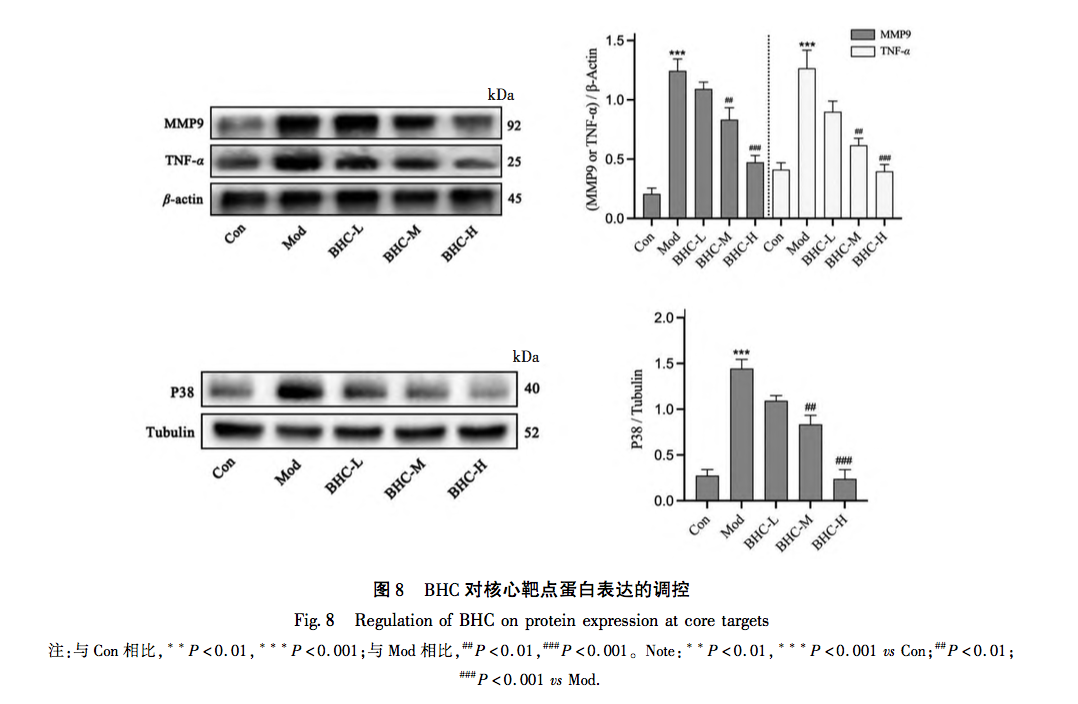
Ovenstående undersøgelse viste, at BHC udøver anti-PF-funktion ved at gribe ind i TNF-signalvejen gennem p38-, MMP9- og TNF-α-mål. Tumornekrosefaktor (TNF) blev udviklet i 1970'erne af E A. Carswell og hans forskerteam, der opdagede, at TNF, som syntetiseres og udskilles af mononukleære makrofager, ikke blev defineret specifikt før 1958. Efterfølgende opdagede forskerne gradvist, at andre celler, herunder NK-celler og T-lymfocytter, også kan producere TNF. Forskning har vist, at TNF - α er tæt involveret i den inflammatoriske reaktion i lokale væv, hovedsageligt fordi det kan fremme produktionen af inflammatoriske stoffer repræsenteret af NLRP3-legemer, fremkalde aktivering af lungefibroblaster og udskille ekstracellulær matrix. Samtidig kan TNF - α også forværre inflammatoriske skader, hvilket kommer til udtryk i dens evne til at virke alene eller sammen med komplement C3A og C5A og udøve cytotoksiske virkninger. Sammenfattende spiller TNF - α en afgørende rolle i dannelsen og udviklingen af PF. MMP'er er zinkafhængige proteaser, hvis hovedfunktion er at nedbryde ECM. Efter deres første opdagelse i 1961 er der blevet opdaget flere proteaser i samme familie. Under normale forhold er aktiviteten af MMP9 meget lav. Efter proteinaktivering er den hovedsageligt ansvarlig for nedbrydningen af ECM. Det er blevet bekræftet, at aktiviteten af MMP9 er markant forøget i lungevæv hos PF-patienter, og indholdet er markant forøget i bronchoalveolær skyllevæske. Hovedårsagen er at eliminere de negative virkninger af ECM-sekretion på en adaptiv måde. I de senere år har det vist sig, at forskellige biologiske processer er forbundet med dannelsen af PF-sygdom, blandt hvilke p38-protein, der er tæt knyttet til celleapoptose og cellecyklus, har fået stigende opmærksomhed. P38, der syntetiseres i type II alveolære epitelceller, mononukleære pulmonale makrofager og endotelceller, deltager i flere stadier af PF-dannelse ved at formidle inflammatorisk celleinfiltration, fibroblastdifferentiering og andre processer. Ved at læse relevant litteratur i de senere år fandt man ud af, at processen med p38-medieret PF hovedsageligt involverer følgende punkter: For det første er det velkendt, at TGF - β er et nøglemolekyle i PF-dannelse. p38 fremmer syntesen af TGF - β, inducerer epithelial mesenchymal transition (EMT) i alveolære epithelceller og deltager i dannelsen af PF ved at aktivere fibroblaster. For det andet regulerer p38 aktiviteten af NF - κ B-proteinet og deltager i patogenesen af PF. NF-κ B er et DNA-bindende protein, der består af p65- og p50-underenhederne i Rel-proteinfamilien. Det er en vigtig transkriptionsregulator i eukaryote celler og kan deltage i reguleringen af immunrespons i tidlig pulmonal alveolær inflammation (PF) ved at fremme transkriptionen af inflammatoriske gener og TGF - β-gener. For det tredje spiller p38 en afgørende rolle i spredningen og differentieringen af fibroblaster samt i aflejringen af ekstracellulær matrix. I overlevende myofibroblaster deltager p38 i nedbrydningen af PF ekstracellulær matrix ved at fremme mRNA-transkription af MMP'er.
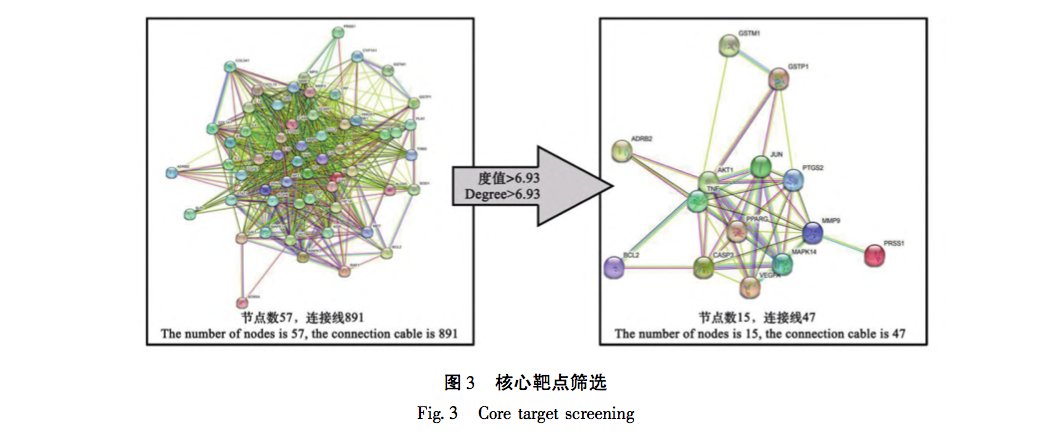
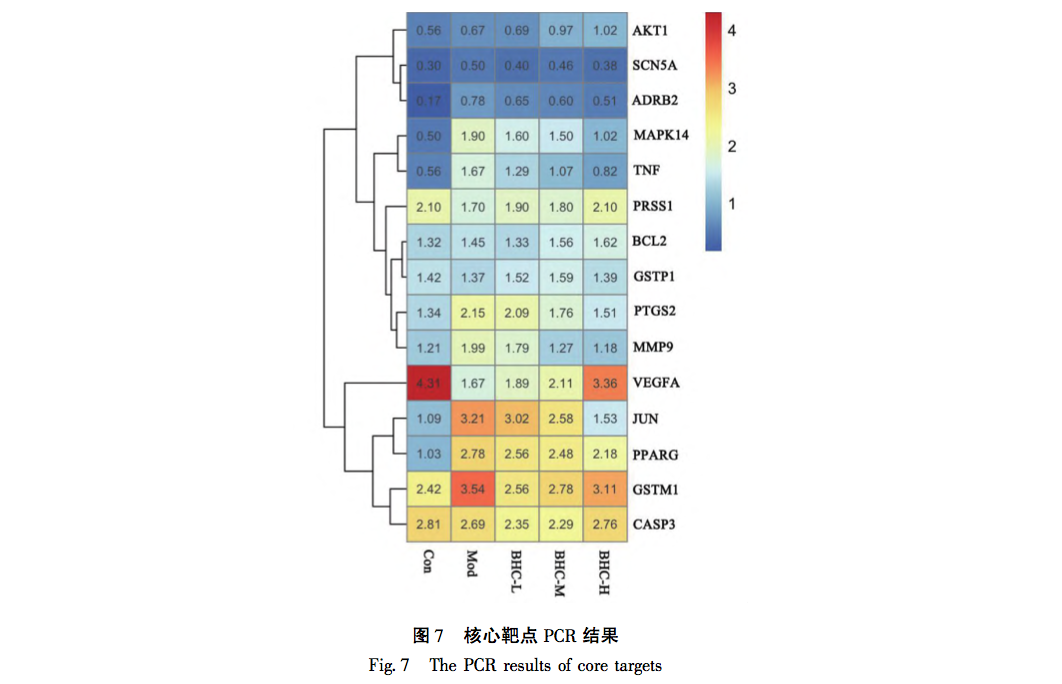
Ud fra ovenstående analyse kan man se, at de tre forskelligt udtrykte proteiner (TNF - α, MMP-9, p38) i denne undersøgelse alle er placeret ved opstrøms- og nedstrøms-knudepunkter i TNF-signalvejen, og deres udtryk er tæt forbundet med forekomsten og udviklingen af PF. Flere aspekter og signalveje er involveret i de molekylærbiologiske ændringer af PF. Ud fra dette kan man se, at kendetegnene ved traditionel kinesisk medicinintervention er multi-target og multi pathway-effekter. Samtidig er de forskellige veje tæt forbundne og påvirker og regulerer hinanden. Det afspejler også det overordnede koncept for virkningerne af traditionel kinesisk medicin. I denne undersøgelse blev det konstateret, at ændringerne i tre proteiner (TNF - α, MMP-9, p38) viste signifikant højt udtryk i modelgruppen. Med ændringer i dosis udviste proteinudtrykket også gradientændringer og koncentrationsafhængighed. Den eksperimentelle del pegede ikke kun på retningen for vores efterfølgende forskning, men bekræftede også den videnskabelige validitet af berigelsesanalyseresultaterne i vores tidligere afsnit om netværksfarmakologi.


 Den BHC, der er involveret i denne undersøgelse, behandles hovedsageligt med metoden til at fremme blodcirkulationen og fjerne blodstasis. På grund af sygdommens sjældenhed og kompleksiteten i dens ætiologi er der i øjeblikket relativt få opdaterede epidemiologiske data om PF. Klinisk set stiger forekomsten dog betydeligt, hvilket kan skyldes den langsigtede eksistens af nyt coronavirus, gentagne infektioner og andre faktorer, som gentagne gange stimulerer lungeinterstitiet. Selvom der er gjort betydelige fremskridt i behandlingen af COVID-19, er der stadig mange problemer, der skal løses for de langsigtede følger af sådanne patienter, især til behandling af PF. Som bekendt er PF det endelige resultat af den langsomme udvikling af mange lungesygdomme, herunder kronisk obstruktiv lungesygdom (KOL), bronkiektasi og emfysem. I de tidlige stadier af PF er det hovedsageligt forårsaget af qi-stagnation og blodstasis, dårlig cirkulation af qi og blod og mangel på lungenæring. Kendetegnene for dette stadie er hurtig debut, kort cyklus og nem kontrol. Derfor bør tidlig behandling fokusere på at fremme blodcirkulationen og fjerne blodstasis, suppleret med nærende qi og yin; Hos PF-patienter i slutstadiet er qi-mangel og åndenød, svagt overfladeforsvar og sarte lunger mere modtagelige for invasion af eksterne patogener. Egenskaberne ved dette trin er langsom sygdomsprogression, lang cyklus og vanskelig reversering. I denne fase bør behandlingsstrategien primært fokusere på at give næring til qi og yin, suppleret med at fremme blodcirkulationen og fjerne blodstasis. Den dyremodel, der er involveret i denne undersøgelse, er i overensstemmelse med den tidlige akutte fase af PF, og behandlingen bør primært fokusere på at fremme blodcirkulationen og fjerne blodstasis, hvilket er i tråd med effekten af BHC. Dette afslører indirekte effektiviteten og videnskabeligheden af BHC og giver også en retning for vores forskningsgruppes fremtidige forskning.
Den BHC, der er involveret i denne undersøgelse, behandles hovedsageligt med metoden til at fremme blodcirkulationen og fjerne blodstasis. På grund af sygdommens sjældenhed og kompleksiteten i dens ætiologi er der i øjeblikket relativt få opdaterede epidemiologiske data om PF. Klinisk set stiger forekomsten dog betydeligt, hvilket kan skyldes den langsigtede eksistens af nyt coronavirus, gentagne infektioner og andre faktorer, som gentagne gange stimulerer lungeinterstitiet. Selvom der er gjort betydelige fremskridt i behandlingen af COVID-19, er der stadig mange problemer, der skal løses for de langsigtede følger af sådanne patienter, især til behandling af PF. Som bekendt er PF det endelige resultat af den langsomme udvikling af mange lungesygdomme, herunder kronisk obstruktiv lungesygdom (KOL), bronkiektasi og emfysem. I de tidlige stadier af PF er det hovedsageligt forårsaget af qi-stagnation og blodstasis, dårlig cirkulation af qi og blod og mangel på lungenæring. Kendetegnene for dette stadie er hurtig debut, kort cyklus og nem kontrol. Derfor bør tidlig behandling fokusere på at fremme blodcirkulationen og fjerne blodstasis, suppleret med nærende qi og yin; Hos PF-patienter i slutstadiet er qi-mangel og åndenød, svagt overfladeforsvar og sarte lunger mere modtagelige for invasion af eksterne patogener. Egenskaberne ved dette trin er langsom sygdomsprogression, lang cyklus og vanskelig reversering. I denne fase bør behandlingsstrategien primært fokusere på at give næring til qi og yin, suppleret med at fremme blodcirkulationen og fjerne blodstasis. Den dyremodel, der er involveret i denne undersøgelse, er i overensstemmelse med den tidlige akutte fase af PF, og behandlingen bør primært fokusere på at fremme blodcirkulationen og fjerne blodstasis, hvilket er i tråd med effekten af BHC. Dette afslører indirekte effektiviteten og videnskabeligheden af BHC og giver også en retning for vores forskningsgruppes fremtidige forskning.
