Étude du mécanisme d'action de la médecine tibétaine Weng Bu sur la colite ulcéreuse
Le wengbu est un médicament tibétain traditionnel, qui provient des feuilles tendres de diverses plantes de Myricaria, Tamaricaceae, et qui est largement répandu dans le Xizang, le Qinghai, le Yunnan et d'autres endroits. La recherche moderne a montré que les principaux composants chimiques du Wenbu sont des flavonoïdes et des composés polyphénoliques. Ses parties médicinales sont des branches tendres, de couleur verte, de nature plate et au goût légèrement amer. Il est utilisé pour traiter la maladie de l'eau jaune, la chaleur toxique de la cavité interne et les éruptions cutanées dispersées. Il est également utilisé pour traiter des maladies telles que la peste, la chaleur du sang, le syndrome de la chaleur toxique, l'opacité de la rougeole et les maux de gorge. La pathogénie fondamentale de la "diarrhée chronique" est l'accumulation d'une insuffisance de la rate, d'une chaleur humide et d'une disharmonie entre le qi et le sang, tandis que la "chaleur du sang" est un facteur pathogène important dans la phase active de la colite ulcéreuse. La recherche pharmacologique moderne a montré que l'onbu a également des effets antibactériens, anti-inflammatoires, analgésiques, antirhumatismaux, anti-fatigue et antioxydants.
La colite ulcéreuse (CU) est une maladie inflammatoire chronique du côlon dont l'étiologie n'est pas claire. Les lésions sont limitées à la muqueuse et à la sous-muqueuse du gros intestin et les principaux symptômes sont les douleurs abdominales, la diarrhée, les selles muqueuses purulentes et sanglantes, etc. L'affection est sujette à récidive et difficile à guérir. Les immunosuppresseurs, les corticostéroïdes et les préparations à base d'aminosalicylate de sodium sont actuellement les principaux moyens de traiter la RCH, avec des effets thérapeutiques significatifs à court terme, mais il existe des problèmes tels que des effets indésirables importants et l'impossibilité de maintenir le traitement. On ne sait pas encore si l'Onbu a un effet thérapeutique sur la RCH. Cette étude vise à explorer l'effet et le mécanisme de la médecine tibétaine Ongbu dans le traitement de la RCH grâce à la technologie UHPLC-Q-Exactive-Orbitrap-MS, à la pharmacologie de réseau, à l'amarrage moléculaire et à l'expérimentation animale, fournissant ainsi une référence pour le développement et l'utilisation rationnels de l'Ongbu.












 Cette étude a utilisé la technologie UHPLC-Q-Exactive-Orbitrap-MS pour analyser 171 composants du Wenbu, et a criblé 23 composants actifs du Wenbu par le biais de la plateforme TCMSP. D'après le diagramme du réseau "Weng Bu Active Ingredient UC", les 5 premiers composants ayant le plus de cibles correspondantes sont le pyréthroïde, le pyréthroïde déméthylé, la rhéine, l'isorhamnétine et l'acide tannique. Les recherches de He et al. montrent que l'acide tannique a des effets pharmacologiques tels que des propriétés antioxydantes et anti-inflammatoires. Zheng et al. ont découvert que l'acide tannique réduit de manière significative la libération de TNF-α, IL-1 β et NO en inhibant des voies telles que MAPK/I κ B - α/NF - κ B/COX, améliorant ainsi la RCH. La rhéine a des activités antitumorales, antibactériennes et anti-inflammatoires, et des études ont montré qu'elle peut inhiber la transmission des signaux inflammatoires en inhibant des protéines cibles telles que JAK2, réduire la libération de facteurs inflammatoires et atténuer la réponse inflammatoire causée par une fonction immunitaire anormale dans la RCH. L'isorhamnétine (ISO) est un composé flavonoïde naturel de petite taille, largement présent dans diverses plantes, qui possède de multiples fonctions biologiques telles que des effets anti-inflammatoires et antiviraux. L'ISO peut exercer des effets anti-inflammatoires et thérapeutiques sur l'entérite inflammatoire en inhibant l'activité de la MPO, en inhibant la libération de médiateurs pro-inflammatoires (TNF-α, IL-2, IL-6) et en régulant à la baisse la voie de signalisation NF- κ B. La lactone de scutellaire peut inhiber l'activation de l'inflammasome NLRP3 et la pyroptose cellulaire, exerçant ainsi des effets anti-inflammatoires in vivo.
Cette étude a utilisé la technologie UHPLC-Q-Exactive-Orbitrap-MS pour analyser 171 composants du Wenbu, et a criblé 23 composants actifs du Wenbu par le biais de la plateforme TCMSP. D'après le diagramme du réseau "Weng Bu Active Ingredient UC", les 5 premiers composants ayant le plus de cibles correspondantes sont le pyréthroïde, le pyréthroïde déméthylé, la rhéine, l'isorhamnétine et l'acide tannique. Les recherches de He et al. montrent que l'acide tannique a des effets pharmacologiques tels que des propriétés antioxydantes et anti-inflammatoires. Zheng et al. ont découvert que l'acide tannique réduit de manière significative la libération de TNF-α, IL-1 β et NO en inhibant des voies telles que MAPK/I κ B - α/NF - κ B/COX, améliorant ainsi la RCH. La rhéine a des activités antitumorales, antibactériennes et anti-inflammatoires, et des études ont montré qu'elle peut inhiber la transmission des signaux inflammatoires en inhibant des protéines cibles telles que JAK2, réduire la libération de facteurs inflammatoires et atténuer la réponse inflammatoire causée par une fonction immunitaire anormale dans la RCH. L'isorhamnétine (ISO) est un composé flavonoïde naturel de petite taille, largement présent dans diverses plantes, qui possède de multiples fonctions biologiques telles que des effets anti-inflammatoires et antiviraux. L'ISO peut exercer des effets anti-inflammatoires et thérapeutiques sur l'entérite inflammatoire en inhibant l'activité de la MPO, en inhibant la libération de médiateurs pro-inflammatoires (TNF-α, IL-2, IL-6) et en régulant à la baisse la voie de signalisation NF- κ B. La lactone de scutellaire peut inhiber l'activation de l'inflammasome NLRP3 et la pyroptose cellulaire, exerçant ainsi des effets anti-inflammatoires in vivo.
Le criblage des technologies pharmacologiques en réseau a permis d'identifier 285 cibles d'Onbu, dont 2 415 cibles pour la colite ulcéreuse. Après intersection, 111 cibles potentielles pour le traitement de la colite ulcéreuse ont été obtenues. En construisant le réseau "Onbu Active Ingredient UC", le mécanisme moléculaire de l'Onbu dans le traitement de la colite ulcéreuse a été révélé ; en prédisant les cibles clés de l'Onbu dans le traitement de la colite ulcéreuse par le biais de réseaux d'interactions protéiques, l'analyse du réseau PPI a révélé que l'Onbu peut exercer des effets thérapeutiques sur la colite ulcéreuse en régulant les protéines cibles telles que TNF, CASP3, EGFR, PTGS2, et HSP90AA1. Ces gènes participent directement ou indirectement à des processus tels que l'inflammation cellulaire, l'apoptose et le stress oxydatif. Le TNF-α est une cible clé pour le traitement de la colite ulcéreuse. Des études ont montré que les niveaux de TNF-α sont élevés dans les échantillons fécaux et les biopsies de la muqueuse du côlon des patients atteints de colite ulcéreuse. Les anticorps monoclonaux anti-TNF-α peuvent avoir des effets anti-inflammatoires en bloquant leur activité biologique. Les anticorps monoclonaux anti-TNF-α ont de bons effets thérapeutiques dans le traitement de la colite ulcéreuse. Les caspases sont impliquées dans l'apoptose cellulaire, et la caspase 3 (CASP3) joue un rôle important dans le processus d'apoptose cellulaire. L'apparition de la colite ulcéreuse est étroitement liée à l'apoptose cellulaire. Des études animales ont montré que la teneur en CASP3 dans la muqueuse intestinale du groupe modèle de la colite ulcéreuse est significativement augmentée, et après un traitement médicamenteux efficace, son niveau d'expression est régulé à la baisse, et le taux d'apoptose des cellules du côlon est significativement réduit. La protéine prostacycline endoperoxyde synthase (PTGS2) est impliquée dans de multiples voies de signalisation inflammatoires, et l'inhibition de cette protéine peut réduire la production de médiateurs inflammatoires. La voie de signalisation de l'EGFR, qui est une voie de signalisation clé dans le corps humain, intervient dans l'apoptose et la prolifération des cellules et est associée à l'apparition de lésions de la muqueuse colique. Par conséquent, l'intervention sur la voie de signalisation de l'EGFR offre la possibilité de traiter la RCH. Des études montrent que les lésions de la muqueuse intestinale de la colite ulcéreuse peuvent affecter l'expression de l'EGFR, réduisant ainsi ses effets protecteurs et réparateurs sur la muqueuse colique, et il a été constaté que les niveaux d'EGFR sont étroitement liés à la récurrence de la RCH. La HSP90AA1 est étroitement liée à l'inflammation et peut réguler la prolifération cellulaire et l'apoptose. L'inhibition de HSP90AA1 peut induire l'autophagie et améliorer la colite ulcéreuse.
On suppose que Weng Bu peut exercer des effets thérapeutiques sur la RCH en régulant les cinq protéines cibles mentionnées ci-dessus pour l'anti-inflammation, l'antioxydation et la réduction de l'apoptose cellulaire. Les résultats de l'amarrage moléculaire ont également montré que Weng Bu a une bonne activité de liaison avec les cinq gènes principaux mentionnés ci-dessus.
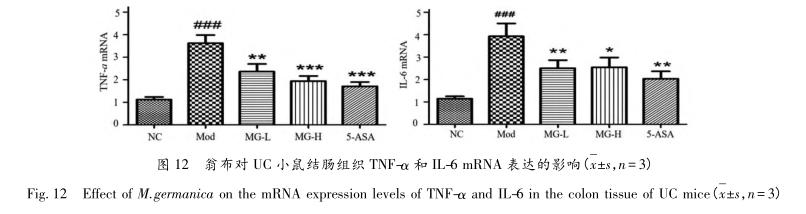
Les résultats de l'étude KEGG ont montré que les principales voies du traitement de la colite ulcéreuse par Onbu comprennent les voies principales de la recherche immunitaire cellulaire, telles que la voie de signalisation des récepteurs des cellules T, la voie de signalisation MAPK et la voie de signalisation du TNF-α. L'IL-6, le facteur de nécrose tumorale alpha et l'interleukine-1 bêta sont trois facteurs inflammatoires courants dans la réponse inflammatoire. Le TNF-α et l'IL-1 β sont des facteurs pro-inflammatoires importants au stade précoce de la RCH aiguë. L'effet inhibiteur des facteurs pro-inflammatoires sur l'apoptose des cellules T joue un rôle pro-inflammatoire soutenu, participant ainsi à l'apparition et au développement de la RCH. Certaines études montrent que les lésions pathologiques des tissus pulmonaires et intestinaux peuvent être améliorées par la voie de signalisation TNF-α/NF-κ B, ce qui permet de traiter à la fois les poumons et les intestins. La voie de signalisation de la protéine kinase activée par les mitogènes comprend les voies de signalisation ERK et p38 MAPK, qui peuvent participer à la régulation de divers processus physiologiques et pathologiques tels que l'inflammation, le stress oxydatif, la différenciation cellulaire et l'apoptose. La transduction de la signalisation MAPK est étroitement liée à la réponse inflammatoire de la RCH.
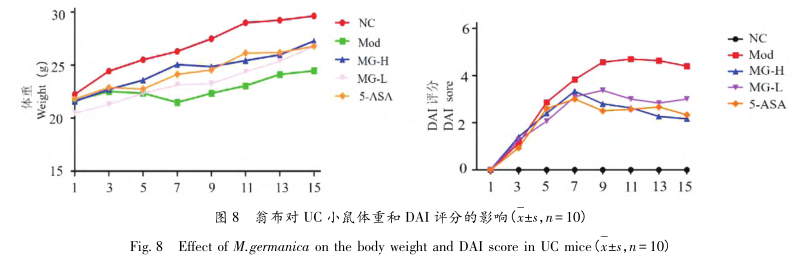
Le TNF-α est la première cytokine libérée par des stimuli nocifs dans le corps, et l'IL-1 β peut être induite par le TNF-α. L'augmentation de l'IL-1 β peut stimuler de manière synergique la production d'IL-6 avec le TNF-α. Par conséquent, cette étude a utilisé la pharmacologie de réseau et les techniques d'amarrage moléculaire pour prédire les cibles thérapeutiques potentielles et les voies de signalisation de l'Onbu sur la colite ulcéreuse. Un modèle murin de colite ulcéreuse a été reproduit par la consommation libre de DSS pour l'évaluation pharmacologique. Onbu peut améliorer la longueur du côlon et les lésions de la muqueuse du côlon induites par le DSS chez les souris atteintes de colite ulcéreuse, réduire les niveaux de TNF-α et d'IL-6 dans le côlon et le sérum, et atténuer la réponse inflammatoire du côlon ulcéreux.
En résumé, cette étude a analysé systématiquement le mécanisme d'action de l'Onbu dans le traitement de la RCH par des méthodes de pharmacologie de réseau et a validé de manière préliminaire sa cible à l'aide de la technologie d'ancrage moléculaire. Parallèlement, l'efficacité d'Onbu dans le traitement de la RCH a été testée par des expériences in vivo sur des souris C57BL-6. Les résultats préliminaires de la recherche indiquent que l'Onbu peut traiter la RCH par une thérapie "multi-cibles, multi-voies" et atténuer la réponse inflammatoire induite par le DSS, mais son mécanisme n'est pas encore clair. Des recherches ultérieures seront menées afin de fournir une référence pour le mécanisme d'action de l'Onbu dans le traitement de la colite ulcéreuse.
