Exploration du mécanisme de la dihydromyricétine dans l'amélioration de la fibrose rénale chez les souris db/db sur la base de la pharmacologie des réseaux et de la vérification expérimentale
La néphropathie diabétique est l'une des principales complications microvasculaires du diabète sucré de type 2 (DT2) et la principale cause d'insuffisance rénale terminale. Ses principales caractéristiques sont l'épaississement de la membrane basale glomérulaire, l'expansion du mésentère et de la matrice tubulo-interstitielle, et la perte de podocytes, entraînant l'apparition d'une microalbuminurie et une diminution de la fonction rénale. Avec le développement continu de la maladie rénale diabétique (MRD), la microstructure du tissu rénal subit une inflammation et des dommages persistants, conduisant à une fibrose interstitielle diffuse qui détruit la microstructure rénale normale et se développe finalement en fibrose rénale (FR). Actuellement, les moyens d'atténuer la progression de la maladie coronarienne vers la fibrose rénale se concentrent principalement sur l'amélioration de la maladie coronarienne. Cependant, le mécanisme de la plupart des complications du diabète, y compris la maladie coronarienne, n'a pas encore été élucidé, de sorte que le mécanisme complexe du processus d'évolution de la maladie coronarienne vers la fibrose rénale n'est pas clair, ce qui conduit à des effets thérapeutiques insatisfaisants de la maladie coronarienne et de la fibrose rénale. Il est donc urgent d'explorer la pathogenèse de la maladie de DKD et de découvrir de nouvelles cibles thérapeutiques pour inhiber son développement.
La dihydromyricétine (DHM) est un composé flavonoïde naturel ayant divers effets pharmacologiques, notamment anti-inflammatoires, antioxydants, piégeage des radicaux libres, amélioration du dysfonctionnement mitochondrial et régulation de l'autophagie. À l'heure actuelle, de nombreuses études ont montré que le DHM a un grand potentiel dans le traitement des maladies métaboliques. Il peut non seulement améliorer la résistance à l'insuline et réduire la glycémie en induisant l'autophagie, en améliorant le stress oxydatif, en inhibant l'inflammation et en augmentant l'activité mitochondriale, mais aussi améliorer de nombreuses complications du diabète, telles que l'encéphalopathie diabétique, la cardiomyopathie diabétique, etc. Cependant, la recherche sur l'amélioration des complications du diabète par le DHM n'est pas suffisante, et le mécanisme pharmacologique associé doit encore être approfondi. En outre, peu de recherches ont été menées pour déterminer si la DHM peut améliorer davantage la FR causée par la DHM, et l'effet thérapeutique n'est toujours pas clair.
La pharmacologie de réseau peut construire un réseau d'interaction "médicament composant cible maladie" basé sur la structure des composants de la médecine traditionnelle chinoise, leurs effets biologiques et les cibles liées à la maladie dans le contexte d'un vaste réseau de processus biologiques. Il s'agit d'un moyen efficace d'explorer les composants efficaces, les mécanismes moléculaires et les cibles potentielles de la médecine traditionnelle chinoise. Le docking moléculaire peut simuler l'interaction entre les molécules et les protéines, prédire la conformation des ligands et des récepteurs, calculer et prédire l'affinité et les modes de liaison afin de vérifier le mode d'action spécifique des composants des médicaments sur les principales cibles. Par conséquent, cette étude a utilisé la pharmacologie des réseaux pour cribler et prédire les cibles potentielles de la DHM sur la DKD et la RF, a construit un réseau d'interaction "composant cible maladie" et a validé les cibles principales prédites par docking moléculaire et par des expériences in vivo. Le mécanisme moléculaire de la dihydromyricétine améliorant la fibrose rénale chez les souris db/db a été exploré, fournissant une base théorique pour l'application clinique du DHM.



À l'heure actuelle, le traitement courant du diabète repose principalement sur le contrôle de la glycémie, alors que la maladie de von Willebrand, l'une des complications les plus graves du diabète, ne fait l'objet d'aucune stratégie de traitement efficace. Il est donc très important de comprendre en profondeur la pathogenèse de la maladie de von Willebrand et de trouver des stratégies de traitement efficaces pour empêcher la maladie de von Willebrand de se transformer en fibrose rénale. Il a été prouvé que les médicaments naturels présentent des avantages uniques, à savoir moins d'effets secondaires et une efficacité multicible, ce qui en fait une source importante pour le développement de nouveaux médicaments contre les maladies chroniques au cours des dernières années. Des recherches plus approfondies sur le DHM ont révélé un potentiel thérapeutique significatif dans l'amélioration des maladies métaboliques. Par conséquent, sur la base de l'amélioration de la fibrose rénale chez les souris db/db par le DHM, cette étude combine la pharmacologie de réseau et la technologie d'ancrage moléculaire pour explorer les cibles thérapeutiques potentielles et les mécanismes moléculaires du DHM dans l'amélioration de la fibrose rénale chez les souris db/db, et les vérifie par des expériences sur les animaux.
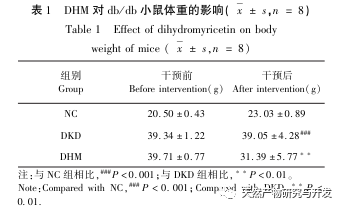
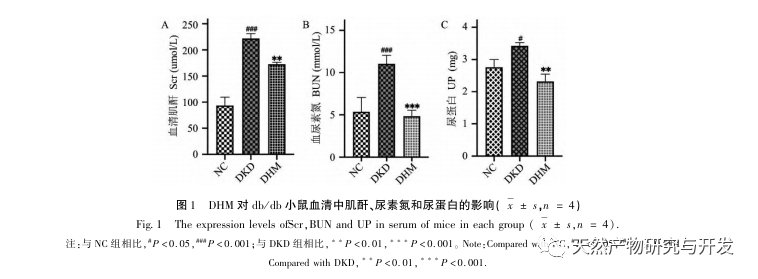
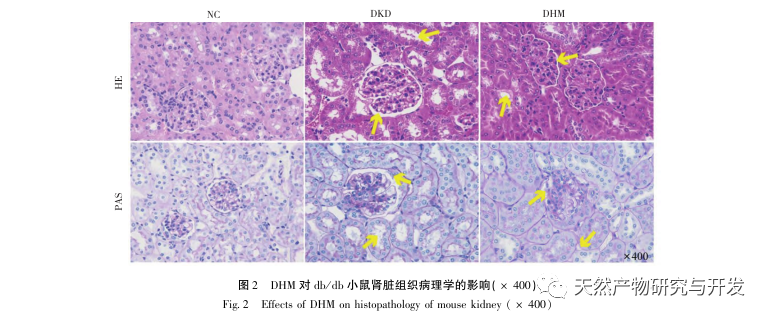
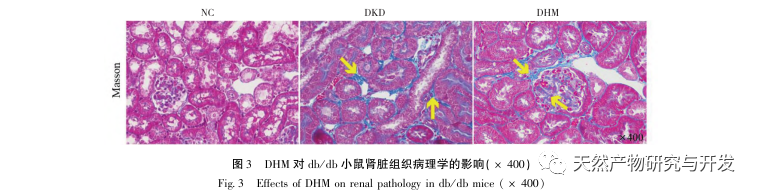
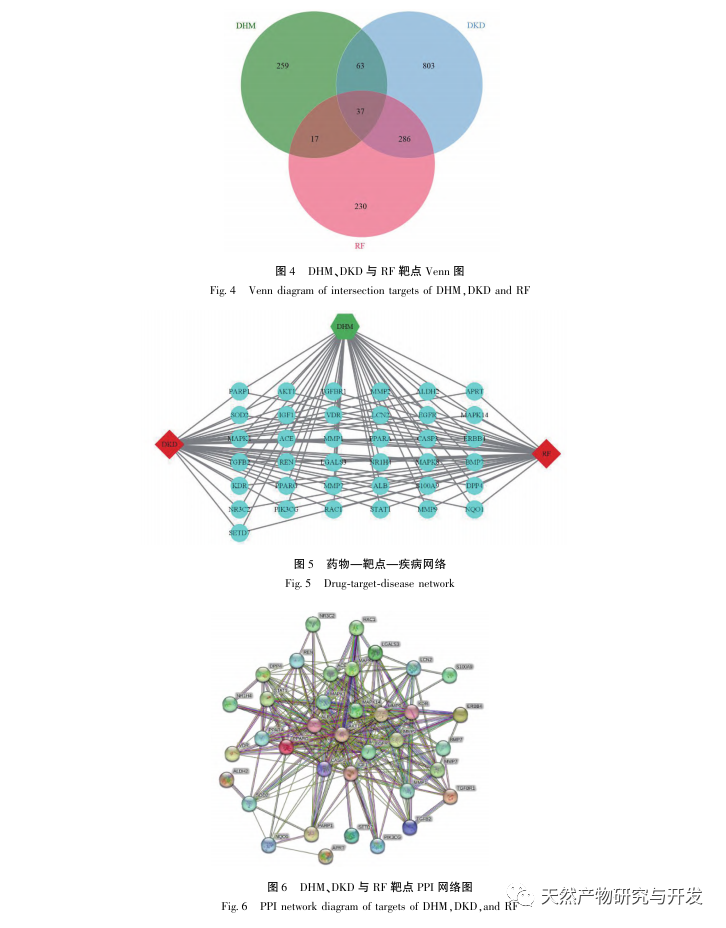
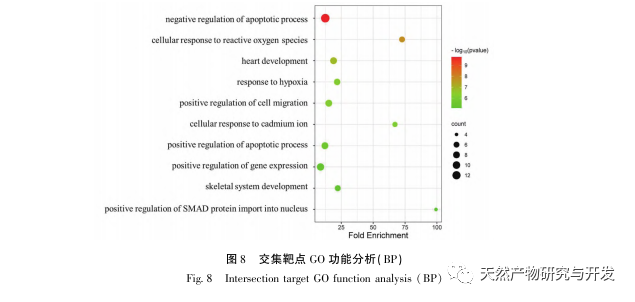
Tout d'abord, nous avons observé que 10 semaines d'intervention de la DHM peuvent réduire efficacement la glycémie, le poids corporel, la créatinine, l'azote uréique, les protéines urinaires et les manifestations pathologiques rénales chez les souris db/db, ce qui indique que la DHM peut atténuer les dommages de la fonction rénale et ralentir le développement de la maladie de DKD chez les souris db/db. Après avoir analysé et criblé 37 cibles croisées de la DHM, de la DKD et du RF, il a été constaté que 10 cibles, dont AKT1, ALB, CASP3, EGFR, MMP9, IGF1, PPARG, KDR, MMP2, ACE, pourraient être des cibles clés pour la DHM afin d'améliorer la DKD. Il a été confirmé que AKT1, CASP3, EGFR, MMP9, IGF1, MMP2, ACE sont activés dans l'environnement du diabète, et l'inhibition spécifique peut améliorer l'état endommagé de la maladie de DKD et ralentir la tendance au développement de la fibrose. PPARG et KDR sont inhibés dans l'environnement physiologique du diabète et jouent un rôle dans la protection rénale après l'activation. L'ALB est un indicateur biochimique important pour observer le degré d'endommagement des reins au cours du développement du diabète. Il augmente généralement avec l'apparition de la maladie de von Willebrand et diminue après l'amélioration de la maladie de von Willebrand. Cela signifie que les 10 gènes clés que nous avons sélectionnés peuvent non seulement servir de biomarqueurs potentiels de la maladie de DKD, mais aussi de cibles clés pour explorer davantage la pathogenèse et le traitement de la maladie de DKD.
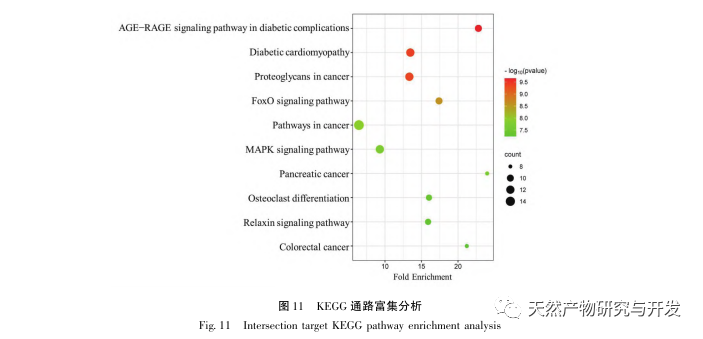
L'analyse de l'enrichissement des voies KEGG a montré que l'amélioration de la DHM sur la DKD pourrait impliquer la voie de signalisation AGE-RAGE, la cardiomyopathie diabétique et la voie de signalisation FoxO. La voie de signalisation AGE-RAGE et la voie de signalisation FoxO jouent un rôle régulateur essentiel dans le développement de la DKD. Les recherches ont montré que les AGE sont spécifiquement activés dans les cellules endothéliales, les tubules rénaux, les cellules mésangiales et les podocytes des patients atteints de la maladie de DKD, et que leur interaction avec RAGE est renforcée, ce qui exacerbe encore le stress oxydatif et l'inflammation dans les reins, entraînant la détérioration de la maladie de DKD. En outre, l'activation de FoxO3a peut inhiber le niveau de stress oxydatif dans les reins des rats diabétiques, améliorer l'inflammation, puis inhiber l'apparition de la maladie de DKD. La régulation spécifique de la voie de signalisation AGE-RAGE ou de la voie de signalisation FoxO pourrait être d'une grande importance pour la prévention et le traitement de la maladie coronarienne.
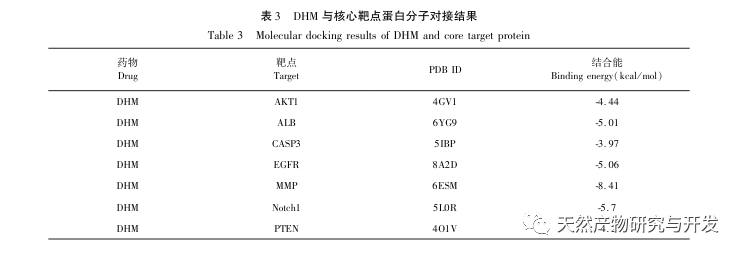
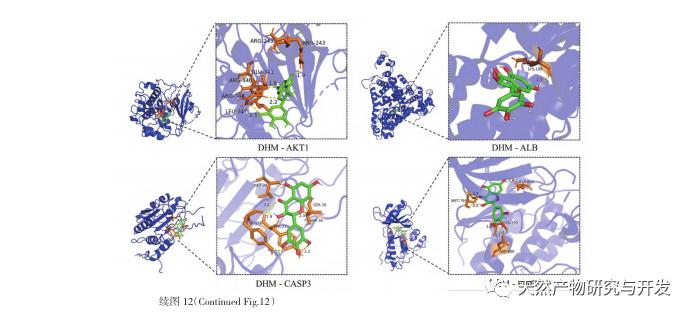
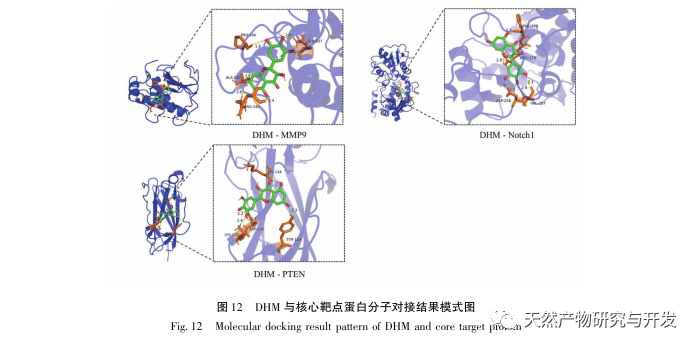
Les résultats de l'amarrage moléculaire ont montré que le DHM présentait une bonne affinité de liaison avec les cinq premières cibles sélectionnées, ce qui indique que l'efficacité du DHM dans le traitement de la maladie de DKD a été validée au niveau moléculaire. En outre, nous avons remarqué que le gène cible clé AKT1, classé premier dans la sélection, était étroitement lié à la voie de signalisation AGE-RAGE et à la voie de signalisation FoxO dans le développement de la maladie de Parkinson, grâce à l'analyse d'enrichissement de la voie KEGG. La voie de signalisation AGE-RAGE peut entrer en synergie avec la voie de signalisation PI3K/Akt pour induire un stress oxydatif et une inflammation chronique dans les reins, conduisant à une maladie rénale. L'activation de la voie PI3K/Akt/FoxO3a peut améliorer la fonction physiologique des reins dans le diabète. Nous avons donc tenté d'étudier l'interaction entre la voie Notch en amont d'AKT1 et le DHM et avons procédé à la validation de l'amarrage moléculaire. Les résultats de l'amarrage moléculaire ont montré que le DHM présentait une bonne affinité de liaison avec Notch1 et PTEN.
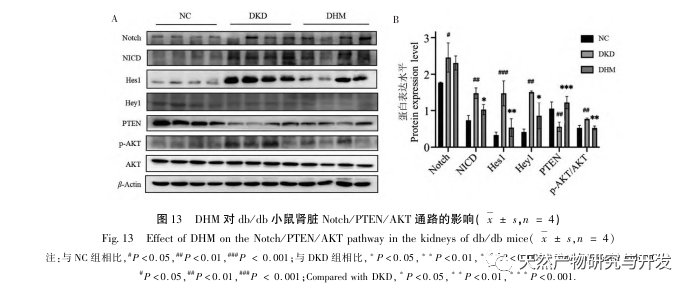
Des études antérieures ont montré que la voie Notch est suractivée au cours du développement de la maladie de DKD, ce qui se manifeste par une expression accrue de Notch1, NICD, Hes1 et Hey1. Les inhibiteurs de Notch1 peuvent activer la PTEN en réduisant l'activation de Hes1, améliorant ainsi les troubles de l'autophagie et ralentissant l'apparition du FR. En outre, d'autres études ont montré que l'activation de la PTEN peut également atténuer la progression de la maladie de DKD en inhibant la voie PI3K/Akt. Sur la base des résultats ci-dessus, nous supposons que la DHM peut améliorer la DKD en régulant la voie Notch/PTEN/AKT. Les résultats du Western blot ont montré une augmentation anormale de l'activation de la voie Notch, une diminution de l'expression de PTEN et une augmentation de la phosphorylation d'AKT dans les reins des souris db/db. La prise de DHM peut inhiber l'activation de la voie Notch, activer la PTEN et inhiber la phosphorylation de l'AKT. Bien que l'axe du signal Notch/PTEN/AKT en tant que voie globale ait rarement été étudié dans le cadre de la protection rénale dans le diabète, notre recherche a permis d'améliorer la recherche pertinente dans une certaine mesure et d'enrichir le mécanisme moléculaire de la protection biologique du DHM par le biais de cibles multiples.
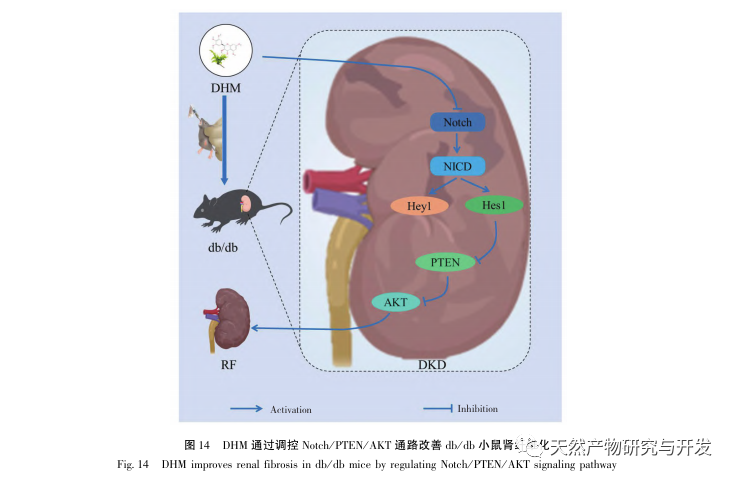
En résumé, sur la base de l'observation de l'amélioration des manifestations pathologiques de la maladie de DKD par le DHM, cette étude a combiné la pharmacologie de réseau et la technologie d'ancrage moléculaire pour démontrer de manière préliminaire que le rôle du DHM dans l'amélioration de la progression de la maladie de DKD peut être atteint par des cibles clés telles que AKT1, ALB, CASP3, EGFR, MMP9, IGF1, PPARG, KDR, MMP2, ACE, et a analysé les voies correspondantes ; Enfin, une validation et une analyse préliminaires ont été effectuées sur les cibles AKT potentielles du DHM par le biais d'expériences animales, et il a été constaté que le DHM pourrait jouer un rôle dans la prévention et le traitement de la maladie de DKD en régulant la voie Notch/PTEN/AKT (voir la figure 14). Toutefois, les recherches sur les complications de la DHM dans le DT2 sont actuellement relativement peu nombreuses et son potentiel thérapeutique doit encore faire l'objet d'études plus approfondies.
