Astragalosid IV'ün yüksek doz S-ketamin kaynaklı PC12 hücre hasarı üzerindeki koruyucu etkisi
Dünya çapında her yıl milyonlarca bebek ve küçük çocuk genel anestezi almaktadır. Çok sayıda çalışma, tek ve kısa süreli anestezinin sinir sisteminin gelişimi üzerinde olumsuz etkileri olmadığını, ancak anestezik ilaçlara yüksek dozlarda veya tekrar tekrar maruz kalmanın bilişsel işlev bozukluğuna ve nörolojik gelişim bozukluklarına neden olabileceğini göstermiştir. Anestezik ilaçların gelişmekte olan beyin üzerindeki etkisi birçok ebeveynin dikkatini çekmiştir.
S-ketamin (SK) ketaminin S enantiyomeridir ve 2019 yılında şiddetli depresyon tedavisinde yardımcı ilaç olarak FDA tarafından resmen onaylanmıştır. Ayrıca pediatrik ve obstetrik ameliyatlarda yaygın olarak kullanılan bir anesteziktir. İnsanların, neden olabileceği potansiyel risklere çok fazla dikkat etmeden, sadece antidepresan etkilerini incelemekle ilgileniyor gibi görünmesi endişe vericidir. Yakın zamanda yapılan bir çalışmada SK ile ilgili 962 advers olay analiz edilmiş ve kadın hastaların, yüksek doz SK alan hastaların ve birden fazla ilaç tedavisi alan hastaların advers reaksiyon yaşama olasılığının daha yüksek olduğu bulunmuştur. Bu nedenle, SK kaynaklı sinir hasarının mekanizmasını araştırmak ve hem bebek hem de yetişkin anestezisi için ilgili başa çıkma önlemlerini bulmak büyük önem taşımaktadır.
Astragaloside IV (ASIV), geleneksel Çin ilacı Astragalus membranaceus'tan izole edilen ana aktif bileşenlerden biridir. Çalışmalar, anti-tümör, anti-enflamatuar, antioksidan, anti fibrotik ve anti apoptotik etkiler de dahil olmak üzere çok çeşitli farmakolojik etkilere sahip olduğunu göstermiştir. Ayrıca, doğal bir nöroprotektif ajan olduğu kanıtlanmıştır. Bununla birlikte, ASIV'in anestezik ilaçların neden olduğu sinir hasarını hafifletip hafifletemeyeceği konusunda çok az rapor vardır. Bu nedenle, bu çalışmada SK'nin in vitro hasar modelini oluşturmak, ASIV'nin nöroprotektif etkisini araştırmak ve SK'nin rasyonel kullanımı ve ASIV için yeni ilaçların geliştirilmesi için referans sağlamak üzere yaygın olarak kullanılan nöral hücre hattı sıçan adrenal feokromositoma hücreleri, yani PC12 hücreleri seçilmiştir.




Anestezik ilaçların nörotoksisitesi her zaman uluslararası toplumun bir endişesi olmuştur. ABD Gıda ve İlaç İdaresi ve Uluslararası Anesteziyoloji Çalışmaları Derneği, klinik öncesi araştırmaların standartlaştırılmasının ve anesteziye bağlı perinatal nörotoksisite için raporlama standartlarının oluşturulmasının önemini tartışmak üzere ortak bir toplantı düzenlemiş ve bu alandaki bazı önemli sorunları ele almak için yeni yöntemlerin kullanılmasını önermiştir. Ketamine gelince, çoğu anesteziğin aksine, bir NMDA reseptör antagonistidir. NMDA reseptörlerinin ilaçla bloke edilmesi, beyin gelişimi için gerekli olan uyarıcı inhibitör dengeyi değiştirerek nörotoksisiteye yol açabilir. Çalışmalar, ketaminin insanlarda mitokondriyal apoptoz yolu üzerinden zamana ve doza bağlı bir şekilde nörotoksisiteyi indükleyebildiğini gösterirken, enantiyomeri S-ketaminin benzer yan etkiler ürettiği bildirilmemiştir. Bu nedenle, belirli bir konsantrasyon eşiğine ulaşıldığında, SK'nin de mitokondriyal apoptoz yolunu aktive edebileceği ve hücre apoptozuna neden olabileceği tahmin edilmektedir.
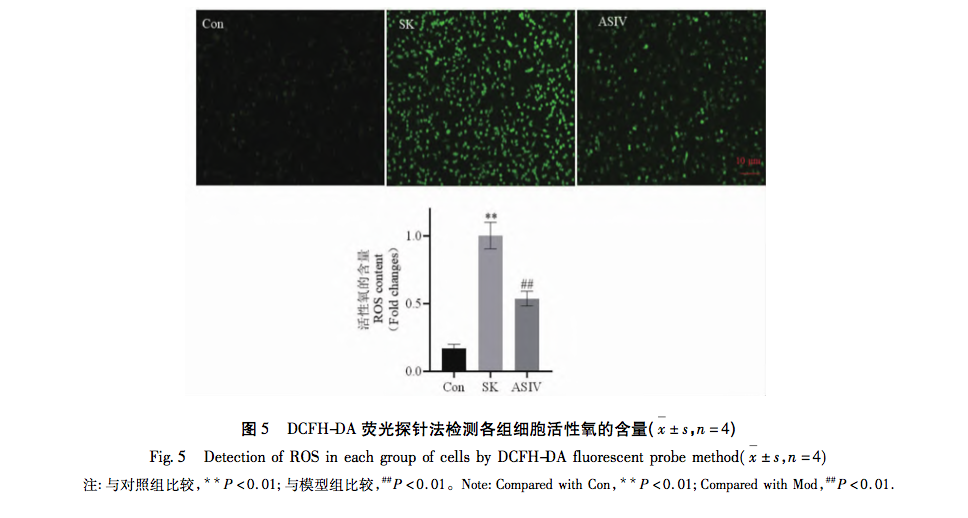
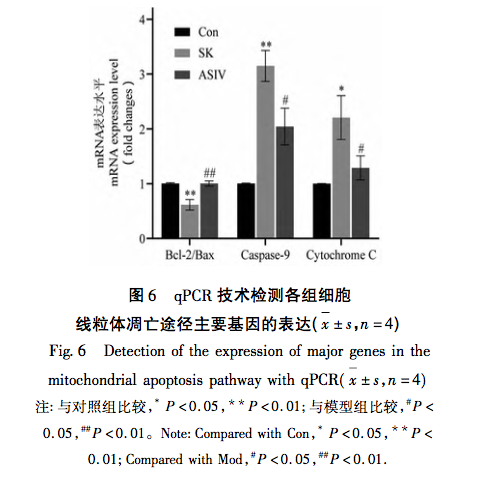
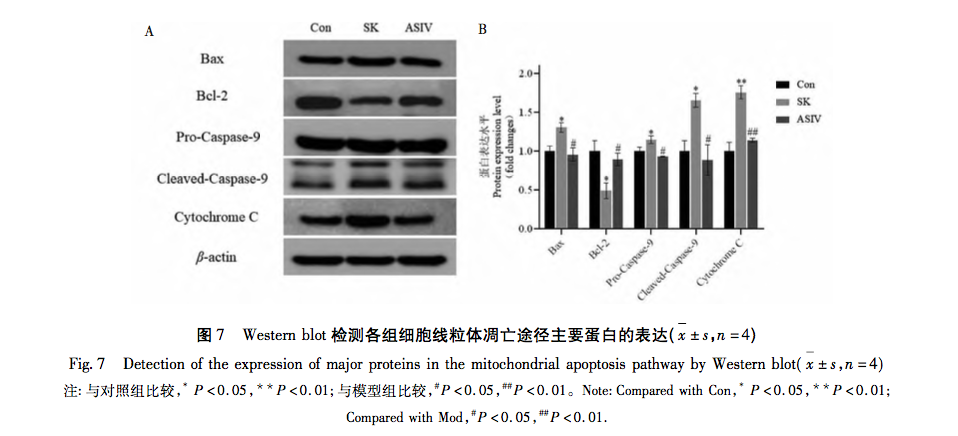
Hücresel metabolizmanın merkezi ve redoks dengesinin ana düzenleyicisi olan mitokondri, hastalıkların ortaya çıkmasında ve gelişmesinde çok önemli bir rol oynamaktadır. Mitokondrinin aracılık ettiği birçok fizyolojik reaksiyon arasında oksidatif stres, mitokondriyal apoptoz yolunun aktive edilmesinde kilit faktörlerden biridir ve aşırı ROS, oksidatif stresin ortaya çıkmasının maddi temelidir. Klinik uygulamada yaygın olarak kullanılan anesteziklerin oksidatif stres derecesini arttırdığı veya azalttığı kanıtlanmıştır. Örneğin, inhalasyon anestezisi sevofluran, hücre içi Ca2+ konsantrasyonunu artırarak, ROS seviyelerini yükselterek ve mitokondriyal apoptoz yolu ile ilgili proteinler Cleaved-Caspase-9, Cytochrome C ve Bax/Bcl-2 ekspresyonunu artırarak nöronal apoptozu indükleyebilir. Lokal anestezik bupivakain, ROS aracılı otofajiyi aktive ederek otofaji akışının bozulmasına ve hücre canlılığının azalmasına neden olur. Bununla birlikte, reaktif oksijen türleri temizleyicilerinin kullanımı bu otofajik hasarı önemli ölçüde tersine çevirebilir. Mitokondriyal yolda, ROS içeriğindeki artış Bax ve Bcl-2'nin göreceli ifade seviyelerinde değişikliklere yol açar. Bax aktive olur ve mitokondrinin dış membranında oligomerize olur ve daha sonra mitokondriyal membran geçirgenliğini değiştirmek için spesifik moleküllere bağlanır. Sitokrom C bu nedenle mitokondriden sitoplazmaya salınır, Apaf-1 gibi faktörlerle bağlanarak apoptotik cisimler oluşturur ve Pro-Caspase-9'u bölünmek üzere aktive eder. Bölünmüş Kaspaz-9 ayrıca aşağı akışla ilgili apoptotik faktörleri aktive ederek hücre apoptozunu teşvik eder.
Astragaloside IV güçlü antioksidan özelliklere sahip doğal bir aktif maddedir ve araştırmalar bazı etkilerinin mitokondri ile yakından ilişkili olduğunu göstermiştir. Örneğin, ASIV mitokondriyal otofajiyi teşvik edebilir, hasarlı mitokondri birikimini ve mitokondriyal reaktif oksijen türlerinin oluşumunu azaltabilir. Liu ve arkadaşları ayrıca ASIV'lerin mitokondrinin iç zarında bulunan ve insan beyninde yüksek oranda ifade edilen bir protein olan alfa sinükleini hedef alarak nöroprotektif etkiler gösterebileceğini bulmuştur. ASIV'nin anestezik ilaçların neden olduğu sinir hasarını tedavi etme potansiyeline sahip olduğu görülebilir.
Yukarıdaki araştırma sonuçlarına ve analizlere dayanarak, bu çalışma, ASIV ile yüksek doz SK kaynaklı sinir hasarını tedavi etmek için bir ipucu olarak mitokondriyal apoptoz yolunu kullanan bir in vitro deney gerçekleştirmiştir. SK ve ASIV'in nihai deneysel konsantrasyonları CCK-8 testi kullanılarak sırasıyla 450 μg/mL ve 25 μmol/L olarak belirlenmiştir. Ek olarak, deney, yüksek dozda SK'ye maruz kalan PC12 hücrelerinin sadece apoptoz oranında ve ROS içeriğinde önemli bir artış göstermekle kalmayıp, aynı zamanda mitokondriyal apoptoz yolundaki ana yukarı akış molekülleri Bax, Bcl-2, Caspase-9 ve Cytochrome C'yi de aktive ettiğini buldu. Bu, yüksek doz SK'nin ROS aracılı mitokondriyal apoptoz yolunu aktive ederek PC12 hücrelerinde apoptozu indüklediğini göstermektedir. ASIV ile tedaviden sonra, SK tarafından indüklenen bu değişiklikler önemli ölçüde engellenmiştir, bu da ASIV'in bu süreç sırasında PC12 hücreleri üzerinde belirli bir koruyucu etkiye sahip olduğunu göstermektedir.
Özet olarak, Astragaloside IV, PC12 hücrelerinde yüksek doz S-ketamin kaynaklı hasarı hafifletebilir ve mekanizması mitokondriyal apoptoz yolunun inhibisyonu ile ilişkili olabilir.
