Az asztragalozid IV védő hatása a nagy dózisú S-ketamin által kiváltott PC12 sejtkárosodásra
Világszerte évente több millió csecsemőt és kisgyermeket altatnak általános érzéstelenítésben. Számos tanulmány kimutatta, hogy az egyszeri és rövid ideig tartó altatásnak nincs káros hatása az idegrendszer fejlődésére, de a nagy dózisú vagy ismételt altatószer-expozíció kognitív zavarokat és neurológiai fejlődési rendellenességeket okozhat. Az altatószerek hatása a fejlődő agyra számos szülő széles körű figyelmét felkeltette.
Az S-ketamin (SK) a ketamin S enantiomerje, és az FDA 2019-ben hivatalosan engedélyezte a súlyos depresszió kezelésére szolgáló adjuváns gyógyszerként. Gyermek- és szülészeti műtéteknél is gyakran alkalmazott érzéstelenítő. Aggasztó, hogy úgy tűnik, az embereket csak az antidepresszáns hatásainak tanulmányozása érdekli, anélkül, hogy túl nagy figyelmet fordítanának a lehetséges kockázatokra, amelyeket okozhat. Egy nemrégiben készült tanulmány 962 SK-val kapcsolatos mellékhatást elemzett, és megállapította, hogy a női betegeknél, a nagy dózisú SK-t kapó betegeknél és a többszörös gyógyszeres kezelésben részesülő betegeknél nagyobb volt a mellékhatások előfordulásának valószínűsége. Ezért nagy jelentőséggel bír az SK által kiváltott idegkárosodás mechanizmusának feltárása és a megfelelő megküzdési intézkedések megtalálása mind a csecsemő-, mind a felnőtt anesztézia esetében.
Az Astragaloside IV (ASIV) az Astragalus membranaceus hagyományos kínai gyógyszerből izolált egyik fő hatóanyaga. Vizsgálatok kimutatták, hogy farmakológiai hatásainak széles skálája van, beleértve a daganatellenes, gyulladáscsökkentő, antioxidáns, antifibrotikus és antiapoptotikus hatásokat. Ezenkívül természetes neuroprotektív hatásúnak bizonyult. Kevés jelentés szól azonban arról, hogy az ASIV képes-e enyhíteni az altatószerek által okozott idegkárosodást. Ezért ez a tanulmány a gyakran használt idegsejtvonalat patkány mellékvesekéreg-fehérje-fehromocitóma sejteket, nevezetesen a PC12 sejteket választotta ki az SK in vitro sérülési modelljének létrehozásához, az ASIV neuroprotektív hatásának feltárásához, és referenciát nyújt az SK racionális felhasználásához és az ASIV új gyógyszerek kifejlesztéséhez.




Az altatószerek neurotoxicitása mindig is aggodalommal töltötte el a nemzetközi közösséget. Az Egyesült Államok Élelmiszer- és Gyógyszerügyi Hivatala és a Nemzetközi Aneszteziológiai Tanulmányozó Szövetség közös ülést tartott, hogy megvitassák a preklinikai kutatások szabványosításának és az altatás okozta perinatális neurotoxicitás jelentési szabványainak kialakításának fontosságát, és új módszerek alkalmazását javasolták az e területen felmerülő néhány fontos kérdés megoldására. Ami a ketamint illeti, a legtöbb altatószertől eltérően ez egy NMDA-receptor-antagonista. Az NMDA-receptorok gyógyszeres blokkolása megváltoztathatja az agy fejlődéséhez szükséges excitatorikus-gátló egyensúlyt, ami neurotoxicitáshoz vezethet. Vizsgálatok kimutatták, hogy a ketamin emberekben a mitokondriális apoptózis útvonalán keresztül idő- és dózisfüggő módon neurotoxicitást idézhet elő, míg az S-ketamin enantiomerje nem okoz hasonló mellékhatásokat. Ezért feltételezhető, hogy egy bizonyos koncentrációs küszöbérték elérésekor az SK is aktiválhatja a mitokondriális apoptózis útját és sejt apoptózist okozhat.
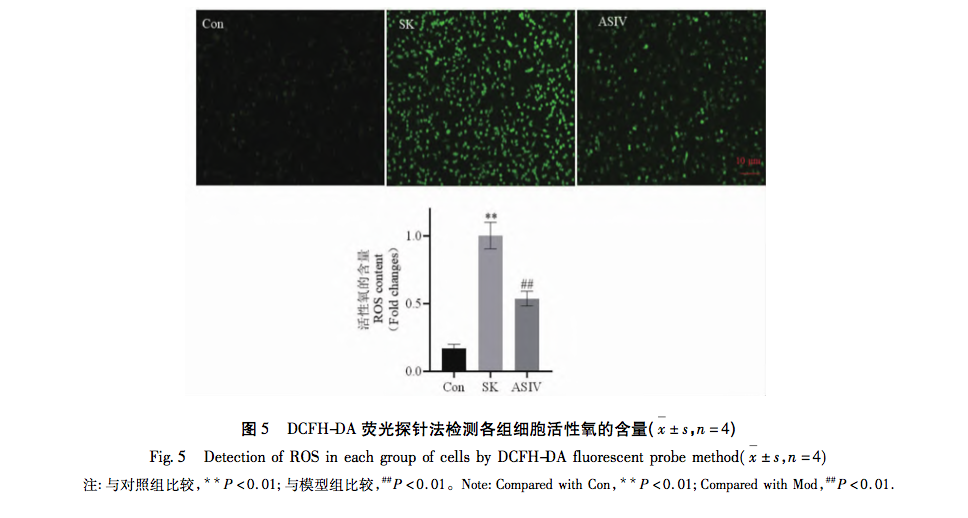
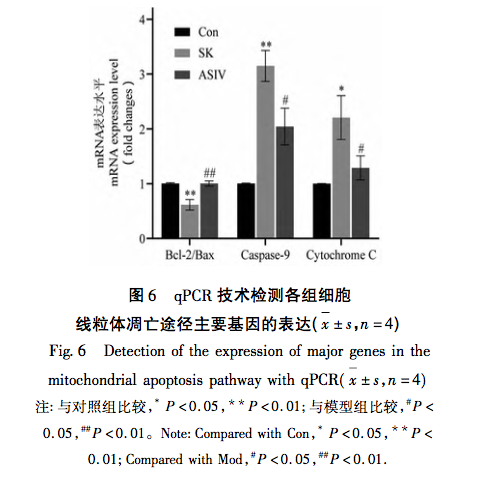
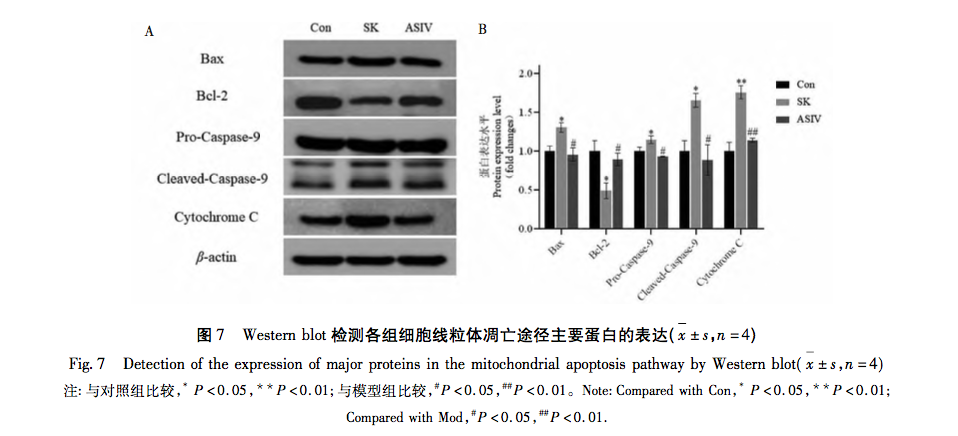
A mitokondriumok, mint a sejtek anyagcseréjének központja és a redox egyensúly fő szabályozója, döntő szerepet játszanak a betegségek kialakulásában és fejlődésében. A mitokondriumok által közvetített számos élettani reakció közül az oxidatív stressz az egyik legfontosabb tényező a mitokondriális apoptózis útvonal aktiválásában, és a túlzott ROS az oxidatív stressz kialakulásának anyagi alapja. A klinikai gyakorlatban általánosan használt anesztetikumok bizonyítottan elősegítik vagy csökkentik az oxidatív stressz mértékét. Például az inhalációs anesztézia, a sevoflurán az intracelluláris Ca2+koncentráció növelése, a ROS-szintek emelkedése és a mitokondriális apoptózis útvonalhoz kapcsolódó fehérjék, a Cleaved-Caspase-9, a Cytochrome C és a Bax/Bcl-2 expressziójának növelése révén idézhet elő neuronális apoptózist. A helyi érzéstelenítő bupivakain aktiválja a ROS által közvetített autofágiát, ami károsodott autofágia-áramláshoz és csökkent sejtéletképességhez vezet. A reaktív oxigénfajok fékezőinek alkalmazása azonban jelentősen visszafordíthatja ezt az autofágikus károsodást. A mitokondriális útvonalon a ROS-tartalom növekedése a Bax és a Bcl-2 relatív expressziós szintjének változásához vezet. A Bax aktiválódik és oligomerizálódik a mitokondriumok külső membránjánál, majd specifikus molekulákhoz kötődve megváltoztatja a mitokondriumok membránpermeabilitását. A citokróm C ezért a mitokondriumokból a citoplazmába szabadul fel, apoptotikus testeket képezve olyan faktorokhoz kötődik, mint az Apaf-1, és a Pro-Caspase-9-et aktiválja a hasításhoz. A hasított kaszpáz-9 tovább aktiválja a downstream kapcsolódó apoptotikus faktorokat, elősegítve a sejt apoptózisát.
Az asztragalozid IV egy erős antioxidáns tulajdonságokkal rendelkező természetes hatóanyag, és a kutatások kimutatták, hogy egyes hatásai szorosan kapcsolódnak a mitokondriumokhoz. Az ASIV például elősegítheti a mitokondriális autofágiát, csökkentheti a sérült mitokondriumok felhalmozódását és a mitokondriális reaktív oxigénfajok keletkezését. Liu és munkatársai azt is megállapították, hogy az ASIV-ek neuroprotektív hatást fejthetnek ki az alfa-szinukleinin, a mitokondriumok belső membránjában található és az emberi agyban nagymértékben kifejeződő fehérje célpontjaként. Látható, hogy az ASIV potenciálisan alkalmas az altatószerek által okozott idegkárosodás kezelésére.
A fenti kutatási eredmények és elemzések alapján ez a tanulmány in vitro kísérletet végzett a mitokondriális apoptózis útvonalának felhasználásával, mint nyomravezetőt a nagy dózisú SK által kiváltott idegkárosodás ASIV-vel történő kezelésére. Az SK és az ASIV végső kísérleti koncentrációját 450 μ g/mL, illetve 25 μ mol/l értékben határoztuk meg CCK-8 vizsgálat segítségével. Ezenkívül a kísérlet azt mutatta, hogy a nagy dózisú SK-nak kitett PC12 sejtek nemcsak az apoptózis sebességének és ROS-tartalmának jelentős növekedését mutatták, hanem aktiválták a Bax, Bcl-2, Caspase-9 és Cytochrome C fő upstream molekulákat is a mitokondriális apoptózis útvonalban. Ez azt jelzi, hogy a nagy dózisú SK apoptózist indukál a PC12 sejtekben a ROS által közvetített mitokondriális apoptózis útvonal aktiválásával. ASIV-kezelés után ezek az SK által indukált változások jelentősen gátoltak, ami azt mutatja, hogy az ASIV-nek bizonyos védő hatása van a PC12 sejtekre ebben a folyamatban.
Összefoglalva, az asztragalozid IV enyhítheti a PC12 sejtek nagy dózisú S-ketamin által kiváltott károsodást, és mechanizmusa a mitokondriális apoptózis útvonalának gátlásához kapcsolódhat.
