Erforschung des Mechanismus von Dihydromyricetin zur Verbesserung der Nierenfibrose bei db/db-Mäusen auf der Grundlage von Netzwerkpharmakologie und experimenteller Überprüfung
Die Diabetesnephropathie (DKD) ist eine der wichtigsten mikrovaskulären Komplikationen des Typ-2-Diabetes mellitus (T2DM) und die Hauptursache für Nierenerkrankungen im Endstadium. Ihre Hauptmerkmale sind die Verdickung der glomerulären Basalmembran, die Ausdehnung des Mesenteriums und der tubulointerstitiellen Matrix sowie der Verlust von Podozyten, was zur Entwicklung einer Mikroalbuminurie und einer verminderten Nierenfunktion führt. Mit der fortschreitenden Entwicklung der diabetischen Nierenerkrankung (DKD) kommt es zu einer anhaltenden Entzündung und Schädigung der Mikrostruktur des Nierengewebes, was zu einer diffusen interstitiellen Fibrose führt, die die normale Mikrostruktur der Niere zerstört und sich schließlich zur Nierenfibrose (RF) entwickelt. Gegenwärtig konzentrieren sich die Maßnahmen zur Abschwächung des Fortschreitens von DKD zu RF hauptsächlich auf die Verbesserung der DKD. Der Mechanismus der meisten Komplikationen des Diabetes, einschließlich der DKD, ist jedoch noch nicht geklärt, so dass der komplexe Mechanismus bei der Entwicklung von DKD zu RF nicht klar ist, was zu unbefriedigenden therapeutischen Effekten von DKD und RF führt. Daher ist es dringend erforderlich, die Pathogenese der DKD zu erforschen und neue therapeutische Angriffspunkte zu finden, um ihre Entwicklung zu hemmen.
Dihydromyricetin (DHM) ist eine natürliche Flavonoidverbindung mit verschiedenen pharmakologischen Wirkungen, darunter entzündungshemmende, antioxidative, freie Radikale einfangende, die mitochondriale Dysfunktion verbessernde und die Autophagie regulierende Eigenschaften. Mehrere Studien haben gezeigt, dass DHM ein großes Potenzial bei der Behandlung von Stoffwechselkrankheiten hat. Es kann nicht nur die Insulinresistenz verbessern und den Blutzuckerspiegel senken, indem es die Autophagie anregt, den oxidativen Stress verbessert, Entzündungen hemmt und die Aktivität der Mitochondrien erhöht, sondern es kann auch viele Komplikationen von Diabetes wie Diabetes-Enzephalopathie, Diabetes-Kardiomyopathie usw. verbessern. Die Forschung zur Verbesserung der Komplikationen von Diabetes durch DHM ist jedoch nicht ausreichend, und der damit verbundene pharmakologische Mechanismus muss noch weiter erforscht werden. Darüber hinaus gibt es nur begrenzte Forschung darüber, ob DHM die durch DHM verursachten RF weiter verbessern kann, und die therapeutische Wirkung ist noch unklar.
Die Netzwerk-Pharmakologie kann ein Interaktionsnetzwerk "Arzneimittel-Komponente-Ziel-Krankheit" konstruieren, das auf der Struktur der Komponenten der traditionellen chinesischen Medizin, ihren biologischen Wirkungen und krankheitsbezogenen Zielen im Kontext eines riesigen Netzwerks biologischer Prozesse basiert. Dies ist ein wirksames Mittel zur Erforschung der wirksamen Bestandteile, molekularen Mechanismen und potenziellen Ziele der traditionellen chinesischen Medizin. Molekulares Docking kann die Interaktion zwischen Molekülen und Proteinen simulieren, die Konformation von Liganden und Rezeptoren vorhersagen, die Affinität und die Bindungsmodi berechnen und vorhersagen, um die spezifische Wirkungsweise von Arzneimittelkomponenten auf wichtige Targets zu überprüfen. Daher wurde in dieser Studie die Netzwerkpharmakologie eingesetzt, um potenzielle Ziele von DHM bei DKD und RF zu screenen und vorherzusagen, ein Interaktionsnetzwerk "Komponente-Ziel-Krankheit" aufzubauen und die vorhergesagten Hauptziele durch molekulares Docking und In-vivo-Experimente zu validieren. Der molekulare Mechanismus der Verbesserung der Nierenfibrose bei db/db-Mäusen durch Dihydromyricetin wurde erforscht, wodurch eine theoretische Grundlage für die klinische Anwendung von DHM geschaffen wurde.



Gegenwärtig hängt die übliche Behandlung von Diabetes hauptsächlich von der Kontrolle des Blutzuckers ab, während es für DKD, eine der schwerwiegendsten Komplikationen von Diabetes, keine wirksame Behandlungsstrategie gibt. Daher ist es sehr wichtig, die Pathogenese der DKD genau zu verstehen und wirksame Behandlungsstrategien zu finden, um die Entwicklung der DKD zu einer Nierenfibrose zu verhindern. Naturheilmittel haben nachweislich die einzigartigen Vorteile, dass sie weniger Nebenwirkungen haben und vielseitig wirksam sind, was sie in den letzten Jahren zu einer wichtigen Quelle für die Entwicklung neuer Medikamente gegen chronische Krankheiten gemacht hat. Weitere Forschungen zu DHM haben ein erhebliches therapeutisches Potenzial zur Verbesserung von Stoffwechselkrankheiten ergeben. Ausgehend von der Verbesserung der Nierenfibrose bei db/db-Mäusen durch DHM werden in dieser Studie die Netzwerkpharmakologie und die molekulare Docking-Technologie kombiniert, um die potenziellen therapeutischen Ziele und molekularen Mechanismen von DHM bei der Verbesserung der Nierenfibrose bei db/db-Mäusen zu erforschen, und sie werden durch Tierversuche verifiziert.
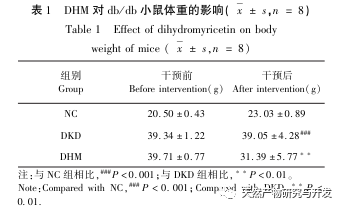
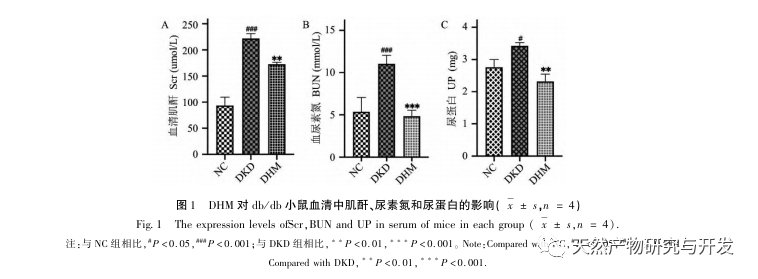
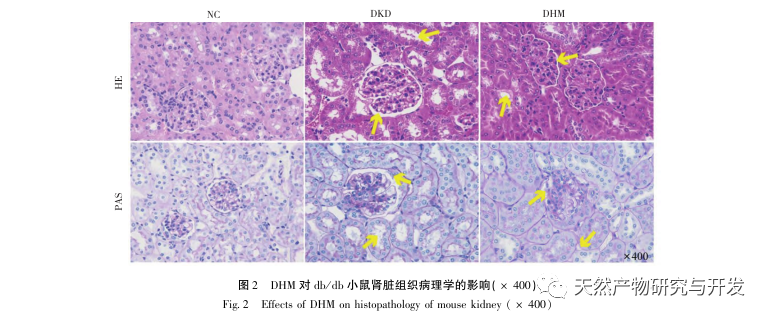
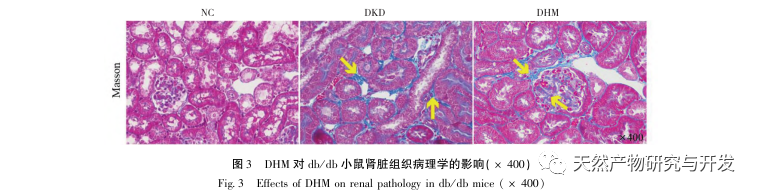
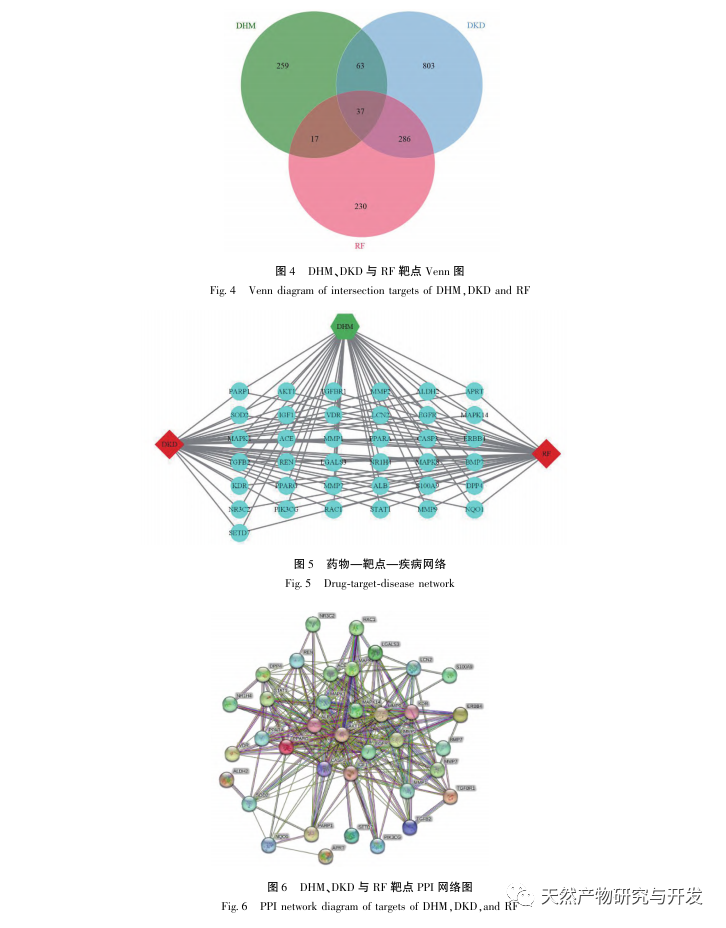
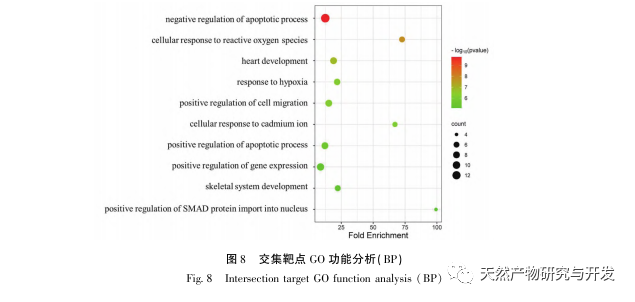
Erstens haben wir festgestellt, dass eine 10-wöchige DHM-Intervention Blutzucker, Körpergewicht, Kreatinin, Harnstoff-Stickstoff, Urinprotein und pathologische Nierenmanifestationen bei db/db-Mäusen wirksam lindern kann, was darauf hindeutet, dass DHM die Schädigung der Nierenfunktion lindern und die Entwicklung von DKD bei db/db-Mäusen verlangsamen kann. Nach der Analyse und dem Screening von 37 sich überschneidenden Zielmolekülen von DHM, DKD und RF wurde festgestellt, dass 10 Zielmoleküle, darunter AKT1, ALB, CASP3, EGFR, MMP9, IGF1, PPARG, KDR, MMP2 und ACE, wichtige Zielmoleküle für DHM zur Verbesserung von DKD sein könnten. Es wurde bestätigt, dass AKT1, CASP3, EGFR, MMP9, IGF1, MMP2 und ACE im Umfeld von Diabetes aktiviert werden, und eine spezifische Hemmung kann den geschädigten Zustand von DKD verbessern und die Entwicklungstendenz der Fibrose verlangsamen. PPARG und KDR werden in der physiologischen Umgebung von Diabetes gehemmt und spielen eine Rolle beim Nierenschutz nach der Aktivierung. ALB ist ein wichtiger biochemischer Indikator, um den Grad der Nierenschädigung während der Entwicklung von Diabetes zu beobachten. Er steigt in der Regel mit dem Auftreten von DKD an und sinkt nach der Verbesserung der DKD. Dies bedeutet, dass die 10 Schlüsselgene, die wir untersucht haben, nicht nur als potenzielle Biomarker für DKD dienen können, sondern auch als Schlüsselziele für die weitere Erforschung der Pathogenese und Behandlung von DKD.
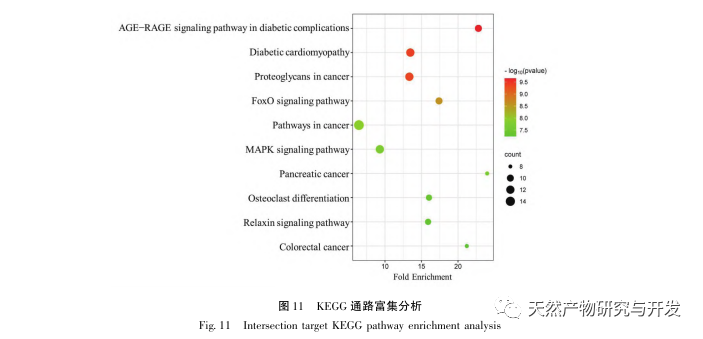
Die Analyse der Anreicherung von KEGG-Signalwegen zeigte, dass die Verbesserung von DHM bei DKD mit dem AGE-RAGE-Signalweg, der Diabetes-Kardiomyopathie und dem FoxO-Signalweg zusammenhängen könnte. Der AGE-RAGE-Signalweg und der FoxO-Signalweg spielen bei der Entwicklung von DKD eine wichtige Rolle. Forschungen haben ergeben, dass AGEs spezifisch in Endothelzellen, Nierentubuli, Mesangialzellen und Podozyten von DKD-Patienten aktiviert werden und ihre Interaktion mit RAGE verstärkt wird, was den oxidativen Stress und die Entzündung in den Nieren weiter verschärft und zur Verschlechterung der DKD führt. Darüber hinaus kann aktiviertes FoxO3a das Ausmaß an oxidativem Stress in der Niere von Diabetes-Ratten hemmen, die Entzündung verbessern und dann das Auftreten von DKD verhindern. Dies deutet darauf hin, dass eine spezifische Regulierung des AGE-RAGE-Signalwegs oder des FoxO-Signalwegs für die Prävention und Behandlung von DKD von großer Bedeutung sein könnte.
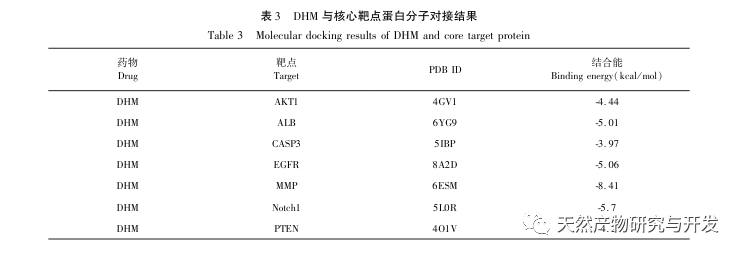
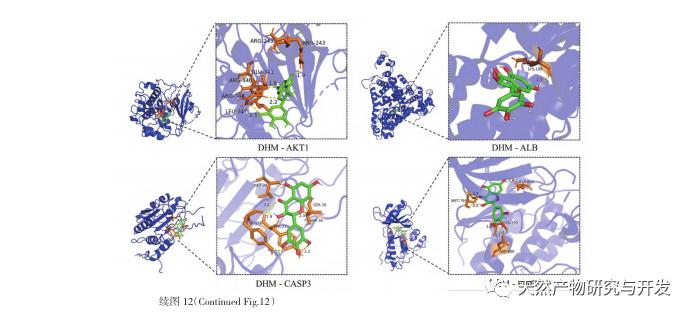
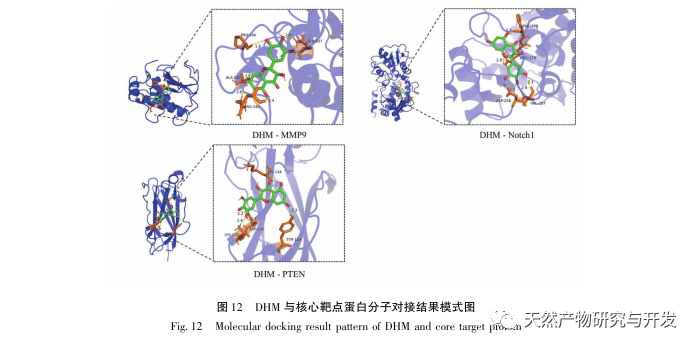
Die molekularen Docking-Ergebnisse zeigten, dass DHM eine gute Bindungsaffinität mit den fünf ausgewählten Targets aufwies, was darauf hindeutet, dass die Wirksamkeit von DHM bei der Behandlung von DKD auf molekularer Ebene validiert wurde. Darüber hinaus stellten wir fest, dass das Hauptzielgen AKT1, das beim Screening an erster Stelle stand, durch die Anreicherungsanalyse des KEGG-Signalwegs eng mit dem AGE-RAGE-Signalweg und dem FoxO-Signalweg bei der Entwicklung von DKD verbunden war. Der AGE-RAGE-Signalweg kann in Synergie mit dem PI3K/Akt-Signalweg oxidativen Stress und chronische Entzündungen in den Nieren hervorrufen, was zu Nierenerkrankungen führt. Die Aktivierung des PI3K/Akt/FoxO3a-Signalwegs kann die physiologische Funktion der Niere bei Diabetes verbessern. Daher haben wir weiter versucht, die Interaktion zwischen dem Notch-Signalweg vor AKT1 und DHM zu untersuchen und eine molekulare Docking-Validierung durchgeführt. Die Ergebnisse des molekularen Dockings zeigten, dass DHM eine gute Bindungsaffinität mit Notch1 und PTEN aufweist.
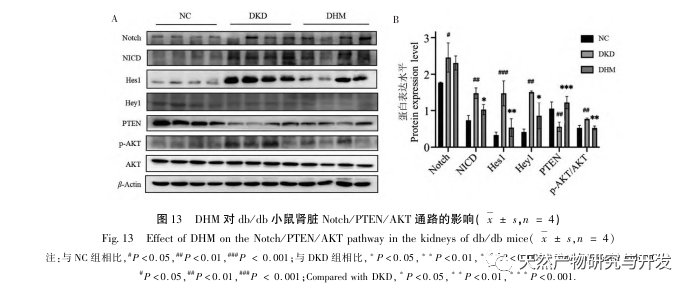
Frühere Studien haben gezeigt, dass der Notch-Signalweg während der Entwicklung von DKD überaktiviert ist, was sich in einer erhöhten Expression von Notch1, NICD, Hes1 und Hey1 zeigt. Inhibitoren von Notch1 können PTEN aktivieren, indem sie die Aktivierung von Hes1 verringern und so die Autophagiestörungen verbessern und das Auftreten von RF verlangsamen. Darüber hinaus haben andere Studien ergeben, dass die PTEN-Aktivierung auch das Fortschreiten der DKD durch Hemmung des PI3K/Akt-Signalwegs abmildern kann. Auf der Grundlage der oben genannten Ergebnisse spekulieren wir, dass DHM die DKD durch Regulierung des Notch/PTEN/AKT-Signalwegs verbessern kann. Western-Blot-Ergebnisse zeigten eine abnorme Zunahme der Aktivierung des Notch-Signalwegs, eine Abnahme der PTEN-Expression und eine Zunahme der AKT-Phosphorylierung in den Nieren von db/db-Mäusen. Die Einnahme von DHM kann die Aktivierung des Notch-Signalwegs hemmen, PTEN aktivieren und die Phosphorylierung von AKT hemmen. Obwohl die Notch/PTEN/AKT-Signalachse als ganzer Signalweg nur selten auf den Nierenschutz bei Diabetes untersucht wurde, hat unsere Forschung die einschlägige Forschung bis zu einem gewissen Grad verbessert und den molekularen Mechanismus des biologischen Schutzes von DHM durch mehrere Ziele bereichert.
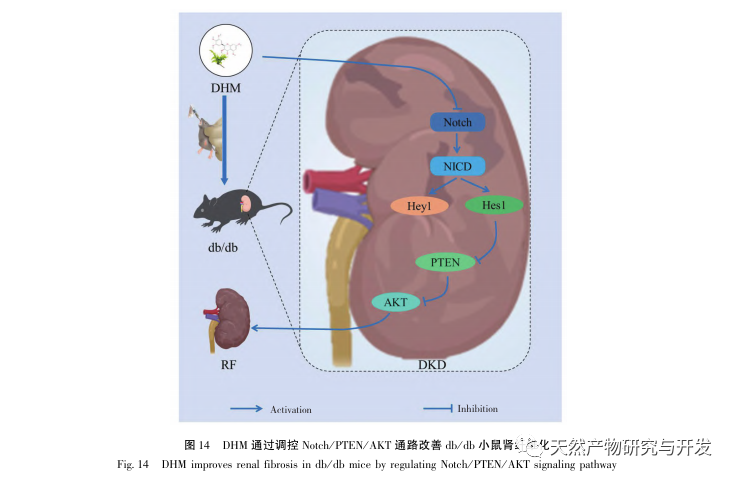
Zusammenfassend lässt sich sagen, dass diese Studie, basierend auf der Beobachtung, dass DHM die pathologischen Manifestationen von DKD verbessert, die Netzwerk-Pharmakologie und die molekulare Docking-Technologie kombiniert hat, um vorläufig zu zeigen, dass die Rolle von DHM bei der Verbesserung des Fortschreitens von DKD durch Schlüsselziele wie AKT1, ALB, CASP3, EGFR, MMP9, IGF1, PPARG, KDR, MMP2, ACE erreicht werden kann, und die relevanten Pfade analysiert hat; Schließlich wurde eine vorläufige Validierung und Analyse der potenziellen AKT-Ziele von DHM durch Tierversuche durchgeführt, und es wurde festgestellt, dass DHM eine Rolle bei der Vorbeugung und Behandlung von DKD durch die Regulierung des Notch/PTEN/AKT-Signalwegs spielen könnte (siehe Abbildung 14). Allerdings gibt es derzeit relativ wenig Forschung zu den Komplikationen von DHM bei T2DM, und sein therapeutisches Potenzial muss noch weiter untersucht werden.
