Флавоноиды из внешней кожицы кислой сои и оценка их антиоксидантной активности
Tamarinus indica Linn. - бобовое растение, плоды которого также известны как Luo Huang Zi, Кислый рог, Сладкий рог, Luo Wang Zi и др. Родом из Африки, в настоящее время культивируется в различных тропических регионах. Обычно встречается в Тайване, Фуцзяне, Гуандуне, Гуанси, южной, центральной и северной Юньнани (долина реки Цзиньша). Кислые бобы имеют долгую историю использования в медицине. В "Сборнике лекарственных средств" говорится, что "Ло Хуан Цзы... лечит рост насекомых в органах и боли в животе, вызванные тем, что дети едят землю"; в "Дянь Нань Бэнь Цао" говорится, что "кислые пельмени... лечат превращение вина в флегму и изолируют ее в желудке". Кислые бобы содержат различные структурные типы веществ, такие как флавоноиды, антоцианы, олигомерные антоцианы, терпены, полисахариды и органические кислоты, которые обладают такими биологическими свойствами, как антиоксидантное, противовоспалительное, антивозрастное и понижающее кровяное давление.
В последние годы все больше исследований посвящено цветкам, листьям, плодам и семенам кислой фасоли как на внутреннем, так и на международном уровне. Однако в настоящее время имеется мало сообщений о составе и активности внешней кожицы кислой фасоли. Для выяснения состава и антиоксидантной активности внешней кожицы кислых бобов в данном эксперименте изучались химический состав и антиоксидантная активность ацетонового экстракта из внешней кожицы кислых бобов, чтобы обеспечить научную основу для последующего лечения и развития кислых бобов.
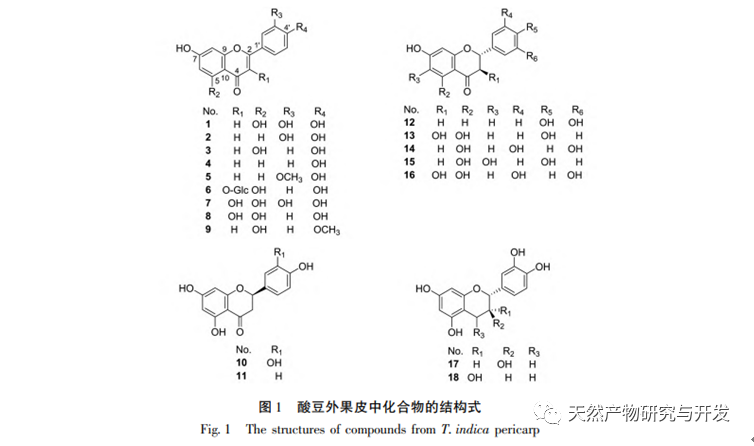
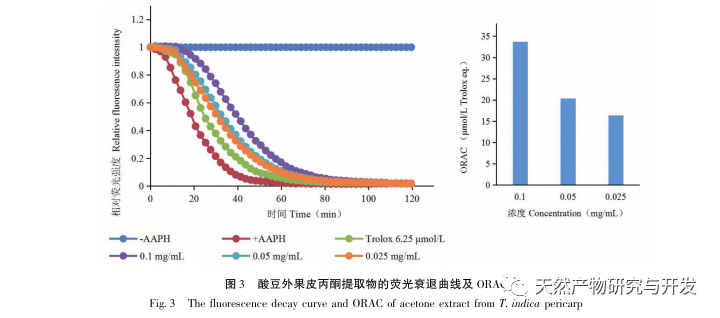
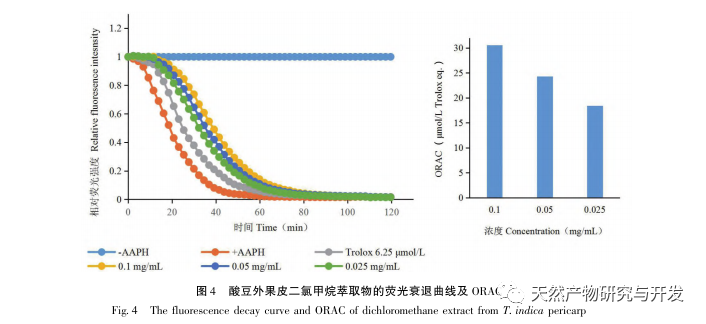
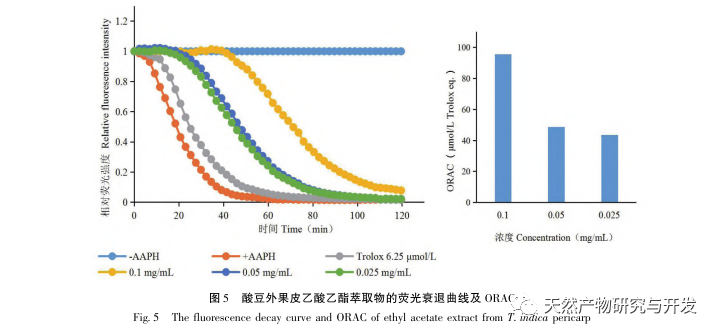
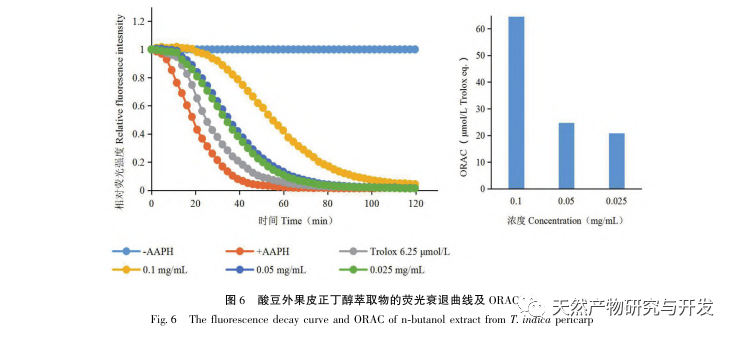
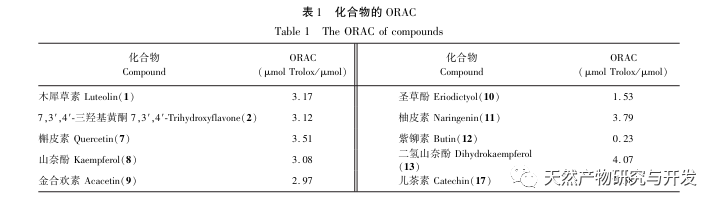
Кислые бобы содержат различные структурные типы веществ, такие как флавоноиды, органические кислоты, антоцианы, олигомерные антоцианы, полисахариды и терпены. Однако внешняя оболочка кислых бобов часто игнорируется как побочный продукт пищевой промышленности. В этом эксперименте из внешней кожицы кислой фасоли было выделено 18 флавоноидных соединений, включая 6 флавоноидов (1-5, 9), 2 флавонола (7, 8), 5 дигидрофлавоноидов (10-12, 14, 15), 2 дигидрофлавонола (13, 16), 2 флаванола (17, 18) и один флавоноидный гликозид (6). Среди них 10 соединений (2, 4-6, 9, 11, 13-16) были выделены из растений этого рода впервые, что свидетельствует о том, что внешняя оболочка кислой фасоли содержит большое количество флавоноидов, что согласуется с большим количеством компонентов, содержащихся в кислой фасоли. Результаты эксперимента ORAC показали, что ацетоновый экстракт, дихлорметановый экстракт, этилацетатный экстракт, н-бутанольный экстракт и 9 соединений (1, 2, 7-10, 12, 13, 17) из внешней кожицы кислой фасоли обладали хорошей антиоксидантной активностью in vitro.
Антиоксидантная активность флавоноидов тесно связана с их структурой, и количество и расположение гидроксильных групп, а также наличие карбонильных групп в С-кольце оказывают определенное влияние на антиоксидантную активность флавоноидов. В связи с непосредственным участием фенольных гидроксильных групп в выжигании свободных радикалов, количество замещенных фенольных гидроксильных групп играет важную роль в антиоксидантном действии флавоноидов. Результаты эксперимента показали, что значение ORAC дигидрокаемпферола в типе дигидрофлавоноидов было выше, чем у нарингенина, а кверцетина - выше, чем у других типов флавоноидов, таких как лютеолин и каемпферол. Как видно, чем больше гидроксильных групп, тем сильнее антиоксидантная способность соединения. Исследования показали, что основным местом антиоксидантной активности флавоноидов является замещение гидроксильных групп в кольце В, при этом наиболее сильной активностью обладает фенольная гидроксильная группа, примыкающая к кольцу В. Это явление может быть связано с тем, что прилегающая фенольная гидроксильная группа в кольце В более восприимчива к электронной атаке. Результаты экспериментов показывают, что количество гидроксильных групп в магнололе и каэмпфероле одинаково, но значение ORAC у магнолола выше. Предполагается, что гидроксильная группа B-кольца может обладать большей антиоксидантной активностью, чем гидроксильная группа A-кольца, а примыкающая к ней фенольная гидроксильная группа играет важную роль; Двойные связи являются электроноакцепторными группами, и их индукционный эффект может снизить антиоксидантную способность флавоноидов. Присутствие двойных связей также может продлить сопряженную систему флавоноидов, повысить стабильность продуктов свободных радикалов и улучшить антиоксидантную активность; Результаты эксперимента показали, что при одинаковых заместителях значение ORAC дигидрокаэмпферола больше, чем каэмпферола, а значение ORAC пурпурина больше, чем 7,3',4'-тригидроксифлавона. Видно, что влияние наличия двойных связей С-кольца на антиоксидантную активность еще требует изучения; значение ORAC дигидрокаэмпферола значительно выше, чем у катехинов, что свидетельствует о том, что наличие 4-карбонильной группы оказывает определенное стимулирующее влияние на антиоксидантную активность. В ходе данного эксперимента были проанализированы антиоксидантные эффекты некоторых флавоноидов и взаимосвязь между их структурами, а также проверены соответствующие выводы о влиянии указанных структур на силу антиоксидантной способности.
