Erforschung des Mechanismus von Taro acuminata gegen Brustkrebs anhand von UPLC-Q-TOF-MS/MS und Netzwerkpharmakologie
Weltweit ist Brustkrebs für 10% der Inzidenz aller Krebsarten und 15% der tumorbedingten Sterblichkeit bei Frauen verantwortlich. Der jüngste von der Weltgesundheitsorganisation veröffentlichte Global Cancer Report 2020 zeigt, dass im Jahr 2018 2,1 Millionen neue Fälle von Brustkrebs auftraten und 27000 Menschen an Brustkrebs starben, was eine ernsthafte Bedrohung für die menschliche Gesundheit darstellt. Daher ist eine wirksame Behandlung von Brustkrebs besonders wichtig. Nach der Theorie der Syndromdifferenzierung und -behandlung hat die traditionelle chinesische Medizin eine offensichtliche heilende Wirkung auf Brustkrebs, indem sie die Funktionen des Körpers, wie Yin, Yang, Qi, Blut, Eingeweide und Meridiane, anpasst. Die traditionelle chinesische Medizin kann den Stoffwechsel des Körpers verbessern, die Gesamtfunktion des Körpers der Patientin regulieren und das Wiederauftreten und die Metastasierung von Brustkrebs reduzieren, um die klinische Wirksamkeit zu verbessern.
Die Wurzel und der Stamm von Alocassia cuculata (Lour.) Schott, einer Pflanze aus der Familie der Araceae, sind ein traditionelles Volksheilmittel, das hitzeabbauend, entgiftend, abschwellend und schmerzlindernd wirkt. Moderne pharmakologische Studien haben gezeigt, dass Taro Immunfaktoren aktivieren kann, um die Aktivität verschiedener Tumorzellen, wie z. B. Melanome, zu hemmen, die körpereigene Immunabwehr zu verbessern, die Apoptose von Krebszellen herbeizuführen und antitumorale Wirkungen zu entfalten. Die damit verbundenen molekularen Mechanismen umfassen Signalwege wie MAPK und PI3K Akt. In der Literatur wird berichtet, dass die Petroletherfraktion von Alocasia cucullata (EAC) die Proliferation von MDA-MB-231 Brustkrebszellen in vitro Zellexperimenten hemmen kann. Der Mechanismus steht im Zusammenhang mit der Hemmung der p-ERK/ERK-Expression im MAPK-Signalweg. Gleichzeitig ist die Petroletherfraktion von Alocasia cucullata laut GC-MS-Analyse reich an verschiedenen ungesättigten Fettsäuren wie Linolsäure und verschiedenen Phytosterinen wie γ-Sitosterol. Moderne Forschungen zeigen, dass ungesättigte Fettsäuren wie Linolsäure und Phytosterole die Apoptose von Brustkrebszellen durch Regulierung des Bax/Bcl-2-Spiegels auslösen können. Dies deutet darauf hin, dass der brustkrebshemmende Mechanismus der Petroletherfraktion von Taro auch mit der Regulierung des Bax/Bcl-2-Spiegels zusammenhängen könnte. Allerdings ist die Forschung über die chemische Zusammensetzung des Petroletheranteils von Taro acuminata derzeit nur auf die GC-MS-Analyse beschränkt, und es gibt keinen relevanten Bericht über den Mechanismus der brustkrebshemmenden Wirkung des Petroletheranteils von Taro acuminata in vivo. Die Forschung über die materielle Grundlage seiner Wirksamkeit und den Mechanismus der Anti-Brustkrebs-Wirkung in vivo ist relativ schwach. Der Wachstumszustand und die Metastasierungsstelle des 4T1 Zelltransplantationstumormodells können den menschlichen fortgeschrittenen Brustkrebs gut simulieren und sind ein gutes Modell für die Bewertung von Medikamenten gegen fortgeschrittenen Brustkrebs. Daher wurde in dieser Arbeit der Petrolether-Teil von Taro acuminata als Forschungsobjekt genommen, und die chemische Zusammensetzung des Petrolether-Teils von Taro acuminata wurde durch UPLC-Q-TOF-MS/MS bestimmt, während die Netzwerk-Pharmakologie-Strategie in Kombination mit molekularer Docking-Technologie verwendet wurde, um die molekulare Ebene des Anti-Brustkrebs-Mechanismus des Petrolether-Teils von Taro acuminata zu klären. Schließlich wurde die brustkrebshemmende Wirkung des Petrolether-Teils von Taro acuminata acuminata in vivo anhand des 4T1-Brustkrebstumor-Mausmodells bewertet und sein brustkrebshemmender Mechanismus überprüft. Um experimentelle Referenzen für die vertiefte Forschung und Entwicklung des Spitzschwanz-Taros zu liefern.
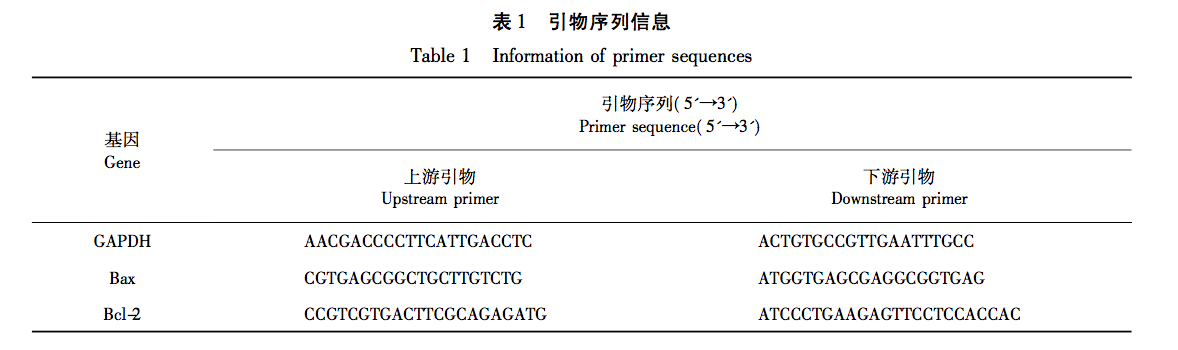
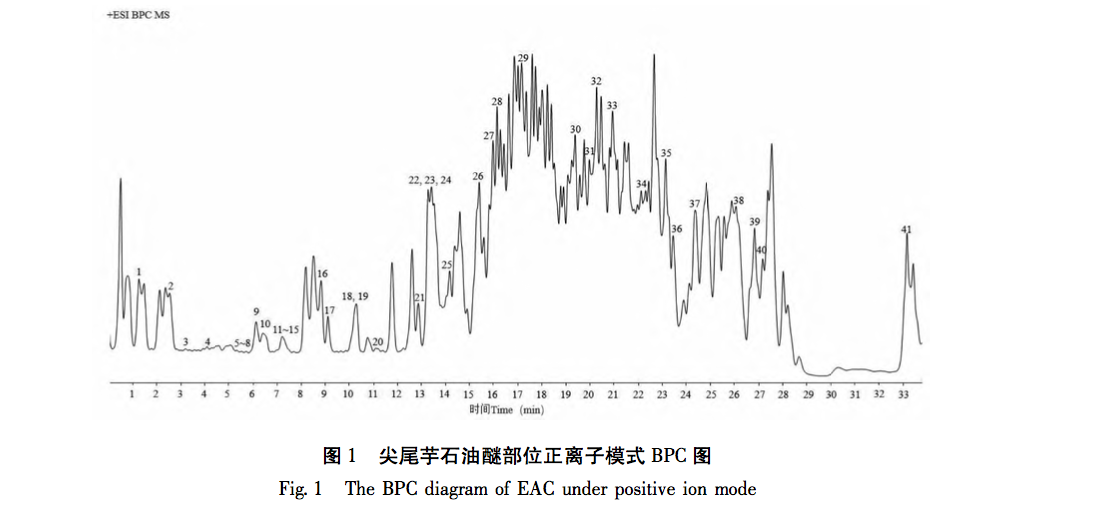


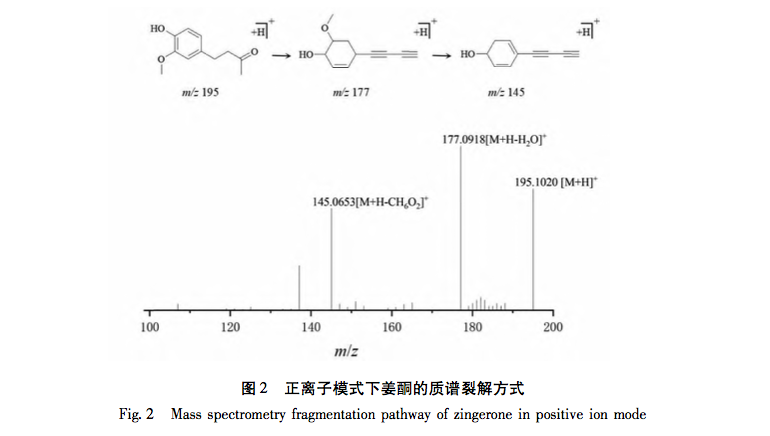
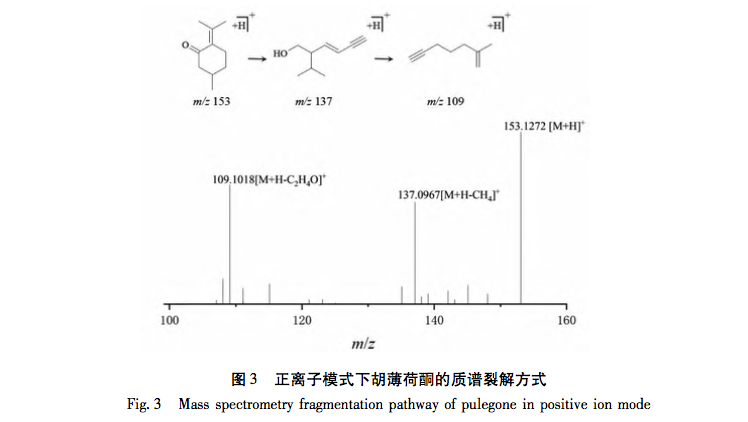
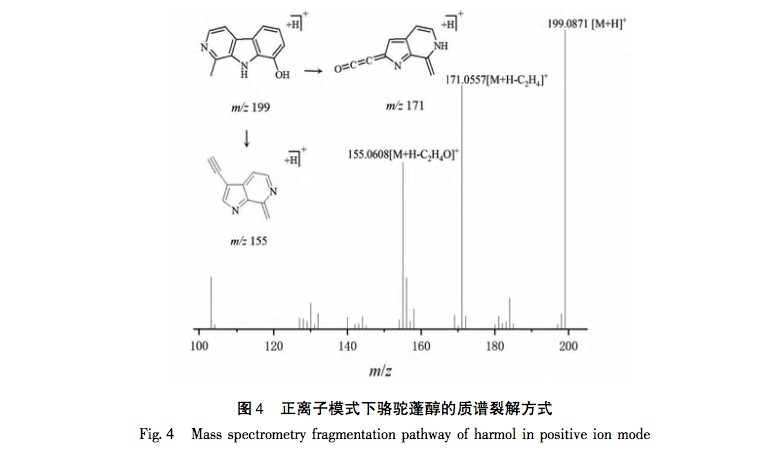


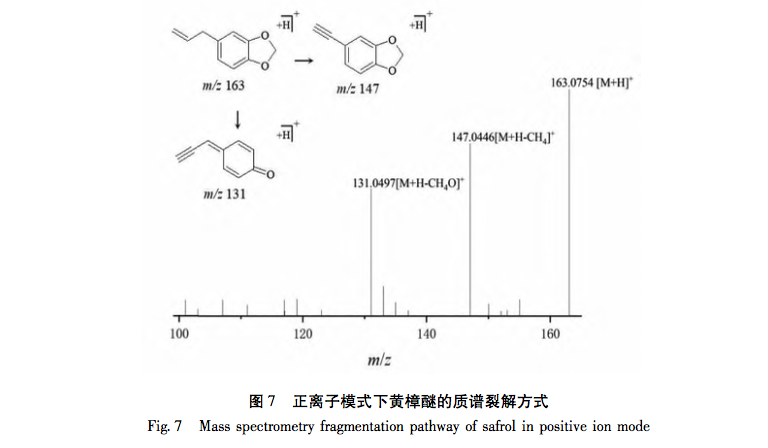
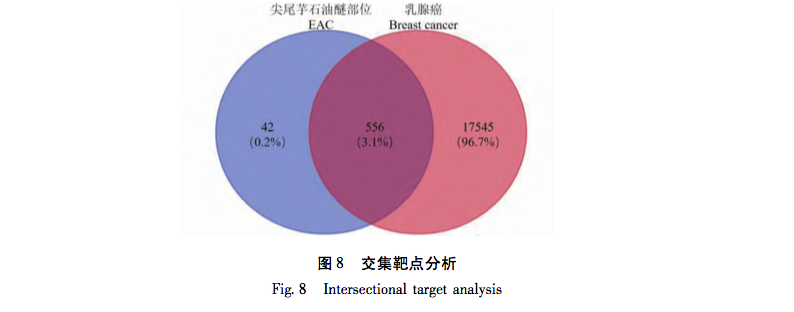
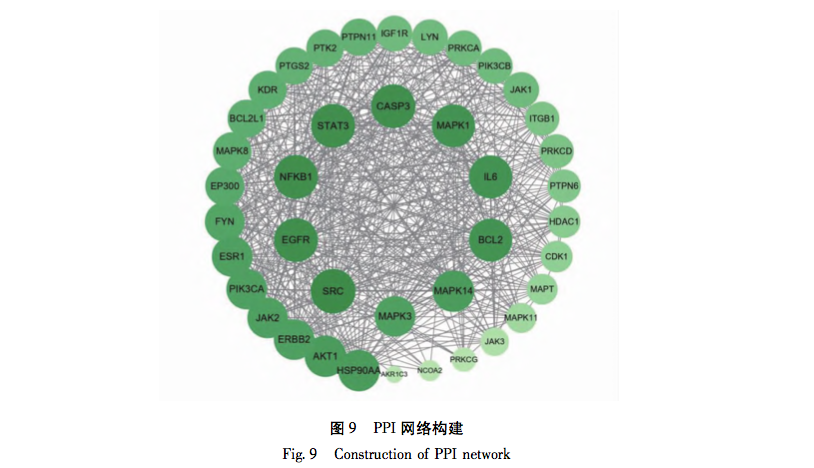

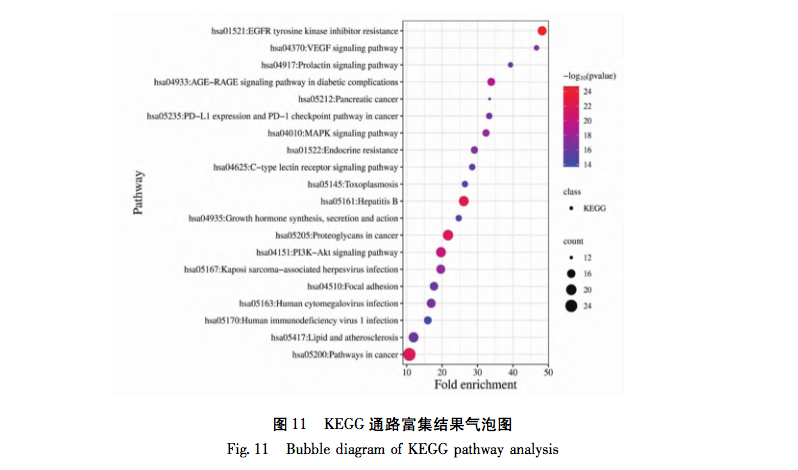


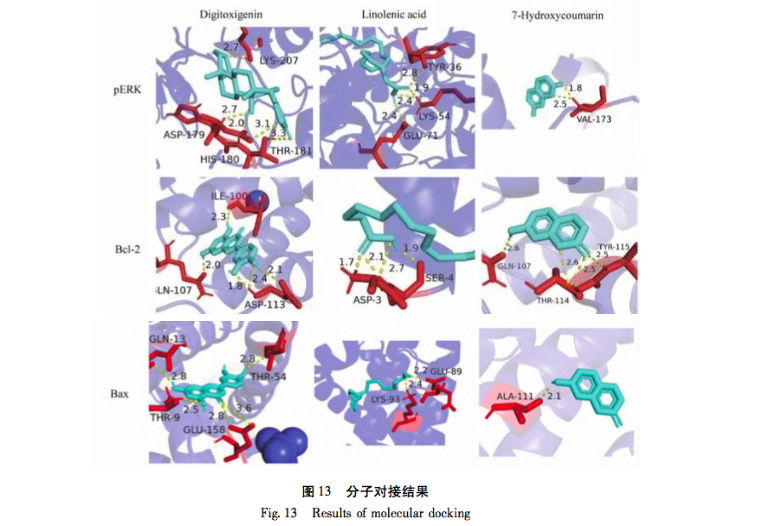




In dieser Studie wurde die UPLC-Q-TOF-MS/MS-Technologie zur Analyse von 41 chemischen Komponenten der Petroletherfraktion von Taro verwendet. Zur gleichen Zeit, 32 Anti-Brustkrebs-Wirkstoffe und 556 Anti-Brustkrebs verwandte Ziele wurden aus dem Petroleum Ether Fraktion von Tara acuminata durch Netzwerk-Pharmakologie-Strategie analysiert. 40 Kernziele wie MAPK1 und Bcl-2 wurden durch das PPI-Netzwerk vorhergesagt, und diese Ziele waren hauptsächlich in der MAPK-Proteinfamilie und der PI3K-Proteinfamilie konzentriert. Darüber hinaus zeigte die GO-Anreicherungsanalyse für biologische Prozesse, dass der biologische Prozess der Petroletherfraktion von Tara acuminata gegen Brustkrebs hauptsächlich an der negativen Regulierung der Zellapoptose und anderer biologischer Prozesse beteiligt ist. Die Analyse der Anreicherung von KEGG-Signalwegen zeigte, dass die Anreicherung von Petroletherfraktion von Tara acuminata gegen Brustkrebs hauptsächlich in PI3K-Akt- und MAPK-Signalwegen stattfand, die beide mit der Zellapoptose verbunden sind. Das PPI-Netzwerk sagte voraus, dass MAPK1, Bcl-2 und andere mit Apoptose zusammenhängende Kerntargets erhalten wurden, und durch molekulare Docking-Technologie wurde weiter verifiziert, dass der Sterolbestandteil Digitalisglykosid-Ligand, der Fettsäurebestandteil Linolensäure und der Cumarinbestandteil 7-Hydroxycumarin frei (Bindungsenergie<0 kcal/mol) mit den verwandten Kerntargets (p-ERK, Bcl-2, Bax) des Petroletheranteils von Amorphophallus senticosus für Brustkrebs binden konnten. Die obigen Ergebnisse deuten darauf hin, dass die brustkrebshemmende Wirkung der Petroletherfraktion von Taro mit ihren Multikomponenten- und Multitarget-Eigenschaften zusammenhängt und ihr brustkrebshemmender Mechanismus mit Apoptose-bezogenen Signalwegen wie PI3K Akt und MAPK zusammenhängt.
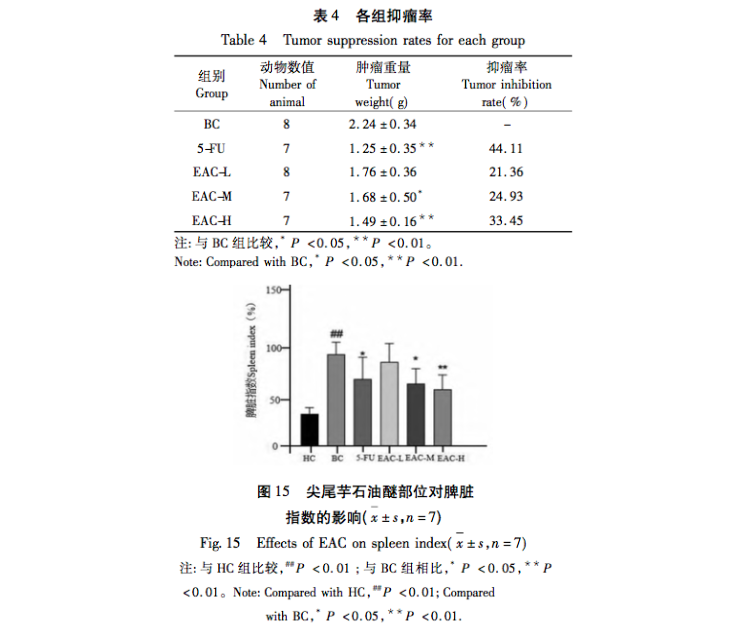
Jianwei Taro wird in der Volksmedizin häufig zur Behandlung verschiedener Krebsarten verwendet, und die in seinen Knollen enthaltenen Verbindungen können das Wachstum verschiedener Krebszellen hemmen. Bei früheren Untersuchungen unserer Forschungsgruppe wurde festgestellt, dass der Wasserextrakt aus Taro das Wachstum von Brustkrebs hemmen und die Überlebenszeit von Mäusen mit Brustkrebs verlängern kann, indem er die Aktivität der Milzzellen von Mäusen erhöht. Im Zellexperiment wurde festgestellt, dass Taro die Differenzierung von Immunmonozyten in Makrophagen erheblich katalysieren, die Funktion von Megaphagozyten stimulieren und das Immunsystem aktivieren kann, um eine Anti-Tumor-Wirkung zu erzielen. Die Petroletherfraktion von Taro kann das Wachstum von menschlichen MDA-MB-231-Brustkrebszellen hemmen und die Apoptose von Krebszellen fördern. Die Ergebnisse dieses Experiments zeigten, dass die Petroletherfraktion von Taro die Wachstumsrate von Brustkrebs in tumortragenden Mäusen hemmen und das Tumorgewicht reduzieren kann, und die Tumorhemmungsrate zeigte einen konzentrationsabhängigen Trend. Die Milz ist ein wichtiges Immunorgan bei Tieren, das die Auswirkungen von Arzneimitteln auf das Immunsystem widerspiegeln kann. Die Mäuse in den Gruppen mit mittlerer und hoher EAC-Dosis, die oral verabreicht wurden, wiesen einen höheren Milzindex und signifikante Unterschiede im Vergleich zu den Mäusen der Modellgruppe auf, was darauf hindeutet, dass die Petroletherfraktion von Taro die Immunfunktion von tumortragenden Mäusen verbessern kann. Die Ergebnisse der HE-Färbung des Tumorgewebes zeigten, dass die Tumorzellen in der Modellgruppe der Mäuse dicht wuchsen, während die 5-Fluorouracil-Gruppe und die mit Taro behandelte Gruppe eine lockere Zellanordnung, verschwommene Zellkonturen und offensichtliche nekrotische Bereiche der Tumorzellen aufwiesen, was auf eine Membranruptur der Tumorzellen hinweist. Die Petrolether-Seite von Taro könnte die Apoptose von Tumorzellen induzieren.
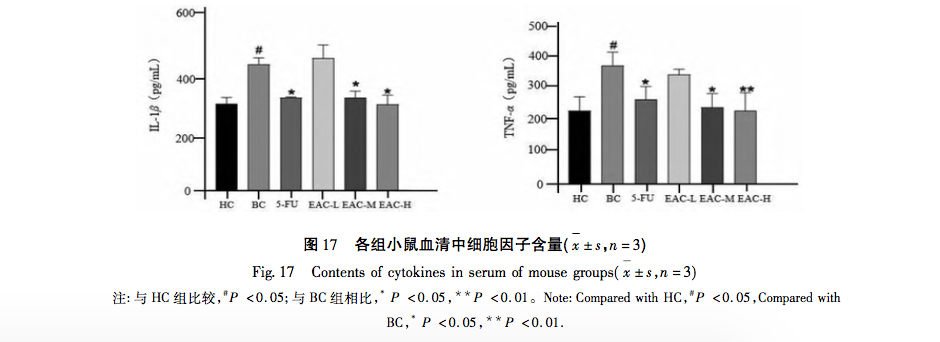
Zahlreiche Studien haben gezeigt, dass Entzündungen bei einer Vielzahl von Krankheiten eine Rolle spielen können, darunter Herz-Kreislauf-Erkrankungen, Krebs, Diabetes, Arthritis, Alzheimer usw. Das anhaltende Vorhandensein von ursächlichen Faktoren kann zu einer Entzündung führen, die nicht beseitigt werden kann, und die Entzündung kann chronisch werden, was zu Zellmutationen und -proliferation führt, was das Auftreten und die Entwicklung von Krebs begünstigt. Der Tumor-Nekrose-Faktor (TNF) ist eines der wichtigsten proinflammatorischen Zytokine. Die Mikroumgebung im Zusammenhang mit Brustkrebs ist durch chronische Entzündungen gekennzeichnet. TNF-α kann das Auftreten und die Entwicklung von Tumoren fördern, indem es den Östrogenstoffwechsel in Tumorzellen und umgebenden Stromazellen stimuliert und Östrogen anreichert. Studien haben ergeben, dass exogenes TNF-α die Apoptose von Tumorzellen in MDAMB-468-, SK-BR3- und MDA-MB-231-Zellen nicht auslösen kann, während endogenes TNF-α in HS578T-Zellen eine schützende anti-apoptotische Wirkung hat. Zu den Hauptquellen des pro-inflammatorischen Zytokins Interleukin-1 β (IL-1 β) gehören myeloische Zellen wie MDSCs, Makrophagen und DCs, die eine Rolle bei der Förderung des Tumorwachstums oder der Verstärkung der Anti-Tumor-Immunerkennung in der Tumor-Mikroumgebung spielen. Es hat sich gezeigt, dass IL-1 β die Anhäufung von MDSCs in unreifen myeloischen Zellen in der Tumormikroumgebung fördert und dadurch die Tumorprogression begünstigt. In dieser Studie wurde durch ELISA-Kit-Nachweis festgestellt, dass im Vergleich zur Modellgruppe die TNF-α- und IL-1-β-Spiegel im Serum der positiven Arzneimittelgruppe und der Gruppen, die mit verschiedenen Konzentrationen von Taro behandelt wurden, reduziert waren, wobei die hochdosierte Gruppe die niedrigsten Werte aufwies. Daher wird spekuliert, dass die Petroletherfraktion von Taro nach der Tumorinokulation in Mäusen die Tumorentwicklung hemmen kann, indem sie die pro-inflammatorischen Zytokinspiegel reduziert. Zusammenfassend lässt sich sagen, dass die Petroletherfraktion von Taro acuminata eine signifikante Wirkung gegen Brustkrebs in vivo hat.
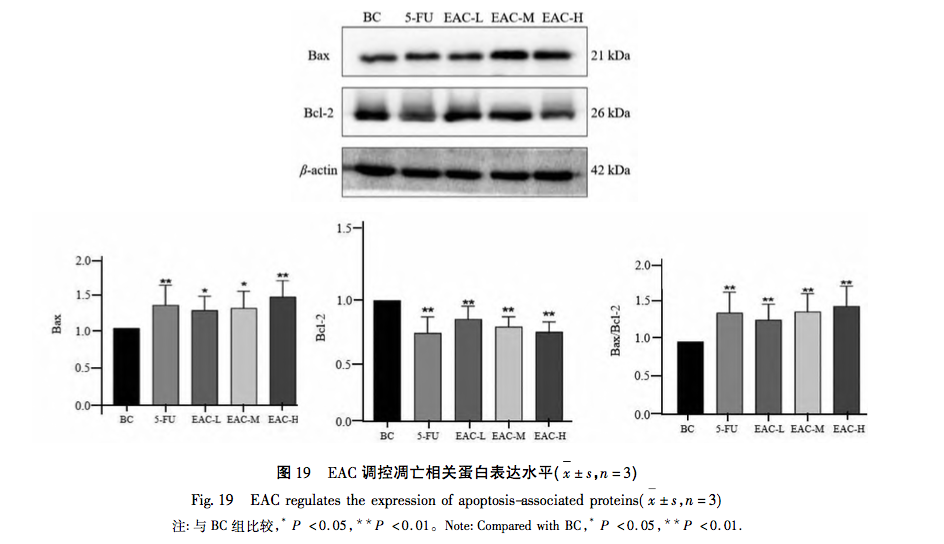
MAPK ist eine Serinproteinkinase, die zum endogenen apoptotischen Signalweg gehört. ERK, JNK und p38 sind die drei wichtigsten Signalwege, die bei Säugetieren entdeckt wurden, mit unterschiedlichen Aktivierungszuständen. Sie sind nach ihrer Aktivierung an den Signalwirkungen verschiedener Wachstumsfaktoren, Zytokine und Hormonrezeptoren beteiligt und regulieren das Zellwachstum und die Zelldifferenzierung. In dieser experimentellen Studie wurde kein signifikanter Unterschied in den Konzentrationen der Proteine des MAPK-Signalwegs, ERK, JNK, p38, p-JNK und p-p38 festgestellt, und die Expression des p-ERK-Proteins wurde reduziert, was darauf hindeutet, dass der Petroletheranteil von Taro eine Rolle bei der Bekämpfung von Brustkrebs spielen kann, indem er die Expression von p-ERK/ERK hemmt, was mit den Ergebnissen früherer Studien in vitro und der netzwerkpharmakologischen Vorhersage verwandter Wege übereinstimmt. Darüber hinaus kann EAC die Expression von Bax/Bcl-2-Protein und das Niveau des Apoptose-Gens Bax/Bcl-2 mRNA erhöhen, was darauf hindeutet, dass EAC eine Rolle bei der Bekämpfung von Brustkrebs spielt, indem es die Apoptose von Tumorzellen fördert.
Zusammenfassend lässt sich sagen, dass die Petroletherfraktion von Taro das Tumorwachstum von Mäusen mit 4T1-Brustkrebs hemmen kann. Seine brustkrebshemmende Wirkung ist auf seine Multikomponenten- und Multi-Target-Eigenschaften zurückzuführen. Der Mechanismus könnte mit der Herunterregulierung der p-ERK/ERK-Expression, der Erhöhung der Bax/Bcl-2-Expression, der Erhöhung des Bax/Bcl-2-mRNA-Niveaus und der Förderung der Apoptose der Tumorzellen zusammenhängen. Diese Studie liefert eine theoretische Referenz für die klinische Anwendung von Taro acuminata bei der Behandlung von Brustkrebs, aber die tieferen materiellen Grundlagen der Wirksamkeit, des Ziels und des Mechanismus müssen weiter erforscht werden.
