Háromszáz PI3K/AKT/mTOR útvonalon alapuló rúd elősegíti a lipopoliszacharid indukálta autofágiát és gátolja a gyulladást a RAW264.7 sejtekben
A lipopoliszacharid (LPS) egy Gram-negatív baktériumok által kibocsátott endotoxin, amely az emberi szervezetben a Gram-negatív baktériumfertőzések által okozott bakteriális toxicitás során az immunrendszer gyulladásos válaszreakcióit serkentheti. A makrofágok gyakran részt vesznek a gyulladásos válaszokban és a fagocitózisban, és az LPS-sel kezelt RAW 264.7 makrofágvonal az immunsejtek gyulladásos válaszainak gyakran használt sejtmodellje. Az autofágia egy olyan katabolikus folyamat, amelyben a citoplazma tartalmát az autofágoszómák a lizoszómákba szállítják, ahol a sejtek homeosztázisának fenntartása érdekében kiterjedt lebontásra kerül. Az autofágia, mint fontos sejtmechanizmus, részt vesz különböző betegségek, például autoimmun betegségek, gyulladásos betegségek és daganatok kialakulásában és fejlődésében. A gyulladásos válasz a szervezet szöveteinek egyfajta immunvédelmi funkciója. A mérsékelt gyulladásos válasz segít a szervezet károsodásának kijavításában, de a túlzott gyulladásos válasz káros reakciókhoz vezethet a szervezetben, a szervek, szövetek és sejtek degenerációját és elhalását okozva, és akár az életet is veszélyeztetve. Számos tanulmány kétirányú kommunikációt talált az autofágia és a gyulladás között. A mérsékelt autofágia gyengítheti a gyulladásos választ, de a túlzott autofágia súlyosbíthatja a gyulladásos választ. Több immunmediátor indukálhatja vagy gátolhatja az autofágiát, de a homeosztázis helyreállítása nagymértékben az autofágiára támaszkodik. Ezért az autofágia gyulladásra gyakorolt szabályozási mechanizmusának teljes megértése hatékonyan kezelheti a gyulladásos és autoimmun betegségeket.
A háromszáz pálcika a Toddalia asiatica (L.) Lam, a Rutaceae családba tartozó növény gyökeréből származik. A "Tujia gyógyászati feljegyzések" egyértelműen rögzítik a "szél és nedvesség eloszlatását, a vérkeringés elősegítését, az inak ellazítását, a duzzanat csökkentését és a fájdalom enyhítését". Kémiai összetétel-vizsgálatok kimutatták, hogy a Sanbai bot fő kémiai összetevői alkaloidok és kumarinok. A modern farmakológiai kutatások megerősítették, hogy a Sanbai bot kivonata reumaellenes, gyulladáscsökkentő, daganatellenes és egyéb hatásokkal rendelkezik. Előzetes kísérleti kutatásaink kimutatták, hogy a Sanbai bot képes blokkolni az autofágia áramlását a foszfatidil-inozitol-3-kináz/protein kináz B/mammalian rapamycin target protein (PI3K/AKT/mTOR) jelátviteli útvonalon keresztül, ezáltal gátolja az MH7A fibroblaszt sejtvonal proliferációját és apoptózist indukál. A Toddalia asiatica alkoholos kivonat (TAAE) autofágiában betöltött szerepe azonban még kiforratlan. E vizsgálat eredményei azt mutatták, hogy a TAAE koncentrációfüggő módon váltja ki az autofágiát. Annak további ellenőrzése érdekében, hogy a TAAE fontos szerepet játszik-e a RAW 264.7 makrofágok autofágiájában a PI3K/AKT/mTOR útvonalon keresztül, ez a kísérlet LPS stimulált RAW 264.7 sejteket használt modellként, hogy megvizsgálja a TAAE hatását a RAW 264.7 sejtek autofágiájára és immunfunkciójára, és feltárja a veleszületett immunválasz TAAE szabályozásának molekuláris mechanizmusát.
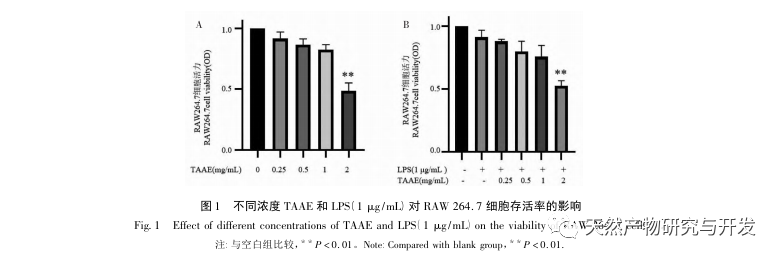
A makrofágok az emberi szervezet egyik fontos immunsejtje. Az emberi szövetekbe és vérbe behatoló kórokozókkal szemben gyorsan képesek stresszállapotokat aktiválni, ami gyulladásos reakciók sorozatához vezet. Fontos veleszületett immunsejtek, amelyek szorosan kapcsolódnak a gyulladások kialakulásához és fejlődéséhez. A gyulladás egy összetett kóros reakció, amelyet az immunrendszer különböző fizikai reakciói okoznak, amikor külső sérülésnek vagy fertőzésnek van kitéve. Számos krónikus betegség, például a neurodegeneratív betegségek, a reumatoid artritisz, az érelmeszesedés stb. patofiziológiájának fontos részét képezi. Egy vizsgálat megállapította, hogy a TAAE képes gátolni a Toll-like receptor 4/nukleáris faktor - κ B (TLR4/NF - κ B) útvonalat, ezáltal csökkenti a kollagén indukálta gyulladásos citokinek, az interleukin-1 β (IL-1 β) és a tumor nekrózis faktor - α (TNF - α) expresszióját patkányok szinóviájában (CIA), gátolja a reumás artritisz szinovitiszét, és elnyomja a reumás artritisz progresszióját. A TAAE gátolhatja az NF - κ B nukleáris belépését is, ezáltal elnyomja a gyulladásos faktorok felszabadulását és gátolja a szinoviális proliferációt. Yang és munkatársai megállapították, hogy a 300 pálcika etanolos és etil-acetát kivonata gátolja az ízületi duzzanatot CIA patkánymodellekben, csökkenti a pro-gyulladásos faktorokat, mint a TNF - α, IL-1 β és interleukin-6 (IL-6), és növeli az immunszuppresszív faktor interleukin-10 (IL-10) expresszióját a szérumban. Mindezek a fentiek a háromszáz pálca kiváló gyulladáscsökkentő és reumaellenes hatását bizonyítják.
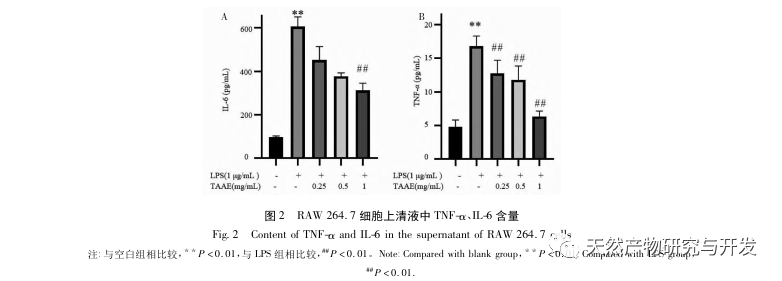
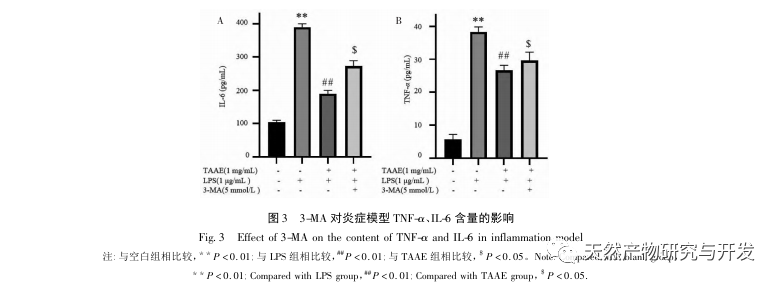
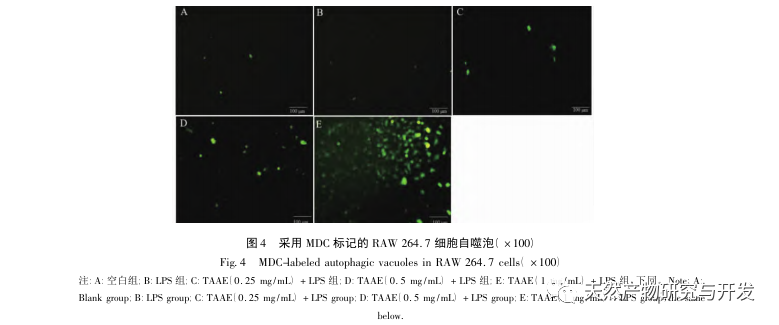
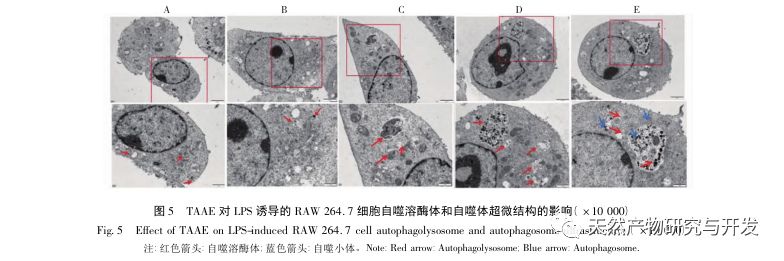
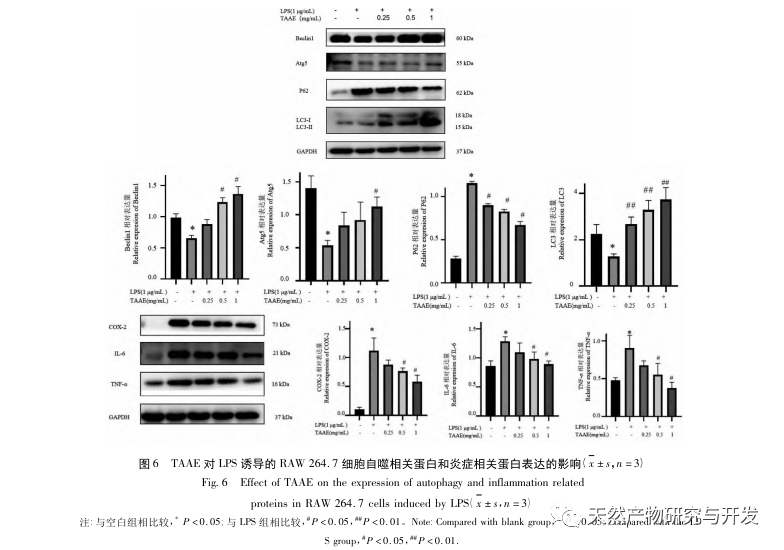
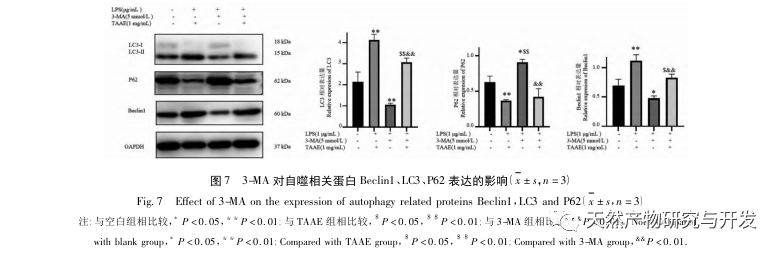
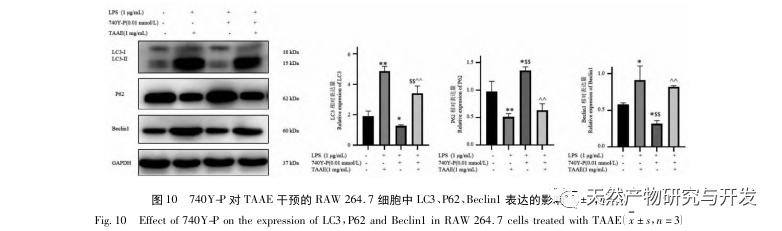
Az autofágia az a folyamat, amelynek során az eukarióta sejtek az autofágiával kapcsolatos gének szabályozásával a lizoszómákat használják fel saját citoplazmatikus fehérjéik és sérült organelláik lebontására. Ez a folyamat képes lebontani a betolakodó patogén mikroorganizmusokat, sérült organellákat és abnormálisan felhalmozódott fehérjéket, és fontos szerepet játszik olyan biológiai folyamatokban, mint a sejtek minőségének ellenőrzése, az anyagcsere, valamint a veleszületett és adaptív immunitás. Számos tanulmány megerősítette, hogy az autofágia kétirányú hatást gyakorol a gyulladásra: egyrészt az autofágia ellensúlyozhatja a gyulladásos válaszokat azáltal, hogy eltávolítja a gyulladásos fehérjeaggregátumokat és leregulálja a szövetkárosodást okozó pro-inflammatorikus citokineket; másrészt az autofágia aktiválja az inflammaszómákat, nagy mennyiségű gyulladásos faktort termelve, ezáltal felgyorsítva a gyulladásos folyamatot. Az immunitás és a gyulladás pozitív és negatív aspektusainak kiegyensúlyozása után az autofágia a fertőzés, az autoimmunitás és a gyulladás védelmezőjének tekinthető. A mikrotubulushoz kapcsolódó fehérje, a könnyű lánc 3-II (LC3-II) az autofágia egyik jellegzetes fehérjéje. Az autofágia során az LC3-I az Atg5-Atg12-Atg16 komplex segítségével egy foszfatidil-etanol molekulához kapcsolódik, és így alakul ki az LC3-II. A P62 az autofágikus lebontás szubsztrátja, amely döntő szerepet játszik a lebontott szubsztrátok felismerésében és bekapszulázásában. Ha a Beclin1-et emlőssejtekben túlexpresszálják, elősegíti a sejtek autofágiáját. Ezért az LC3, a Beclin1, a P62 és az Atg5 az autofágia markerfehérjéiként szolgálhatnak. Annak vizsgálatára, hogy a TAAE által kifejtett gyulladáscsökkentő hatás összefügg-e az autofágiával, ebben a tanulmányban Western blot segítségével kimutattuk az autofágiával kapcsolatos P62, Beclin1, Atg5 és LC3 fehérjék, valamint a gyulladással kapcsolatos TNF - α, IL-6 és ciklooxigenáz-2 (COX-2) fehérjék fehérjeexpresszióját. A kísérleti eredmények azt mutatták, hogy a TAAE beavatkozás után a Beclin1, az Atg5 és az LC3-II/LC3- fehérje expressziós szintje fokozatosan emelkedett, míg a szubsztrát P62 fehérje expressziós szintje fokozatosan csökkent, és a gyulladással kapcsolatos fehérjék expressziója is csökkent. Az autofagoszómák jelölésére szolgáló MDC-módszerrel és az autofagoszómák megfigyelésére szolgáló transzmissziós elektronmikroszkópiával végzett kísérleti eredmények szintén azt mutatták, hogy a TAAE elősegítette az autofágiát a RAW 264.7 sejtekben. Az autofágia gyulladásra gyakorolt hatásának további bizonyítása érdekében a makrofág autofágia kontrollálására, az autofágiás kelátképződés és a fehérjék lebomlásának blokkolására a 3-MA autofágia-inhibitort használtuk, amely egyben a PI3K jelátviteli útvonal specifikus inhibitora is. Az eredmények azt mutatták, hogy a 3-MA autofágia-inhibitor gyengítette a TAAE gyulladásos citokinekre gyakorolt gátló hatását, míg a TAAE beavatkozás hatékonyan csökkentette a TNF - α és IL-6 citokinek szekrécióját a gyulladásos modellben, ismét bizonyítva, hogy a TAAE gyulladáscsökkentő hatást fejt ki az autofágia elősegítésével a RAW 264.7 sejtekben.
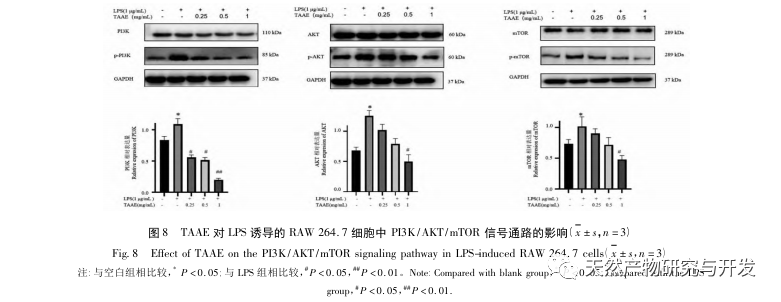
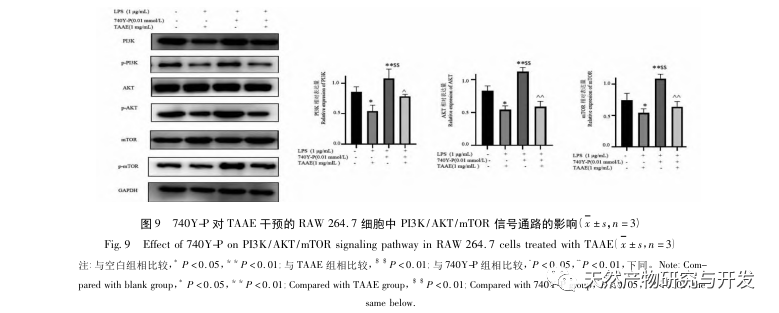
A PI3K/AKT/mTOR jelátviteli útvonal fontos szerepet játszik az autofágia szabályozásában, és az autofágia szintje fokozódik, ha a PI3K/AKT/mTOR útvonal gátolt. Az MTOR a rapamycin emlős célpontja, és fontos szabályozó szerepet játszik az autofágia válaszában, az autofágia kulcsfontosságú negatív szabályozó tengelyeként szolgál. Számos természetes termékről kimutatták, hogy a PI3K/AKT/mTOR által közvetített autofágiát célozva gátolja a gyulladást és az autoimmun betegségeket. Korábbi kísérletek megerősítették, hogy a TAAE a PI3K/AKT/mTOR jelátviteli útvonalon keresztül képes blokkolni az autofágiás áramlást és elősegíteni az MH7A sejtek apoptózisát. A PI3K/AKT/mTOR jelátviteli útvonalat Western blottinggal validáltuk, és a kísérleti adatok azt mutatták, hogy a TAAE jelentősen csökkentette a foszforilált PI3K, AKT és mTOR expressziós szintjét, ami azt jelzi, hogy a TAAE a PI3K/AKT/mTOR útvonal gátlásával váltja ki az autofágiát. A PI3K agonista (740Y-P) egyidejű alkalmazása tovább bizonyította, hogy a TAAE a PI3K/AKT/mTOR jelátviteli útvonal gátlásával indukálja az autofágiát. Ezenkívül a PI3K/AKT/mTOR jelátviteli útvonal közvetlenül kapcsolódik a gyulladáshoz és az immunitáshoz. Ez a vizsgálat megállapította, hogy a TAAE kezelés csökkentette a pro-inflammatorikus citokinek szintjét az LPS által indukált RAW 264.7 sejtekben. Ez a vizsgálat azt mutatja, hogy az LPS által indukált RAW 264.7 sejtek gyulladásos környezetében a TAAE gátolja az autofágiával kapcsolatos PI3K/AKT/mTOR útvonalat, szabályozza az autofágiával kapcsolatos fehérjéket és gyulladásos faktorokat, elősegíti az autofagoszóma lizoszóma fúzióját és degradációját, befolyásolja a gyulladásos sejtek homeosztázisát, gátolja a gyulladásos válaszokat, és így gyulladáscsökkentő hatást fejt ki. E tanulmány eredményei azt sugallják, hogy a PI3K / AKT / MTOR hatékony útvonal a TAAE számára a gyulladáscsökkentő hatások kifejtésére és az autofágikus aktivitás növelésére, ami új ötleteket nyújthat a gyulladással kapcsolatos autoimmun és metabolikus betegségek klinikai kezeléséhez, és érdemes további mélyreható kutatásra.
