12 Nouveaux ingrédients alimentaires approuvés en 2023
1. Streptomyces pseudoentericus
Annonce d'approbation : Annonce de la Commission nationale de la santé sur 28 "Trois nouveaux aliments" dont Leuconostoc pseudomesenteroides (No.1, 2023)
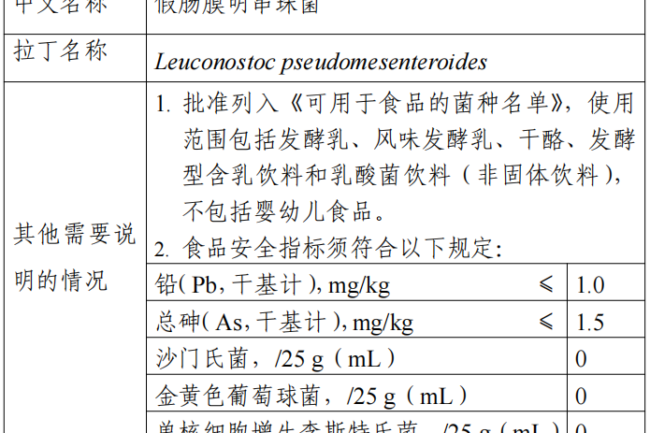
Leuconostoc pseudomesenteroides appartient au genre Leuconostoc et est isolé dans des produits laitiers fermentés traditionnels. Cette souche a été incluse dans la liste des produits biologiques recommandés dans la liste QPS de l'Autorité européenne de sécurité des aliments (EFSA) et dans le Bulletin de la Fédération internationale de laiterie (Bulletin?of?the?IDF?514/2022) "Catalogue of Microbial Species Demonstrated to be Safe in Fermented Foods" et son utilisation a été approuvée dans des pays tels que le Danemark, le Canada et la Corée, la Corée et d'autres pays ont été approuvés.
Conformément à la loi sur la sécurité alimentaire de la République populaire de Chine et aux mesures administratives relatives à l'examen de la sécurité des nouveaux ingrédients alimentaires, la Commission nationale de la santé et du bien-être a chargé l'organisme d'examen d'organiser des experts pour examiner et approuver les documents d'évaluation de la sécurité de Pseudoenteric Membrane Streptomyces conformément aux procédures légales. La production et l'utilisation de nouveaux ingrédients alimentaires doivent être conformes au contenu de l'annonce et aux exigences des réglementations relatives à la sécurité alimentaire.
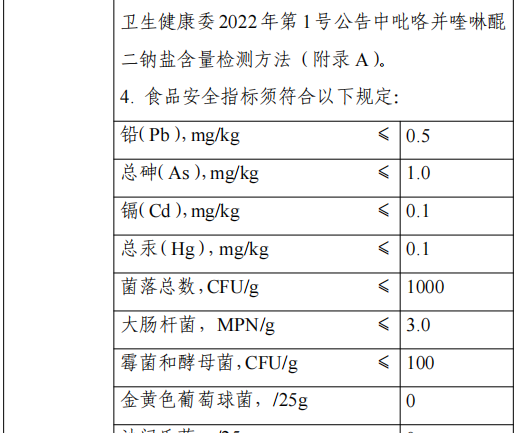
L'utilisation de cette souche comprend le lait fermenté, le lait fermenté aromatisé, le fromage, les boissons à base de lait fermenté et les boissons à base de lactobacilles (boissons non solides), à l'exclusion des aliments pour nourrissons et enfants en bas âge. Les indicateurs de sécurité alimentaire de cette matière première doivent être conformes aux dispositions suivantes : plomb (en tant que Pb, base sèche) ≤ 1,0 mg/kg, arsenic total (en tant que As, base sèche) ≤ 1,5 mg/kg, limites microbiologiques pour Salmonella 0/25 g (mL), Staphylococcus aureus 0/25 g (mL), Listeria monocytogenes 0/25 g (mL). Lorsque les normes nationales de sécurité alimentaire pour les préparations de souches alimentaires seront publiées, elles seront mises en œuvre conformément aux normes pour les préparations de souches alimentaires.
2. anthocyane de myrtille
Annonce d'approbation : Annonce de la Commission nationale de la santé sur 14 types de "trois nouveaux aliments" tels que l'anthocyanine de myrtille (n° 3, 2023)
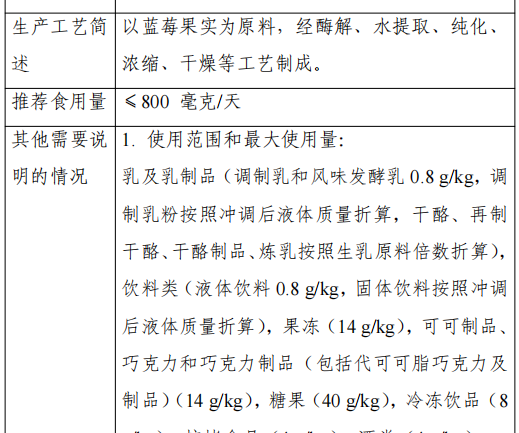
L'anthocyanine de myrtille est une substance poudreuse obtenue à partir du fruit de la myrtille (Vaccinium corymbosum?L.) de la famille des Rhododendrons, par un processus de digestion enzymatique, d'extraction par l'eau, de purification, de concentration et de séchage.
Le Canada approuve l'utilisation de l'extrait de myrtille (teneur en anthocyanes ≥40%) en tant qu'aliment naturel ; l'UE utilise l'anthocyane provenant de sources végétales et fruitières en tant qu'additif alimentaire ; les États-Unis utilisent l'anthocyane provenant de raisins et de peaux de raisins en tant qu'additif alimentaire et autorisent son utilisation dans des boissons et d'autres aliments.
La portion recommandée de ce produit est la suivante : la portion recommandée d'anthocyanoside de myrtille avec 40,0% de teneur totale en anthocyanoside est de 800 mg/jour, et ceux qui dépassent cette teneur sont convertis en fonction de la teneur réelle.
Conformément à la "loi sur la sécurité alimentaire de la République populaire de Chine" et aux "mesures administratives pour l'examen de la sécurité des nouveaux ingrédients alimentaires", la Commission nationale de la santé et de l'hygiène a chargé l'organisme d'examen, conformément aux procédures légales, d'organiser l'évaluation de la sécurité de l'anthocyanoside de myrtille par des experts et de procéder à l'examen et à l'adoption des documents.
La production et l'utilisation de nouveaux ingrédients alimentaires doivent être conformes au contenu de l'annonce et aux exigences des réglementations relatives à la sécurité alimentaire. Compte tenu du manque d'informations sur la sécurité de l'anthocyanine de myrtille chez les nourrissons et les jeunes enfants, les femmes enceintes et les femmes allaitantes, en vertu du principe de prévention des risques, les groupes de personnes susmentionnés ne devraient pas être consommés, l'étiquetage et les instructions devraient être marqués comme étant inappropriés pour la population. Les indicateurs de sécurité alimentaire de la matière première sont conformes à l'annonce.
3. Pollen de seigle
Annonce d'approbation : Annonce de la Commission nationale de la santé sur 14 types de "trois nouveaux aliments" tels que l'anthocyanine de la myrtille (2023 No.3)
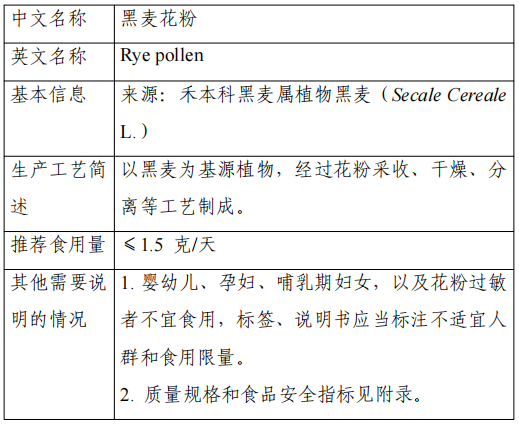
La plante de base de ce produit est le seigle (Secale Cereale L.) de la famille des graminées, originaire d'Asie centrale, de la Méditerranée et d'autres régions, et largement cultivé en Europe. Ce produit est fabriqué à partir du pollen de seigle, qui est récolté, séché et séparé.
Au Japon et en Corée, le pollen de seigle peut être consommé en tant qu'aliment sans que sa plante de base soit limitée à une catégorie d'aliments ; aux États-Unis, le pollen de seigle peut être vendu en tant qu'ingrédient alimentaire. La portion recommandée de ce produit est ≤1,5 g/jour.
Conformément à la loi sur la sécurité alimentaire de la République populaire de Chine et aux mesures administratives relatives à l'examen de la sécurité des nouveaux ingrédients alimentaires, la Commission nationale de la santé et du bien-être a chargé l'organisme d'examen d'organiser des experts pour examiner et approuver les documents d'évaluation de la sécurité du pollen de seigle conformément aux procédures légales.
La production et l'utilisation de nouveaux ingrédients alimentaires doivent être conformes au contenu de l'annonce et aux exigences des réglementations relatives à la sécurité alimentaire. Compte tenu de l'insuffisance des informations sur la sécurité du pollen de seigle chez les nourrissons et les jeunes enfants, les femmes enceintes et les femmes allaitantes, il convient, en vertu du principe de prévention des risques, de ne pas consommer les produits destinés aux groupes susmentionnés et de ne pas consommer les produits destinés aux personnes allergiques au pollen ; l'étiquetage et les instructions doivent porter la mention "inapproprié pour la foule". Les indicateurs de sécurité alimentaire des matières premières doivent être conformes à l'annonce.
4. Amande de mandarine
Annonce d'approbation : Annonce de la Commission nationale de la santé sur 8 types de "trois nouveaux aliments", dont l'amande de Codonopsis pilosula (n° 5, 2023)
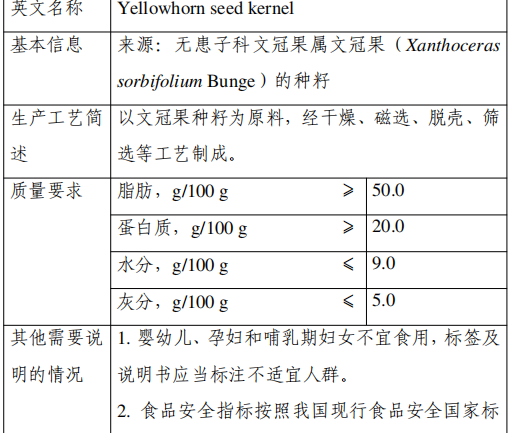
L'amande est obtenue à partir des graines de Xanthoceras?sorbifolium Bunge du genre Xanthoceras, de la famille des Sapindaceae, par séchage, séparation magnétique, décorticage, criblage et autres procédés.
Les principaux nutriments de l'amande de Xanthoceras sont les graisses, les protéines, les hydrates de carbone, les fibres alimentaires, les vitamines, etc. et contiennent une petite quantité de saponine, de stérols et d'autres substances.
La mandarine a été plantée dans le nord-est, le nord-ouest et le nord de la Chine. Elle est consommée depuis longtemps en Mongolie intérieure, au Gansu, au Shaanxi, au Shandong et dans d'autres régions.
Conformément à la "loi sur la sécurité alimentaire de la République populaire de Chine" et à l'"approche de gestion de l'évaluation de la sécurité des nouveaux ingrédients alimentaires", la Commission nationale de la santé et de l'hygiène a chargé l'organe d'évaluation, conformément aux procédures légales, d'organiser l'évaluation de la sécurité du grain d'avena sativa par des experts et de procéder à l'examen du matériel.
La production et l'utilisation de nouveaux ingrédients alimentaires doivent être conformes au contenu de l'annonce et aux exigences des réglementations relatives à la sécurité alimentaire. Compte tenu du manque d'informations sur la sécurité des graines d'Avena sativa chez les nourrissons, les jeunes enfants, les femmes enceintes et les femmes allaitantes, il convient, en vertu du principe de prévention des risques, de ne pas consommer les groupes de personnes susmentionnés et d'indiquer sur les étiquettes et les instructions qu'il s'agit de groupes inappropriés.
Les indicateurs de sécurité alimentaire de cette matière première sont conformes aux normes nationales chinoises en vigueur en matière de sécurité alimentaire pour les fruits à coque et les graines.
5. Feuille de mandarine
Annonce d'approbation : Annonce de la Commission nationale de la santé sur 8 "Trois nouveaux aliments", dont l'amande d'Avena sativa (n° 5, 2023)
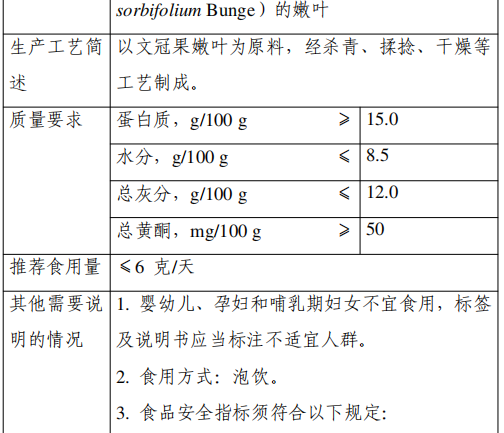
Les feuilles de Xanthoceras sorbifolium Bunge sont fabriquées à partir des jeunes feuilles de Xanthoceras sorbifolium Bunge, de la famille des Sapindaceae, par le biais d'un processus de verdissement, de malaxage, de séchage et d'autres procédés.
Les principaux nutriments contenus dans les feuilles de Xanthoceras sont les hydrates de carbone, les protéines, les graisses, etc., et contiennent une petite quantité de polyphénols de thé, de polysaccharides, de saponines, de flavonoïdes et d'autres substances.
Le Wenwen est planté dans le nord-est, le nord-ouest et le nord de la Chine, et les feuilles du Wenwen sont consommées depuis longtemps dans le Hebei, le Shanxi, la Mongolie intérieure, le Shandong et d'autres régions de Chine. Ce produit déclaré est consommé sous forme d'infusion, et la portion recommandée est de ≤6g/jour.
Conformément à la "loi sur la sécurité alimentaire de la République populaire de Chine" et aux "mesures administratives pour l'examen de la sécurité des nouveaux ingrédients alimentaires", la Commission nationale de la santé et de l'hygiène a chargé l'organisme d'examen, conformément aux procédures légales, d'organiser l'évaluation de la sécurité de la feuille d'avena sativa et de procéder à son examen.
La production et l'utilisation de nouveaux ingrédients alimentaires doivent être conformes au contenu de l'annonce et aux exigences des réglementations relatives à la sécurité alimentaire. Compte tenu du manque d'informations sur la sécurité de l'avena sativa chez les nourrissons et les jeunes enfants, les femmes enceintes et les femmes allaitantes, le principe de prévention des risques veut que les groupes susmentionnés ne soient pas consommés et que l'étiquetage et les instructions soient marqués comme étant inadaptés à la population.
L'indice de sécurité alimentaire de cette matière première est mis en œuvre conformément à l'annonce. Lorsque les normes nationales de sécurité alimentaire pour les succédanés de thé seront publiées, elles seront appliquées conformément aux normes pour les succédanés de thé.
6. Gomme de pêche
Avis d'approbation : Interprétation de l'annonce relative à la pectine de pêche et à 15 autres types de trois nouveaux aliments (n° 8 de 2023)
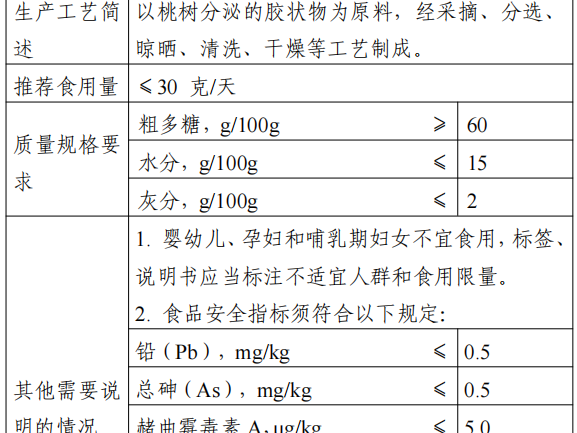
La gomme de pêche est basée sur la sécrétion de la matière gélatineuse des pruniers de Rosaceae (Prunuspersica (L.) Batsch) comme matière première, après la cueillette, le triage, le séchage, le lavage, le séchage et d'autres processus.
Les principaux nutriments sont les fibres alimentaires, les polysaccharides, l'eau, les protéines et les vitamines. En Chine, dans les régions de Hubei, Jiangsu et Zhejiang et dans d'autres régions, la gomme de pêche est consommée depuis longtemps, principalement sous forme de soupe, de bouillie, de potage, de dessert, etc. La portion recommandée de ce produit est de ≤30g/jour.
Conformément à la "loi sur la sécurité alimentaire de la République populaire de Chine" et à l'"approche de gestion de l'évaluation de la sécurité des nouveaux ingrédients alimentaires", la Commission nationale de la santé et de la santé a chargé l'organisme d'évaluation, conformément aux procédures légales, d'organiser des experts pour examiner l'évaluation de la sécurité des matières premières de la gomme de pêche et d'en passer par là.
La production et l'utilisation de nouveaux ingrédients alimentaires doivent être conformes au contenu de l'annonce et aux exigences des réglementations relatives à la sécurité alimentaire. Compte tenu du manque d'informations sur la sécurité de la pectine de pêche chez les nourrissons et les jeunes enfants, les femmes enceintes et les femmes allaitantes, en vertu du principe de prévention des risques, les groupes susmentionnés ne doivent pas être consommés, l'étiquetage et les instructions doivent porter la mention "inadapté à la population" et "limites de consommation". Les indicateurs de sécurité alimentaire de cette matière première sont conformes aux dispositions de l'annonce.
7.Huile Haricot de sauge
Annonce d'approbation : Interprétation de l'"Annonce concernant la gomme de pêche et 15 autres "trois nouveaux aliments"" (n° 8 de 2023)
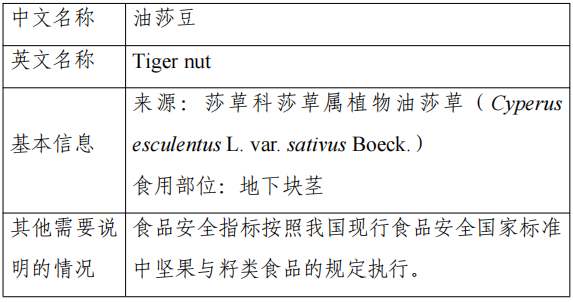
La plante de base de ce produit est Cyperusesculentus L. var. sativusBoeck. La plante de base de ce produit est Cyperusculentus L. var. sativusBoeck. La plante de base de ce produit est Cyperusculentus L. var. sativusBoeck. La plante de base de ce produit est Cyperusculentus L. var. sativusBoeck. La plante de base de ce produit est Cyperusculentus L. var. sativusBoeck.
Déclaration du produit : les graines oléagineuses sont des tubercules souterrains dont les principaux éléments nutritifs sont les glucides, les lipides, les fibres alimentaires, l'eau, les vitamines, etc. L'Europe considérera le soja oléagineux comme une denrée alimentaire courante ; le Canada considérera le lait de soja oléagineux comme une denrée alimentaire dont la sécurité alimentaire est reconnue depuis longtemps.
Conformément à la "loi sur la sécurité alimentaire de la République populaire de Chine" et aux "mesures de gestion pour l'examen de la sécurité des nouveaux ingrédients alimentaires", la Commission nationale de la santé et de l'hygiène a chargé l'organisme d'examen, conformément aux procédures légales, d'organiser l'examen et l'adoption d'experts sur l'évaluation de la sécurité des haricots verts.
La production et l'utilisation de nouveaux ingrédients alimentaires doivent être conformes au contenu de l'annonce et aux exigences des réglementations relatives à la sécurité alimentaire. Les indicateurs de sécurité alimentaire de cette matière première sont conformes aux normes nationales chinoises en vigueur en matière de sécurité alimentaire pour les fruits à coque et les graines.
8. Membrane intestinale brillante de la sous-espèce Streptomyces lactis
Annonce d'approbation : Interprétation de l'annonce "sur la gomme de pêche et autres 15 sortes de" trois nouveaux aliments (n° 8 de 2023)
La sous-espèce Streptomyces intestinalis Lactobacillus se trouve principalement dans les produits laitiers naturellement fermentés, le fromage, le kimchi, etc. La souche utilisée dans ce produit est dérivée de Lactobacillus casei. La souche utilisée dans ce produit a été isolée à partir de produits laitiers et figure dans la liste des agents biologiques recommandés sur la liste des qualifications (QPS) de l'Autorité européenne de sécurité des aliments (EFSA), dans le Bulletin de la Fédération internationale de laiterie (BulletininoftheIDF514/2022), dans le "Catalogue of Microbial Species Demonstrated to be Safe in Fermented Foods", et dans la "List of Food Products" danoise (No. 8, 2023). "La liste des espèces microbiennes utilisées dans les denrées alimentaires a été publiée par la Commission européenne et le Danemark dans son "Record of the List of Microbial Species for Use in Food".
Cet agrément est inclus dans la "Liste des souches utilisables dans les denrées alimentaires", et le champ d'application comprend la fermentation et la transformation du lait et des produits laitiers, des produits à base de fruits et de légumes, et des produits céréaliers, à l'exclusion des aliments pour bébés.
Conformément à la "loi sur la sécurité alimentaire de la République populaire de Chine" et aux "mesures de gestion pour l'examen de la sécurité des nouveaux ingrédients alimentaires", la Commission nationale de la santé et de l'hygiène a mandaté l'organe d'examen conformément aux procédures statutaires, et a organisé des experts sur l'évaluation de la sécurité des membranes intestinales Ming Streptomyces lactis sous-espèces du matériel pour examen et adoption.
La production et l'utilisation de nouveaux ingrédients alimentaires doivent être conformes au contenu de l'annonce et aux exigences des réglementations relatives à la sécurité alimentaire. Lorsque les normes nationales de sécurité alimentaire pour les préparations de souches destinées à la transformation alimentaire sont publiées, elles doivent être mises en œuvre conformément aux normes pour les préparations de souches destinées à la transformation alimentaire.
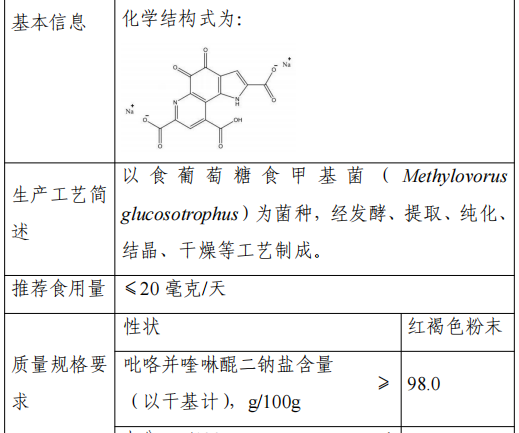
9. sel disodique de pyrroloquinoline quinone
Annonce d'approbation : Interprétation de l'annonce relative à la gomme de pêche et aux 15 autres types de "trois nouveaux aliments" (n° 8 de 2023)
Ce produit est fabriqué à partir de Methylovorusglucosotrophus comme souche de fermentation, par fermentation, extraction, purification, cristallisation, séchage et autres processus.
Le sel disodique de pyrroloquinoline quinone se trouve naturellement dans de nombreux aliments tels que le lait, les œufs, les épinards, etc. Nous avons approuvé la méthode de synthèse du sel disodique de pyrroloquinoline quinone en tant que nouvel ingrédient alimentaire en 2022.
Le sel disodique de pyrroloquinoline quinone est réglementé comme "généralement reconnu comme sûr" (GRAS) aux États-Unis et peut être utilisé comme ingrédient dans les boissons énergétiques, les boissons pour sportifs, les boissons électrolytiques et d'autres produits alimentaires ; il est utilisé dans l'Union européenne et au Canada comme complément alimentaire ou aliment de santé naturel.
La portion recommandée de ce produit est ≤20 mg/jour (c'est-à-dire que la portion recommandée de sel disodique de pyrroloquinoline quinone avec une teneur en 98% est ≤20 mg/jour, et ceux qui dépassent cette teneur sont convertis en fonction de la teneur réelle).
Conformément aux dispositions de la loi sur la sécurité alimentaire et des mesures administratives relatives à l'examen de la sécurité des nouveaux ingrédients alimentaires, la Commission nationale de la santé et de l'hygiène a chargé l'organe d'examen d'organiser des experts pour examiner et approuver les documents d'évaluation de la sécurité du sel disodique de pyrroloquinoléine quinone, conformément aux procédures légales.
La production et l'utilisation de nouveaux ingrédients alimentaires doivent être conformes au contenu de l'annonce et aux exigences des réglementations relatives à la sécurité alimentaire. Compte tenu de l'insuffisance des informations sur la sécurité du sel disodique de pyrroloquinoline quinone dans la population des nourrissons et des jeunes enfants, des femmes enceintes et des femmes allaitantes, en vertu du principe de prévention des risques, il ne convient pas à la consommation par les groupes susmentionnés, et l'étiquette et les instructions doivent mentionner les groupes inappropriés et la limite de consommation. Les indices de sécurité alimentaire de cette matière première sont conformes à l'annonce.
10.Paraguay Holly Leaf (Matei Tea Leaf)
Annonce d'approbation : Interprétation de l'annonce relative aux feuilles de houx du Paraguay (feuilles de thé Matei) et à neuf autres "trois nouveaux aliments" (n° 10 de 2023)
Les feuilles de houx du Paraguay (feuilles de thé Matei) sont fabriquées à partir des feuilles de houx du Paraguay (Ilex?paraguariensis?A.St.-Hil.), une plante du genre Holly, de la famille des houx, par le biais d'un processus de cueillette, de torréfaction, de hachage et de séchage. Les principaux nutriments sont les hydrates de carbone, les fibres brutes, les protéines, les graisses, les vitamines, les minéraux et les acides aminés, ainsi qu'une petite quantité de polyphénols, de flavonoïdes, de saponines et d'autres substances.
Les feuilles de houx du Paraguay (feuilles de maté) sont réglementées comme "généralement reconnues comme sûres" (GRAS) aux États-Unis, approuvées comme nouvel ingrédient alimentaire dans l'Union européenne, approuvées comme produit de santé naturel au Canada et approuvées pour la production de thé au Brésil.
Conformément aux dispositions de la loi sur la sécurité alimentaire de la République populaire de Chine et aux mesures administratives relatives à l'examen de la sécurité des nouveaux ingrédients alimentaires, la Commission nationale de la santé et du bien-être a chargé l'organe d'examen d'organiser des experts pour examiner et approuver les documents d'évaluation de la sécurité des feuilles de houx du Paraguay (feuilles de thé maté) conformément aux procédures légales.
La production et l'utilisation de nouveaux ingrédients alimentaires doivent être conformes au contenu de l'annonce et aux exigences des réglementations relatives à la sécurité alimentaire. Compte tenu de l'insuffisance des informations sur la sécurité de la consommation de feuilles de gaulthérie du Paraguay (feuilles de thé Matei) chez les nourrissons et les jeunes enfants, les femmes enceintes et les femmes allaitantes, le principe de prévention des risques veut que les groupes susmentionnés ne soient pas consommés et que les étiquettes et les instructions mentionnent les groupes inappropriés.
L'indice de sécurité alimentaire de cette matière première est mis en œuvre conformément à l'annonce. Lorsque les normes nationales de sécurité alimentaire pour les succédanés de thé seront publiées, elles seront appliquées conformément aux normes pour les succédanés de thé.
11. Protéines de levure
Annonce d'approbation : Interprétation de l'annonce relative aux 9 "trois nouveaux aliments", dont la feuille de houx du Paraguay (feuille de thé Matei) (n° 10, 2023)
La protéine de levure est fabriquée à partir de la levure de bière (Saccharomyces?Cerevisiae) en tant que souche, qui est collectée après culture, fermentation et centrifugation pour obtenir la matière première de la bactérie, et est fabriquée par élimination de l'acide nucléique, centrifugation, enzymolyse, extraction, purification, isolation, stérilisation et séchage, etc. Le principal élément nutritif est la protéine (protéine).
Les principaux nutriments sont les protéines (≥70,0g/100g), les matières grasses, les fibres alimentaires et l'eau. À l'heure actuelle, les États-Unis ont approuvé les protéines de levure de bière en tant que complément nutritionnel ajouté aux aliments, et l'Union européenne a approuvé les protéines de levure de bière en tant que nouvel ingrédient alimentaire, sans limiter la quantité consommée dans les deux cas.
Conformément à la "loi sur la sécurité alimentaire de la République populaire de Chine" et aux "mesures de gestion pour l'examen de la sécurité des nouveaux ingrédients alimentaires", la Commission nationale de la santé et de l'hygiène a chargé l'organisme d'examen, conformément aux procédures légales, d'organiser l'examen et l'adoption par des experts de l'évaluation de la sécurité des protéines de levure.
La production et l'utilisation de nouveaux ingrédients alimentaires doivent être conformes au contenu de l'annonce et aux exigences des réglementations relatives à la sécurité alimentaire. Compte tenu du manque d'informations sur la sécurité des protéines de levure chez les nourrissons et les jeunes enfants, les femmes enceintes et les femmes allaitantes, le principe de prévention des risques veut que les groupes susmentionnés ne soient pas consommés et que l'étiquetage et les instructions soient marqués comme étant inappropriés pour la population. Les indicateurs de sécurité alimentaire de cette matière première sont conformes à l'annonce.
11. catéchine
Annonce d'approbation : Interprétation de l'annonce relative aux "trois nouveaux aliments", y compris la feuille de thé du Paraguay (feuille de thé Maté) (n° 10 de 2023)
La catéchine est fabriquée à partir du thé comme matière première, par extraction d'alcool, concentration, séparation, extraction, digestion enzymatique, concentration, séchage et autres processus.
Les principaux composants sont les catéchines, notamment l'épicatéchine (EC), l'épigallocatéchine (EGC), le gallate d'épicatéchine hydraté (ECG-H2O), le gallate d'épigallocatéchine hydraté (EGCG-H2O), le gallate de gallocatéchine (GCG), la catéchine (dl-C), dont la teneur totale en catéchine (sur une base sèche) est ≥90 ?g/100g, dont la teneur en EGCG est ≥90?g/100g, dont la teneur en EGCG est ≥90?g/100g. 100g, dont la teneur en EGCG est ≥ 50?g/100g.
L'ancien ministère de la santé a approuvé le gallate d'épigallocatéchine (EGCG) en tant que nouvel aliment-ressource dans l'annonce n° 17 de 2010, avec une consommation quotidienne recommandée de ≤300 mg/jour (en termes d'EGCG).
Les catéchines du thé vert ont été approuvées par le Japon en tant qu'ingrédients fonctionnels pour des aliments de santé spécifiques. L'apport journalier recommandé pour ce produit est ≤300 mg/jour (en termes de catéchines totales) (c'est-à-dire que l'apport journalier recommandé pour les matières premières ayant une teneur en catéchines totales de 100?g/100g est ≤300 mg/jour, et la teneur de 90-100?g/100g est convertie en fonction de la teneur réelle).
Conformément à la "loi sur la sécurité alimentaire de la République populaire de Chine" et aux "mesures administratives pour l'examen de la sécurité des nouveaux ingrédients alimentaires", la Commission nationale de la santé et de l'hygiène a chargé l'organisme d'examen de procéder à l'examen et à l'adoption du matériel d'évaluation de la sécurité des catéchines, conformément aux procédures statutaires, à l'organisation d'experts en la matière. La production et l'utilisation de nouveaux ingrédients alimentaires doivent être conformes au contenu de l'annonce et aux exigences des réglementations relatives à la sécurité alimentaire.
Compte tenu du manque d'informations sur la sécurité des catéchines chez les nourrissons et les jeunes enfants, les femmes enceintes et les femmes allaitantes dans la population, en vertu du principe de prévention des risques, les groupes susmentionnés ne devraient pas être consommés, l'étiquetage et les instructions devraient indiquer qu'ils ne conviennent pas à la population et qu'ils ne doivent pas dépasser les limites de consommation. Les indicateurs de sécurité alimentaire de cette matière première sont conformes aux dispositions de l'annonce.