Exploration du mécanisme de Morinda officinalis contre l'athérosclérose sur la base de la pharmacologie des réseaux et de la vérification expérimentale
L'athérosclérose (AS) est une maladie cardiovasculaire chronique courante caractérisée par la formation d'une plaque d'athérome ou d'une plaque fibreuse dans l'intima des grandes et moyennes artères. L'infiltration de lipides dans l'intima artérielle est devenue la principale pathogénie de l'athérosclérose. Les macrophages rassemblés dans l'intima et la média engloutissent une grande quantité de lipoprotéines de faible densité oxydées (ox LDL) par l'intermédiaire des récepteurs scavenger sur la membrane cellulaire pour former des cellules spumeuses, qui poussent les cellules à libérer un grand nombre de facteurs pro-inflammatoires et de métalloprotéinases matricielles dans l'espace intercellulaire, favorisant l'accumulation de la plaque dans la paroi artérielle, puis se transformant en plaque instable, et enfin évoluant vers l'infarctus du myocarde. Cependant, retarder efficacement la progression de la SA a toujours été l'un des défis qui préoccupent la communauté universitaire. Ces dernières années, il a été prouvé que le Morinda officinalis, un nouveau produit médicinal et comestible populaire, avait de bons effets sur la régulation des lipides sanguins et l'amélioration de l'athérosclérose.
Morinda citrifolia, également connu sous le nom de Noni, est une plante du genre Euphorbia de la famille des Rubiacées. Il a des effets pharmacologiques tels qu'anti-inflammatoires, antioxydants et hypolipidémiants. Selon la théorie de la médecine traditionnelle chinoise, le Morinda officinalis a un goût aigre et doux, une propriété médicinale équilibrée et a pour effet de nourrir l'essence des reins, d'équilibrer le yin et le yang et de retarder le vieillissement. Il peut prévenir efficacement les maladies cardiovasculaires et cérébrovasculaires. Toutefois, le mécanisme spécifique du Hai Ba Ji dans le traitement de la SA n'est pas encore clair. Étant donné la composition chimique complexe de Morinda officinalis, qui est principalement composée d'anthraquinones, de flavonoïdes, de phénylpropanoïdes, d'acides phénoliques et d'autres composants, conformément aux caractéristiques multi-composants et multi-cibles de la médecine traditionnelle chinoise, la pharmacologie des réseaux peut être utilisée pour élucider clairement le mécanisme moléculaire des effets pharmacologiques de Morinda officinalis. Ces dernières années, la pharmacologie des réseaux est devenue une discipline émergente qui intègre l'informatique, la bioinformatique et l'exploration de données. Elle construit un réseau "médicament ingrédient actif maladie cible maladie" et explique ses fonctions biologiques, ce qui permet aux gens de mieux comprendre les mécanismes de la pharmacothérapie des maladies. Cette étude est basée sur les divers ingrédients actifs et les riches cibles de Morinda officinalis, et a l'intention d'utiliser des méthodes de pharmacologie de réseau pour prédire et analyser les cibles, les processus biologiques et les voies de signalisation de Morinda officinalis dans le traitement de la maladie d'Alzheimer. Parallèlement, des expériences in vitro seront utilisées à des fins de vérification, afin de fournir une base pharmacologique pour le développement de médicaments et le traitement de la SA.
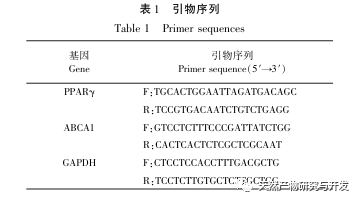 athérosclérose
athérosclérose



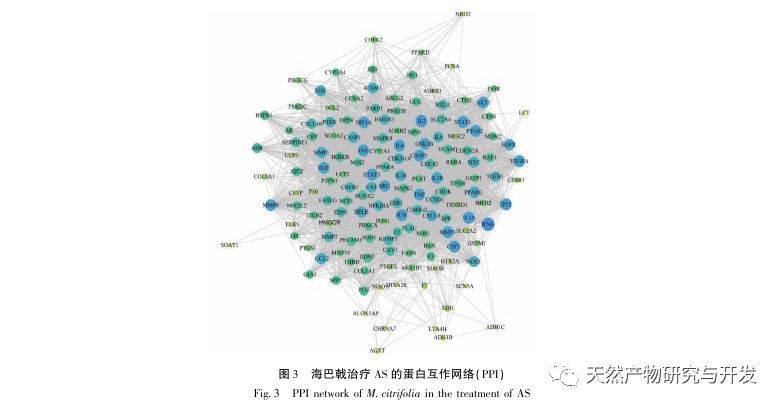
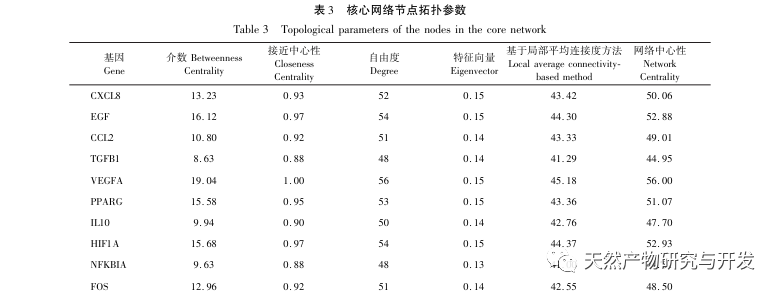
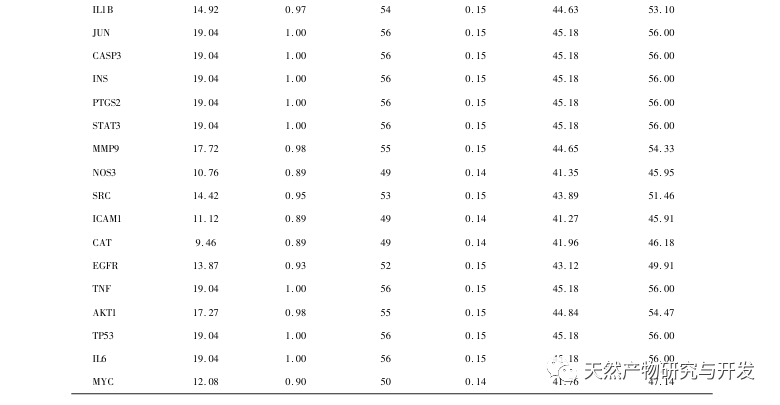
La SA est une maladie cardiovasculaire courante, et sa progression rapide peut directement conduire à des événements cardiovasculaires malins chez les patients, tels que l'infarctus du myocarde. La médecine moderne estime que la théorie des lipides reste le principal mécanisme d'apparition de la SA. Les statines, les inhibiteurs de PCSK9 et d'autres médicaments hypolipidémiants sont couramment utilisés dans la pratique clinique pour ralentir la progression de l'athérosclérose. Toutefois, en raison des effets indésirables tels que les courbatures et les lésions de la fonction hépatique qui surviennent encore aux doses thérapeutiques, de nombreux patients ne peuvent pas tolérer ces médicaments. C'est pourquoi la recherche de nouveaux médicaments plus sûrs et moins toxiques pour traiter la SA revêt une importance positive. En tant que produit médicinal et comestible émergent, Morinda officinalis possède un large éventail de principes actifs et d'effets pharmacologiques, ce qui correspond aux caractéristiques typiques de la médecine traditionnelle chinoise, qui traite les maladies par des cibles et des voies multiples. Cette étude a utilisé la pharmacologie de réseau pour prédire les ingrédients et les cibles efficaces du Morinda officinalis dans le traitement de la SA, et a construit un modèle de macrophage dérivé de la THP-1 pour vérifier que le Morinda officinalis favorise l'efflux de cholestérol intracellulaire par la voie de signalisation PPAR γ.
L'examen de diverses bases de données a permis de constater que 59 composés, dont des flavonoïdes, des phénylpropanoïdes et des acides phénoliques, jouent principalement un rôle thérapeutique dans le traitement de la SA. Ces dernières années, de nombreux rapports de recherche ont montré que les flavonoïdes jouent un rôle clé dans le traitement de la SA et sont les principaux sites actifs de la médecine végétale. Sahib et al. ont constaté que les teneurs en catéchines, quercétine et kaempférol dans le fruit de Morinda officinalis étaient respectivement de 53,68 mg/g, 7,4 mg/g et 6,4 mg/g, ce qui les classe parmi les trois premiers flavonoïdes actifs connus. Ces trois composants jouent un rôle important dans la régulation des anomalies des lipides sanguins et le retardement de l'athérosclérose. Les recherches ont montré que le principal composant des granules de Yixin Tongmai, les catéchines, peut activer directement la voie PPAR γ et améliorer la SA grâce à l'amarrage moléculaire et à des expériences in vitro et in vivo. La quercétine est largement présente dans diverses plantes, avec une proportion significative dans le Morinda officinalis. Jia et al. et Li et al. ont rapporté que la quercétine peut réduire de manière significative le contenu de la plaque dans l'aorte thoracique du modèle de SA de la souris Apoe -/- induit par un régime riche en graisses. Le mécanisme est lié à l'augmentation de l'expression du transporteur de cassette de liaison à l'ATP A1 (ABCA1). La recherche a confirmé que le kaempférol a une forte activité anti-inflammatoire et peut retarder la progression de l'athérosclérose en activant la voie PI3K/AKT/Nrf2.
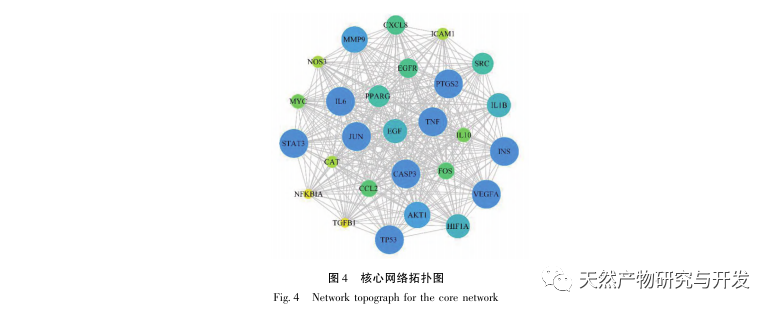
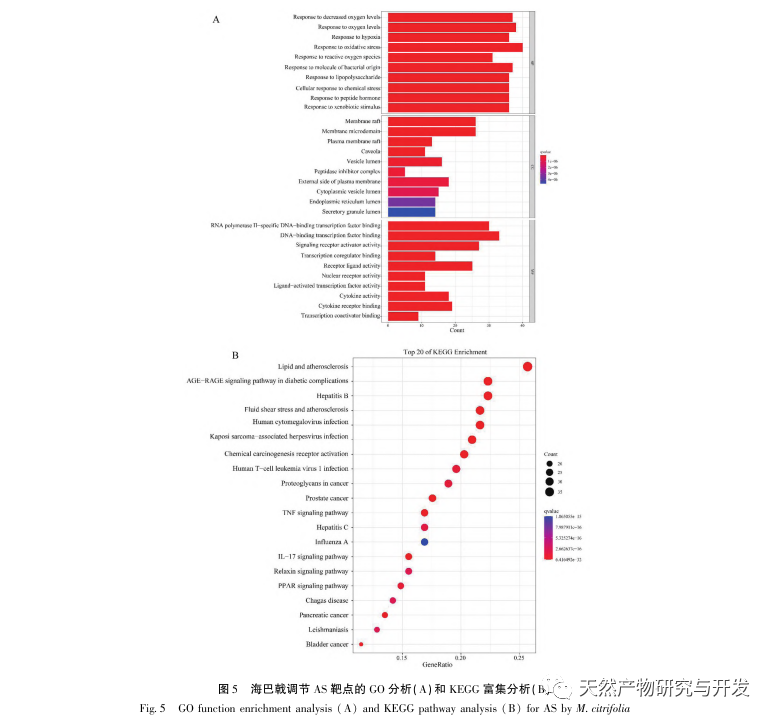
Par la suite, l'analyse d'enrichissement GO a révélé que Morinda officinalis régule principalement des fonctions biologiques telles que les récepteurs membranaires et les récepteurs nucléaires dans les cellules ; l'analyse d'enrichissement des voies de signalisation KEGG a révélé que le traitement de l'AS par Morinda officinalis est associé aux voies de signalisation liées au métabolisme des lipides, la voie de signalisation PPAR étant l'une d'entre elles. La recherche a montré que les voies de signalisation liées au métabolisme des lipides, en particulier la voie de signalisation PPAR, sont étroitement liées aux transporteurs de lipides sur la membrane cellulaire et aux récepteurs dans le noyau. Comme nous le savons tous, les PPAR sont des récepteurs nucléaires classiques situés dans le noyau. Après avoir reçu le signal du second messager, les PPAR augmentent l'expression des transporteurs de cholestérol sur la membrane cellulaire en activant les facteurs de transcription en aval, réduisant ainsi l'accumulation de cholestérol dans les cellules et empêchant les macrophages de se transformer en cellules spumeuses. La voie de signalisation des PPAR joue donc un rôle important dans la réduction de la formation de cellules spumeuses dans les noyaux lipidiques et dans le retardement de la SA. En outre, le gène PPARG est également un nœud important dans le réseau central du réseau cible des composants dans cette étude.
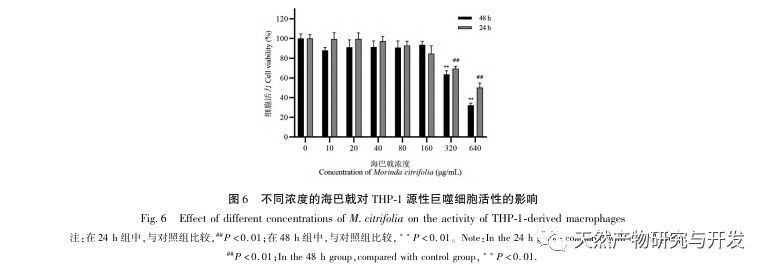
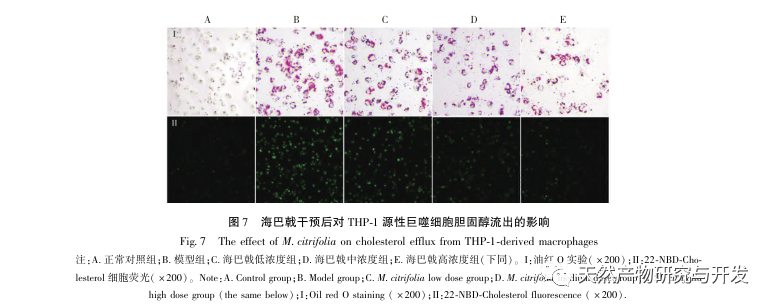
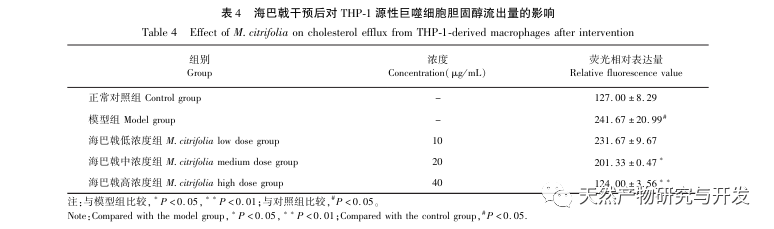
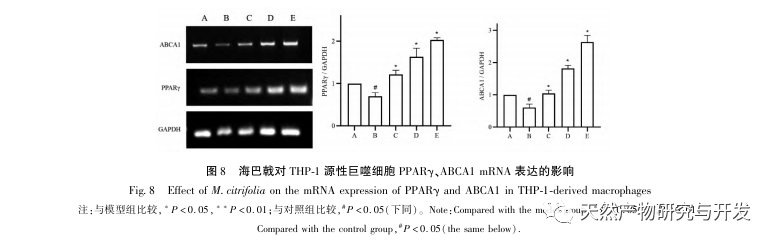
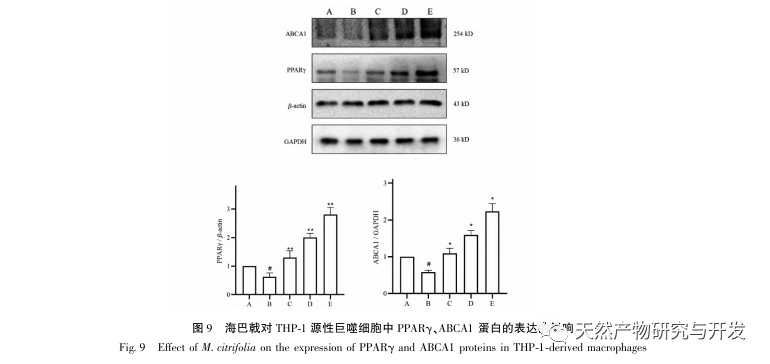
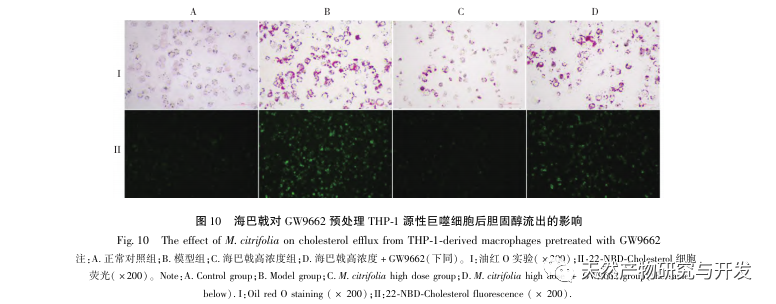
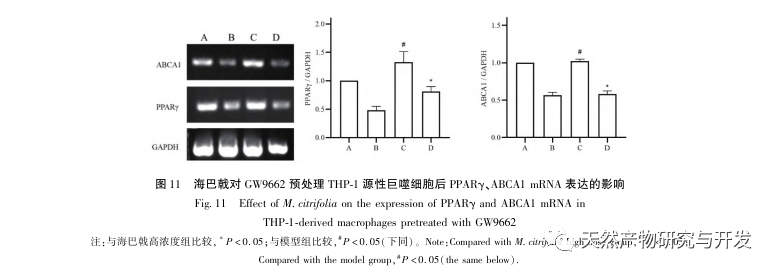
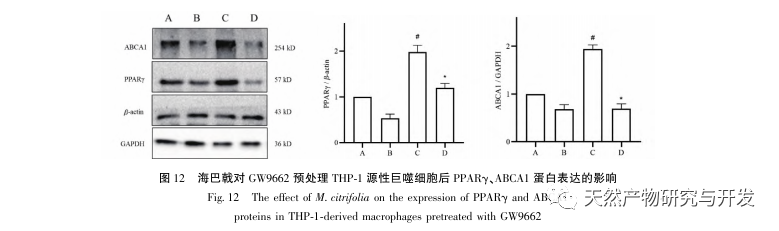
Sur la base de l'analyse pharmacologique en réseau susmentionnée, cette étude a construit des macrophages dérivés de THP-1 pour simuler les cellules spumeuses dans les plaques d'athérosclérose in vitro. Après l'intervention de Morinda officinalis sur les macrophages dérivés de la THP-1, il a été constaté que la teneur en cholestérol intracellulaire était significativement réduite et que l'expression de PPAR γ dans les cellules était significativement régulée à la hausse. Inada et al. et Nerurkar et al. ont respectivement confirmé l'effet hypolipidémiant de Morinda officinalis par des expériences animales. Une étude clinique a montré que le Morinda officinalis peut réduire de manière significative les taux sériques de LDL et augmenter les taux de lipoprotéines de haute densité (HDL) chez les fumeurs invétérés. Récemment, Chong et al. ont confirmé que Morinda officinalis pouvait réduire de manière significative les plaques lipidiques dans l'aorte d'un modèle de rat AS induit par un régime à base d'huile de palme oxydée thermiquement, mais le mécanisme spécifique n'a pas été élucidé. Auparavant, Lee et al. ont extrait la poudre séchée du fruit de Morinda officinalis avec du méthanol 70% et ont découvert qu'elle pouvait exciter les récepteurs PPAR γ dans les cellules musculaires squelettiques C2C12. Ce rapport expérimental est cohérent avec nos résultats. Cette étude a montré pour la première fois que Morinda officinalis peut favoriser l'efflux de cholestérol à partir des macrophages dérivés de THP-1 et, en combinaison avec la pharmacologie des réseaux, a prédit son effet de transport inverse du cholestérol (TAC) en activant la voie de signalisation PPAR γ. L'un des mécanismes importants par lesquels le RCT régule les anomalies lipidiques et améliore la SA in vivo est le transfert du cholestérol des cellules à travers les récepteurs scavenger sur la membrane cellulaire, qui se lie ensuite à l'apolipoprotéine A, à l'apoE et à d'autres protéines dans le plasma et est transporté vers le foie pour y être métabolisé. Il est ensuite converti en acides biliaires et excrété par l'organisme, ce qui permet de remédier aux anomalies du métabolisme des lipides. L'ABCA1, important récepteur piégeur sur la membrane des macrophages, est finement régulé par le facteur de transcription nucléaire en amont PPAR γ et est responsable du transport du cholestérol intracellulaire vers l'espace extracellulaire par le biais du processus RCT. Dans cette étude, le niveau d'expression d'ABCA1 a été augmenté avec l'activation de PPAR γ. Lorsque l'inhibiteur de PPAR γ GW9662 a été utilisé, la tendance à l'augmentation de l'expression du récepteur ABCA1 dans les macrophages dérivés de THP-1 a été inhibée, et il n'y a pas eu de diminution significative de la teneur en cholestérol intracellulaire, ce qui indique qu'ABCA1 médié par PPAR γ est le principal transporteur du cholestérol intracellulaire. De même, la quercétine, la baicaline et la dihydromyricétine peuvent toutes promouvoir le RCT et exercer des effets anti-SA en activant la voie de signalisation PPAR γ/ABCA1. Par conséquent, Morinda officinalis peut favoriser l'efflux de cholestérol des macrophages dérivés de la THP-1 en activant la voie de signalisation PPAR γ.
En résumé, le Morinda officinalis a un goût aigre-doux et des propriétés médicinales équilibrées. Il peut nourrir l'essence des reins, équilibrer le yin et le yang et prévenir les maladies cardiovasculaires et cérébrovasculaires. Cette étude a utilisé la pharmacologie de réseau combinée à des expériences in vitro pour révéler le mécanisme du Morinda officinalis dans le traitement de la SA, et a démontré pour la première fois que le Morinda officinalis peut favoriser l'efflux de cholestérol des macrophages dérivés de la THP-1 et promouvoir la RCT en activant la voie de signalisation PPAR γ. Par conséquent, cette étude fournit un nouveau mécanisme pharmacologique pour la prévention et le traitement efficaces de la SA par Morinda officinalis. Toutefois, cette étude présente encore certaines limites : (1) Comme la base de données TCMSP n'incluait pas la plante médicinale Morinda officinalis, les bases de données CAMUP et SwissADME ont été utilisées pour aider à sélectionner ses principes actifs. Bien qu'il y ait eu des études utilisant plusieurs bases de données pour sélectionner conjointement les ingrédients de la médecine traditionnelle chinoise, les critères de sélection des ingrédients actifs dans les différentes bases de données sont différents, de sorte qu'une vérification supplémentaire est nécessaire en termes de fiabilité de la sélection ; (2) Cette étude a passé au crible 5 bases de données liées à des maladies, et les résultats ont montré qu'il y avait des différences significatives dans le nombre de cibles de la SA dans chaque base de données, ce qui peut être lié à des différences dans les types de maladies incluses dans chaque base de données ; (3) Sur la base des résultats des expériences in vitro, notre groupe de recherche continuera à construire un modèle animal de la SA pour fournir une base expérimentale plus complète pour la promotion de l'ECR et le retard de la SA par Morinda officinalis du point de vue des expériences in vivo.
