Erforschung des Wirkmechanismus von Guanggancao Ding bei der Behandlung von kastrationsresistentem Prostatakrebs auf der Grundlage von Netzwerk-Pharmakologie und experimenteller Überprüfung
Prostatakrebs (PCa) ist der häufigste bösartige Tumor im Fortpflanzungssystem von älteren Männern. Viele frühe Androgenentzugstherapien sind wirksam, aber die meisten entwickeln sich schließlich von einem hormonsensitiven Prostatakrebs zu einem kastrationsresistenten Prostatakrebs (CRPC). CRPC ist ein hochgradig tödlicher und invasiver Prostatakrebs. Bei mehr als 84% der CRPC-Patienten bilden sich Metastasen, und die mittlere Überlebenszeit beträgt nur 20 Monate. Obwohl in den letzten Jahren neue Chemotherapeutika und endokrine Medikamente auf den Markt gekommen sind, haben diese Chemotherapeutika viele Nebenwirkungen, und bei endokrinen Medikamenten gibt es Resistenzprobleme, die die Wirkdauer des Medikaments verkürzen. Daher ist die Suche nach neuen Medikamenten von großer Bedeutung, um den Prozess der Kastrationsresistenz zu verzögern und CRPC zu behandeln.
Glabridin ist eine Flavonoidverbindung, die aus Lakritze extrahiert wird und eine breite Palette biologischer Aktivitäten wie entzündungshemmende, antioxidative, tumorhemmende, neuroprotektive und osteoporosehemmende Eigenschaften aufweist. Es wird berichtet, dass Glycyrrhizin bei Brust-, Leber-, Magen- und Gebärmutterhalskrebs die Vermehrung von Tumorzellen hemmt und die Apoptose auslöst. Der molekulare Mechanismus von Glycyrrhizin bei CRPC ist jedoch noch nicht vollständig geklärt. Die Netzwerkpharmakologie ist eine Kombination aus Pharmakologie, Informatik und Informationsnetzwerken auf der Grundlage der Systembiologie und liefert neue Ideen für die Entdeckung und Auswahl von Arzneimitteln bei komplexen Krankheiten. Um den Wirkmechanismus von Guanggancao Ding auf CRPC weiter zu untersuchen, nutzten wir die Netzwerkpharmakologie, molekulares Docking und Zellexperimente, um den Wirkmechanismus zu erforschen und so Hinweise für die zukünftige Arzneimittelgrundlagenforschung und klinische Anwendungen zu liefern.
In den letzten Jahren wurden erhebliche Fortschritte bei der Behandlung von Prostatakrebs mit traditioneller chinesischer Medizin erzielt, insbesondere bei CRPC. Die Kombination von traditioneller chinesischer Medizin mit Chirurgie oder Chemotherapie bewirkt eine Verringerung der Tumorgröße, eine Senkung des PSA-Wertes, eine Verringerung des Wiederauftretens und eine Verlängerung der Überlebenszeit. Viele Forschungsberichte deuten darauf hin, dass die Wirkstoffe der Süßholzwurzel eine signifikante Anti-Tumor-Wirkung auf CRPC haben. Gioti et al. fanden heraus, dass Lakritzextrakt (GGE) allein oder in Kombination mit Doxorubicin die Proliferation von androgenunabhängigen Prostatakrebszellen (PC-3-Zellen) hemmt und die Expression von Autophagie-bezogenen Genen wie LC3A, ULK1 und AMBRA1 fördern kann. Zhang et al. fanden heraus, dass Isoliquiritigenin die Proliferation von Prostatakrebszellen (PC-3 und 22RV1) hemmen, Apoptose induzieren, den G2/M-Zellzyklus blockieren und das Wachstum von PC-3-Xenografts durch In-vivo-Tierversuche hemmen kann. Lakritze zeigt eine ausgezeichnete Anti-CRPC-Aktivität, und Glycyrrhizin in Lakritze ist eines der vielen Flavonoide, das viel Aufmerksamkeit auf sich gezogen hat und eine gute Anti-Tumor-Aktivität aufweist. Der Wirkmechanismus von CRPC ist es wert, weiter erforscht zu werden.
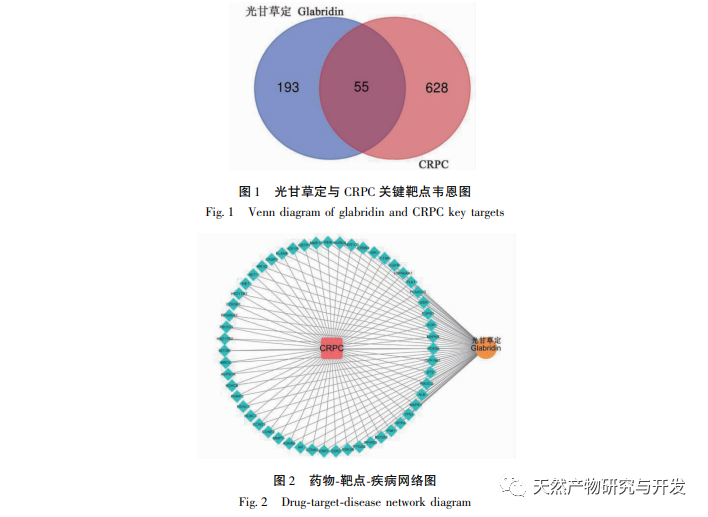
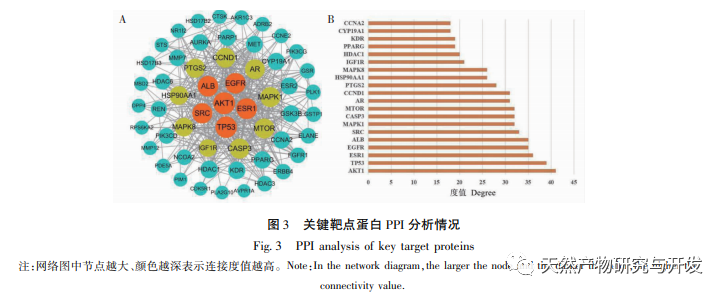
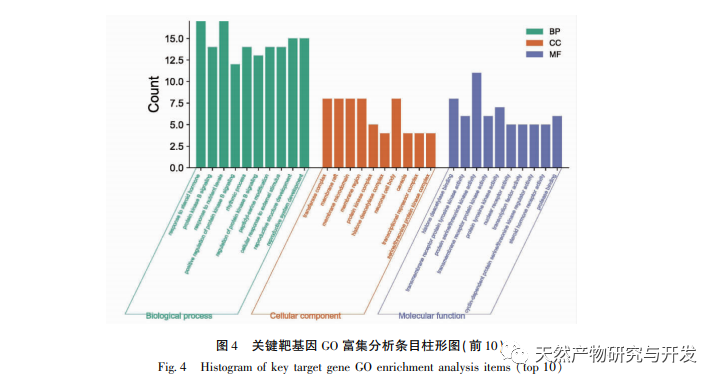
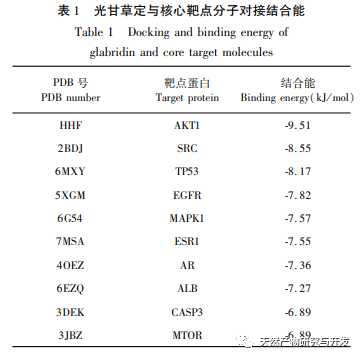
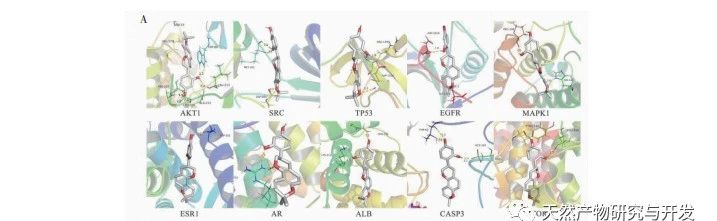
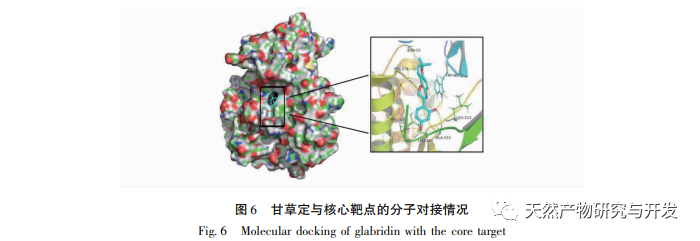
Im Vergleich zur traditionellen Pharmakologie bietet die Netzwerk-Pharmakologie eine neue Perspektive für die Entwicklung neuer Arzneimittel. Um den Wirkmechanismus von Glycyrrhizin bei CRPC besser zu verstehen, verwendeten wir Methoden der Netzwerkpharmakologie, um 683 Ziele von Glycyrrhizin in Datenbanken wie TCMIO, TCMSP und PharmMapper zu sammeln. Wir erhielten 55 Schlüsselziele von Glycyrrhizin für kastrationsresistenten Prostatakrebs mithilfe von Venn-Diagramm-Tools und identifizierten 10 Kernziele wie AKT1, TP53, ESR1, EGFR und ALB durch PPI-Proteininteraktionsnetzwerkanalyse. Die GO-Anreicherungsanalyse zeigte, dass Glycyrrhizin hauptsächlich den Zellstoffwechsel und die Apoptose reguliert, indem es die Proteinphosphorylierung, Oxidationsreaktionen und den Zellzyklus reguliert. Molekulares Docking zeigte außerdem, dass Glycyrrhizin eine gute Docking-Aktivität mit 10 Kernzielen hat. Es wird vorhergesagt, dass Glycyrrhizin durch die Regulierung der Expression dieser Kernzielproteine Anti-Tumoreffekte erzielen kann. Unter diesen Kernzielen hat das AKT1-Protein die höchste Andockaktivität. AKT1 ist einer der wichtigen regulatorischen Faktoren im PI3K/AKT-Signalweg, der an verschiedenen biologischen Prozessen von Tumoren beteiligt ist. Bei Prostatakrebs wurden auf der Grundlage von Genom- und Transkriptomprofilen genetische Variationen und Dysregulationen der Genexpression von Komponenten des PI3K/AKT-Signalwegs in bis zu 42% primärer Prostatakrebs- und 100% metastasierender Prostatakrebsproben nachgewiesen. In frühen Studien wurde vermutet, dass AKT-Subtypen (AKT1, AKT2) den Übergang vom androgensensitiven Stadium zum hormonrefraktären Stadium des Prostatakrebses fördern können. Auf der Grundlage der Grundlagenforschung zur Behandlung von CRPC-Patienten wurde in Studien berichtet, dass die Ausschaltung von AKT1/2 in kastrationsresistenten Prostatakrebs-Tiermodellen zu einer deutlichen Verringerung der In-vivo- und In-vitro-Metastasen führt. Die Hemmung der Expression von AKT1 kann die Überlebensprognose von CRPC-Patienten verbessern, und AKT1-Inhibitoren könnten eine mögliche Behandlung für CRPC-Patienten sein. Unsere Studie legt theoretisch nahe, dass Glycyrrhizin ein AKT1-Inhibitor sein könnte, aber ob Glycyrrhizin ein wirksamer AKT1-Inhibitor für CRPC-Patienten werden kann, muss in Zukunft noch weiter experimentell überprüft werden.
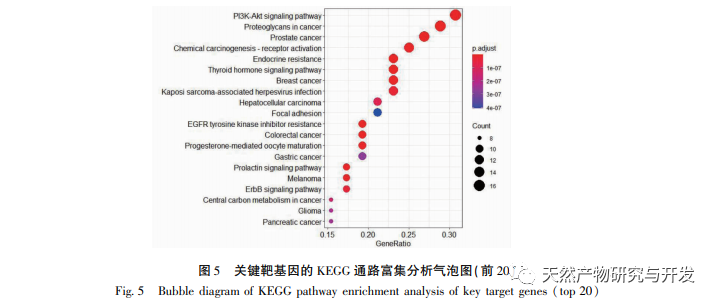
Die Ergebnisse der Anreicherung der KEGG-Signalwege zeigten, dass der PI3K/AKT-Signalweg und die Proteoglykane in 105 verwandte Signalwege involviert waren, darunter Krebs, Prostatakrebs, Chemokinrezeptor-Aktivierung, endokrine Resistenz und Resistenz gegen Rezeptor-Tyrosinkinase-Hemmer des epidermalen Wachstumsfaktors (P<0,01). Unter ihnen ist der Phosphatidyl-3-Kinase (PI3K)/Serin-Threonin-Proteinkinase (AKT)-Signalweg am stärksten betroffen. Der PI3K/AKT-Signalweg ist an der Regulierung von Zellstoffwechsel, Wachstum, Proliferation, Differenzierung und Proteinsynthese beteiligt. Mutationen im PI3K/AKT-Signalweg wurden in vielen menschlichen Tumoren nachgewiesen. Forschungsdaten zeigen, dass bei bis zu 70% bis 100% der Patienten mit fortgeschrittenem Prostatakrebs eine Dysregulierung des PI3K-Signalwegs vorliegt. Außerdem wurde festgestellt, dass der PI3K/AKT-Signalweg eine wichtige Rolle beim Fortschreiten von hormonsensitivem Prostatakrebs zu kastrationsresistentem Prostatakrebs spielt, und sein Wirkmechanismus kann mit der Regulierung des Androgenrezeptor (AR)-Signalwegs zusammenhängen, was als potenzieller Biomarker für CRPC dienen kann. Gegenwärtig sind Inhibitoren, die mit dem PI3K/AKT-Signalweg in Verbindung stehen, wie AZD5363, in die klinische Erprobung eingetreten und haben bedeutende therapeutische Wirkungen erzielt. Die Untersuchung von Inhibitoren, die mit diesem Signalweg in Verbindung stehen, ist für die Behandlung von CRPC von großem Wert.
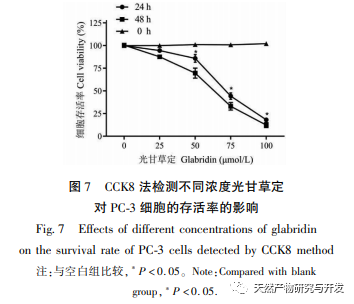
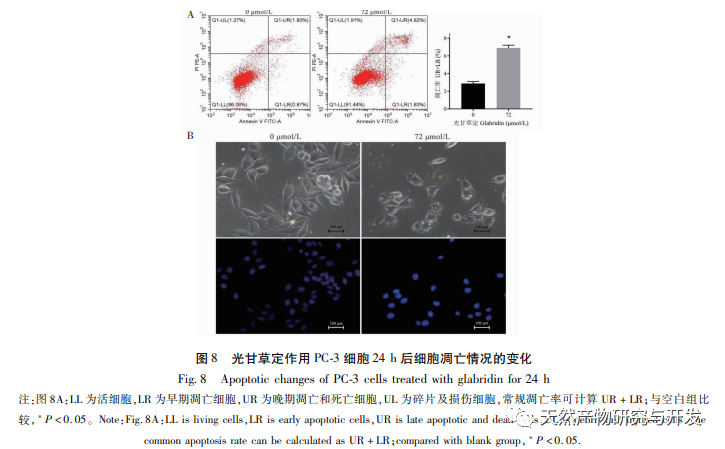
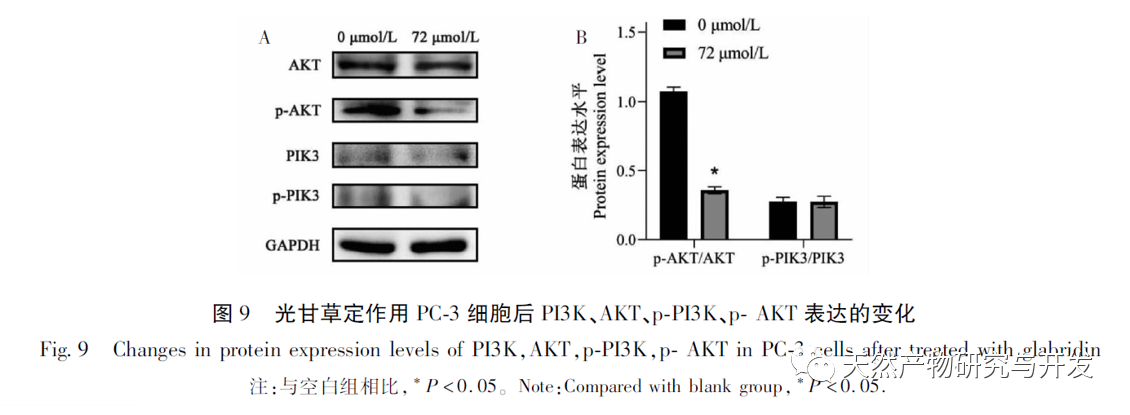
Mit der CCK8-Methode fanden wir außerdem heraus, dass Glycyrrhizin die Proliferation von PC-3-Zellen erheblich hemmen kann. Durchflusszytometrie und DAPI-Färbeexperimente zeigten, dass es die Apoptose von Zellen auslösen kann, und unter dem Mikroskop wurden eine Abnahme der Zellzahl und eine morphologische Schrumpfung beobachtet. Beim Screening der Konzentrationen von Anti-Tumor-Medikamenten stellten wir fest, dass ihre IC50 etwas höher war, was mit der halbflexiblen Docking-Methode zusammenhängt, die für das molekulare Docking verwendet wurde. Im Vergleich zum flexiblen Docking ist die durch semiflexibles Docking berechnete Bindungsenergie niedriger. Außerdem hat Glycyrrhizin als natürliches Antioxidans eine starke antioxidative Wirkung. Allerdings zeigten niedrig dosierte natürliche Antioxidantien keine gute Anti-Tumor-Aktivität in Anti-Tumor-Experimenten, während hoch dosierte natürliche Antioxidantien toxische Wirkungen auf Zellen haben, und der spezifische Mechanismus muss weiter erforscht werden. Basierend auf dem KEGG-Signalweg, der durch die Netzwerkpharmakologie vorhergesagt wurde, sagen wir voraus, dass die hemmende Wirkung von Glycyrrhizin auf PC-3-Zellen hauptsächlich mit dem PI3K/AKT-Signalweg in Verbindung stehen könnte. Weitere Western-Blot-Experimente wurden durchgeführt, um die Wirkung von Glycyrrhizin auf die Expression von Proteinen zu untersuchen, die mit dem PI3K/AKT-Signalweg in PC-3-Zellen zusammenhängen. Die Ergebnisse zeigten, dass Glycyrrhizin den Phosphorylierungsprozess von AKT-Proteinen signifikant hemmen kann. In unserem Experiment wurde beobachtet, dass Glycyrrhizin die Expression von phosphoryliertem AKT-Protein signifikant hemmen kann, aber die hemmende Wirkung auf die Expression von phosphoryliertem PI3K-Protein war nicht wie erwartet. Auch nach wiederholter Anpassung der Konzentration und des Verhältnisses der Proteinbeladung und nach strenger Standardisierung des Vorgangs zeigte das Protein immer noch keine signifikanten Auswirkungen. Es wird angenommen, dass der Grund dafür in der Qualität des p-PI3K-Proteins selbst liegt, das eine geringe Wirksamkeit aufweist. Aufgrund der begrenzten finanziellen Mittel für diese Studie haben wir jedoch die Proteine anderer Produkte nicht ersetzt. In zukünftigen Experimenten werden wir weitere verwandte Proteine dieses Signalweges analysieren, um unsere Hypothese zu überprüfen.
Zusammenfassend wurde in dieser Studie der potenzielle Wirkmechanismus von Glycyrrhizin bei kastrationsresistentem Prostatakrebs durch Netzwerkpharmakologie analysiert und vorhergesagt und durch molekulares Docking und In-vitro-Zellexperimente weiter verifiziert. Die Ergebnisse zeigten, dass Glycyrrhizin die Proliferation hemmen und die Apoptose von PC-3-Zellen auslösen kann, wobei der Mechanismus mit dem Phosphorylierungsprozess des AKT-Proteins zusammenhängt. Daher spekulieren wir, dass sein Anti-CRPC-Mechanismus hauptsächlich durch die Regulierung der Phosphorylierung von Proteinen, die mit dem PI3K/AKT-Signalweg in Verbindung stehen, erfolgen könnte. Diese Studie liefert nicht nur Forschungsideen für die Erforschung des molekularen Mechanismus von Guanggancao Ding bei der Behandlung von kastrationsresistentem Prostatakrebs, sondern auch eine effektive Methode für die Entwicklung und klinische Anwendung von Antitumor-Medikamenten, die Flavonoide in Lakritze enthalten.
