Tre hundrede stave baseret på PI3K/AKT/mTOR-stien fremmer lipopolysakkarid-induceret autofagi og hæmmer inflammation i RAW264.7-celler
Lipopolysaccharid (LPS) er et endotoksin, der frigives af gramnegative bakterier, og som kan stimulere inflammatoriske immunresponser ved bakterietoksicitet forårsaget af gramnegative bakterieinfektioner i menneskekroppen. Makrofager deltager ofte i inflammatoriske reaktioner og fagocytose, og den LPS-behandlede makrofaglinje RAW 264.7 er en almindeligt anvendt cellemodel for inflammatoriske reaktioner i immunceller. Autofagi er en katabolsk proces, hvor cytoplasmatisk indhold transporteres af autofagosomer til lysosomer til omfattende nedbrydning for at opretholde cellulær homeostase. Autofagi, som er en vigtig cellulær mekanisme, er involveret i forekomsten og udviklingen af forskellige sygdomme som autoimmune sygdomme, inflammatoriske sygdomme og tumorer. Inflammatorisk respons er en type immunforsvarsfunktion i kroppens væv. Moderat inflammatorisk respons hjælper med at reparere skader på kroppen, men overdreven inflammatorisk respons kan føre til uønskede reaktioner i kroppen og forårsage degeneration og nekrose af organer, væv og celler og endda bringe livet i fare. Mange studier har fundet en tovejskommunikation mellem autofagi og inflammation. Moderat autofagi kan svække den inflammatoriske reaktion, men overdreven autofagi kan forværre den inflammatoriske reaktion. Flere immunmediatorer kan inducere eller hæmme autofagi, men genoprettelsen af dens homeostase er stærkt afhængig af autofagi. Derfor kan en fuld forståelse af den regulerende mekanisme for autofagi på inflammation effektivt behandle inflammatoriske og autoimmune sygdomme.
Tre hundrede pinde stammer fra roden af Toddalia asiatica (L.) Lam, en plante i Rutaceae-familien. I "Tujia Medicinal Records" står der tydeligt, at den virker ved at "fordrive vind og fugt, fremme blodcirkulationen og afslappe sener, reducere hævelser og lindre smerter". Undersøgelser af den kemiske sammensætning har vist, at de vigtigste kemiske komponenter i Sanbai-staven er alkaloider og coumariner. Moderne farmakologisk forskning har bekræftet, at ekstraktet af Sanbai-staven har antireumatiske, antiinflammatoriske, antitumor- og andre virkninger. Vores foreløbige eksperimentelle forskning har vist, at Sanbai stick kan blokere autofagi flow gennem phosphatidylinositol 3-kinase / proteinkinase B / mammalian rapamycin target protein (PI3K / AKT / MTOR) signalvej og derved hæmme spredningen og inducere apoptose af fibroblastcellelinjen MH7A. Toddalia asiatica alkoholekstrakts (TAAE) rolle i autofagi er dog stadig umoden. Resultaterne af denne undersøgelse viste, at TAAE udløser autofagi på en koncentrationsafhængig måde. For yderligere at verificere, om TAAE spiller en vigtig rolle i autofagi af RAW 264.7-makrofager gennem PI3K/AKT/mTOR-vejen, brugte dette eksperiment LPS-stimulerede RAW 264.7-celler som en model til at undersøge virkningerne af TAAE på autofagi og immunfunktion af RAW 264.7-celler og udforske den molekylære mekanisme for TAAE-regulering af medfødt immunrespons.
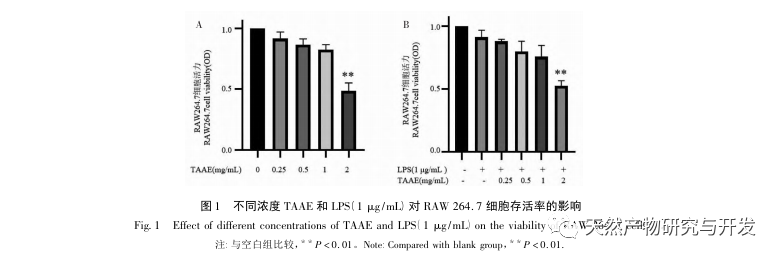
Makrofager er en af de vigtigste immunceller i menneskekroppen. De kan hurtigt aktivere stresstilstande mod patogener, der invaderer menneskets væv og blod, hvilket fører til en række inflammatoriske reaktioner. De er vigtige medfødte immunceller, der er tæt forbundet med forekomsten og udviklingen af inflammation. Inflammation er en kompleks patologisk reaktion, som er forårsaget af en række fysiske reaktioner i immunsystemet, når det udsættes for ekstern skade eller infektion. Det er en vigtig del af patofysiologien ved mange kroniske sygdomme, f.eks. neurodegenerative sygdomme, leddegigt, arteriosklerose osv. En undersøgelse har vist, at TAAE kan hæmme Toll like receptor 4/nuclear factor - κ B (TLR4/NF - κ B) og derved reducere udtrykket af kollageninducerede inflammatoriske cytokiner interleukin-1 β (IL-1 β) og tumornekrosefaktor - α (TNF - α) i synovium hos rotter (CIA), hæmme rheumatoid arthritis synovitis og undertrykke udviklingen af rheumatoid arthritis. TAAE kan også hæmme den nukleare indtrængen af NF - κ B og derved undertrykke frigivelsen af inflammatoriske faktorer og hæmme synovialproliferation. Yang et al. fandt, at ethanolekstraktet og ethylacetatekstraktet af 300 pinde kan hæmme ledhævelse i CIA-rotte-modeller, reducere proinflammatoriske faktorer som TNF - α, IL-1 β og interleukin-6 (IL-6) og øge udtrykket af den immunosuppressive faktor interleukin-10 (IL-10) i serum. Alt det ovenstående viser de fremragende antiinflammatoriske og antireumatiske virkninger af de tre hundrede pinde.
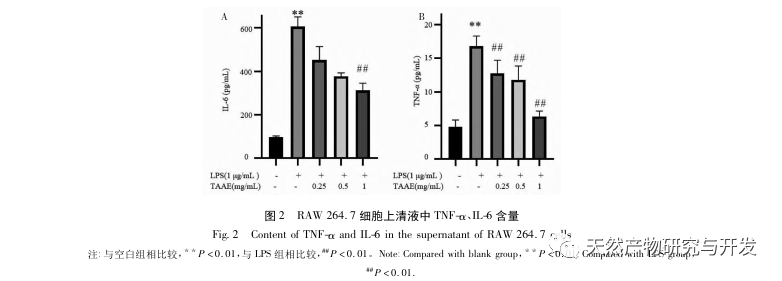
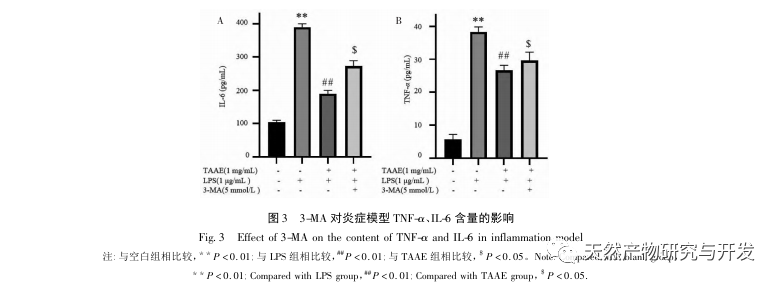
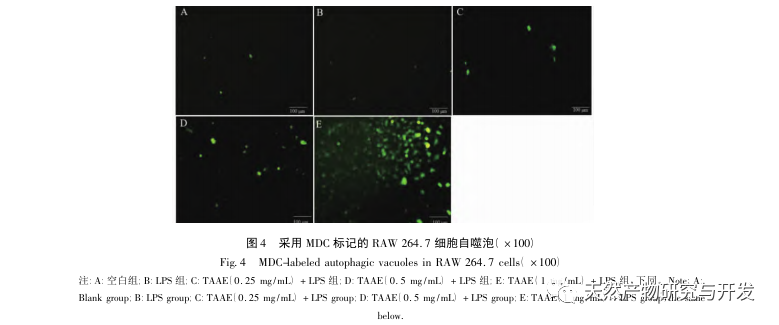
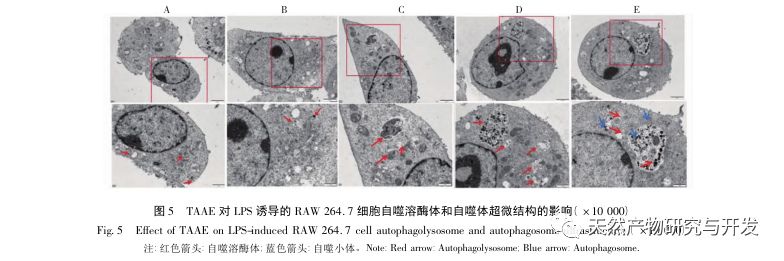
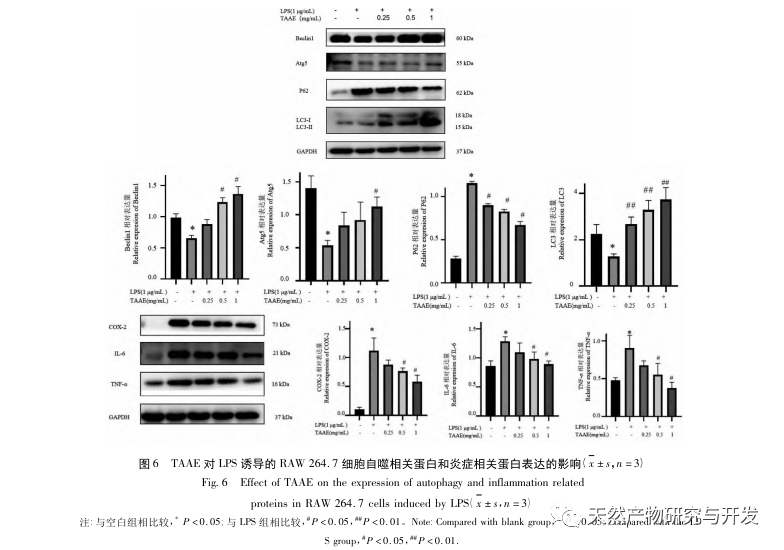
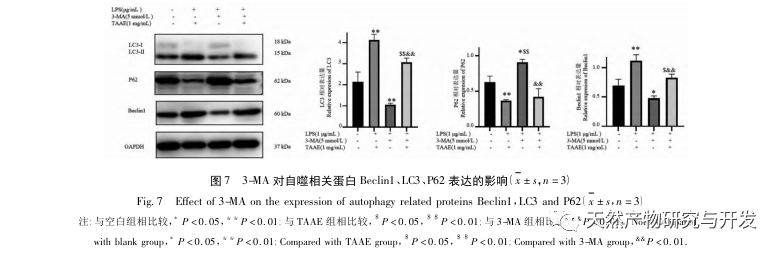
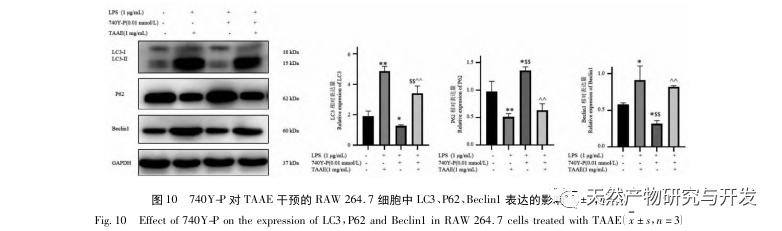
Autofagi er den proces, hvor eukaryote celler bruger lysosomer til at nedbryde deres egne cytoplasmatiske proteiner og beskadigede organeller under regulering af autofagirelaterede gener. Denne proces kan nedbryde invaderende patogene mikroorganismer, beskadigede organeller og unormalt ophobede proteiner og spiller en vigtig rolle i biologiske processer som cellekvalitetskontrol, metabolisme og medfødt og adaptiv immunitet. Mange undersøgelser har bekræftet, at autofagi har en dobbeltrettet effekt på inflammation: På den ene side kan autofagi modvirke inflammatoriske reaktioner ved at fjerne inflammatoriske proteinaggregater og nedregulere proinflammatoriske cytokiner, der forårsager vævsskade; På den anden side aktiverer autofagi inflammasomer, der producerer en stor mængde inflammatoriske faktorer og derved fremskynder den inflammatoriske proces. Efter at have afbalanceret de positive og negative aspekter af immunitet og inflammation kan autofagi ses som en beskytter mod infektion, autoimmunitet og inflammation. Det mikrotubuli-associerede protein light chain 3-II (LC3-II) er et kendetegnende protein for autofagi. Under autofagi forbindes LC3-I til et fosfatidylethanolmolekyle ved hjælp af Atg5-Atg12-Atg16-komplekset for at danne LC3-II. P62 er et substrat for autofagisk nedbrydning og spiller en afgørende rolle i genkendelsen og indkapslingen af nedbrudte substrater. Når Beclin1 er overudtrykt i pattedyrceller, fremmer det cellulær autofagi. Derfor kan LC3, Beclin1, P62 og Atg5 fungere som markørproteiner for autofagi. For at undersøge, om den antiinflammatoriske effekt af TAAE er relateret til autofagi, brugte denne undersøgelse Western blot til at påvise proteinudtrykket af autofagirelaterede proteiner P62, Beclin1, Atg5 og LC3 samt proteinudtrykket af inflammationsrelaterede proteiner TNF - α, IL-6 og cyclooxygenase-2 (COX-2). De eksperimentelle resultater viste, at efter TAAE-intervention steg proteinekspressionsniveauerne af Beclin1, Atg5 og LC3-II/LC3- gradvist, mens ekspressionsniveauet af substrat P62-protein gradvist faldt, og ekspressionen af inflammationsrelaterede proteiner faldt også. De eksperimentelle resultater ved hjælp af MDC-metoden til mærkning af autofagosomer og transmissionselektronmikroskopi til observation af autofagosomer viste også, at TAAE fremmede autofagi i RAW 264.7-celler. For yderligere at demonstrere effekten af autofagi på inflammation blev autofagi-inhibitoren 3-MA, som også er en specifik inhibitor af PI3K-signalvejen, brugt til at kontrollere makrofag-autofagi, blokere autofagisk chelering og proteinnedbrydning. Resultaterne viste, at autofagi-inhibitoren 3-MA svækkede den hæmmende effekt af TAAE på inflammatoriske cytokiner, mens TAAE-intervention effektivt kunne reducere udskillelsen af cytokiner TNF - α og IL-6 i den inflammatoriske model, hvilket igen viser, at TAAE udøver antiinflammatoriske virkninger ved at fremme autofagi i RAW 264.7-celler.
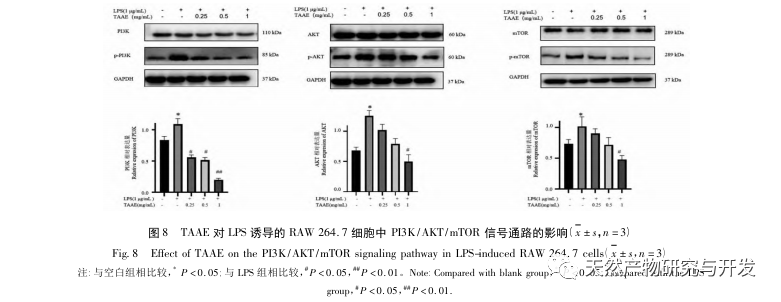
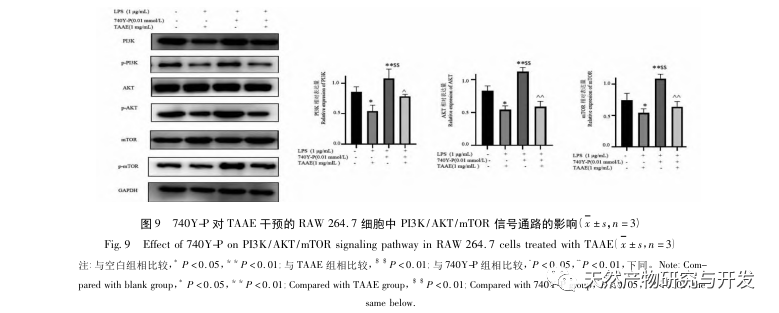
PI3K/AKT/mTOR-signalvejen spiller en vigtig rolle i reguleringen af autofagi, og autofagi-niveauerne øges, når PI3K/AKT/mTOR-vejen hæmmes. MTOR er et pattedyrsmål for rapamycin og spiller en vigtig regulerende rolle i autofagi-responsen, idet det fungerer som en vigtig negativ regulerende akse for autofagi. Mange naturprodukter har vist sig at hæmme inflammation og autoimmune sygdomme ved at målrette PI3K/AKT/mTOR-medieret autofagi. Tidligere eksperimenter har bekræftet, at TAAE kan blokere autofagisk flow og fremme apoptose af MH7A-celler gennem PI3K/AKT/mTOR-signalvejen. PI3K/AKT/mTOR-signalvejen blev valideret ved Western blotting, og eksperimentelle data viste, at TAAE signifikant reducerede ekspressionsniveauerne af phosphoryleret PI3K, AKT og mTOR, hvilket indikerer, at TAAE udløser autofagi ved at hæmme PI3K/AKT/mTOR-vejen. Den samtidige brug af PI3K-agonist (740Y-P) viste yderligere, at TAAE inducerer autofagi ved at hæmme PI3K/AKT/mTOR-signalvejen. Desuden er PI3K/AKT/mTOR-signalvejen direkte relateret til inflammation og immunitet. Denne undersøgelse viste, at TAAE-behandling reducerede niveauerne af pro-inflammatoriske cytokiner i LPS-inducerede RAW 264.7-celler. Denne undersøgelse viser, at i det LPS-inducerede inflammatoriske miljø i RAW 264.7-celler hæmmer TAAE den autofagirelaterede vej PI3K/AKT/mTOR, regulerer autofagirelaterede proteiner og inflammatoriske faktorer, fremmer autofagosomlysosomfusion og nedbrydning, påvirker homeostasen i inflammatoriske celler, hæmmer inflammatoriske reaktioner og udøver således antiinflammatoriske virkninger. Resultaterne af denne undersøgelse tyder på, at PI3K/AKT/mTOR er en effektiv vej for TAAE til at udøve antiinflammatoriske virkninger og øge autofagisk aktivitet, hvilket kan give nye ideer til klinisk behandling af autoimmune og metaboliske sygdomme relateret til betændelse og er værd at yderligere dybtgående forskning.
