Veri madenciliği ve deneysel doğrulamaya dayalı olarak sepsisle ilişkili akut böbrek hasarının tedavisinde emodinin etki mekanizmasının araştırılması
Sepsis, konağın enfeksiyona verdiği yanıttaki dengesizliğin neden olduğu, yaşamı tehdit eden bir organ fonksiyon bozukluğudur. Böbrekler, sepsiste en sık etkilenen organlardan biridir ve sepsisle ilişkili akut böbrek hasarı (SA-AKI), sepsis hastalarında genellikle doğrudan ölüm nedeni haline gelir ve yüksek ölüm oranı ile klinik doktorlar için benzeri görülmemiş zorluklar ortaya çıkarır. AKI devam eder ve potansiyel kronik böbrek hastalığı (KBH) riskini artırır. Hayatta kalan hastalar genellikle kaçınılmaz olarak son dönem böbrek hastalığına (SDBH) ilerleyerek yaşam kaliteleri ve güvenlikleri için ciddi bir tehdit oluşturmaktadır.
Ne yazık ki, SA-AKI'yi önleme ve tedavi etme konusundaki mevcut yetenekler çok sınırlıdır. Aktif sıvı bazlı tedavi güvenilir kanıta dayalı tıbba sahip olmayabilir ve hatta zararlı olabilir. Kan basıncını korumak için vazoaktif ilaçların kullanımı, büyük dolaşım ve mikrosirkülasyon arasında bir denge gerektirir ve AKI oluşumunu önlemeye yardımcı olmak için ne kadar kan basıncı hedefinin korunması gerektiği konusunda bir fikir birliği yoktur. Renal önleme başarısız olursa, tedavi için renal replasman tedavisi (RRT) kullanılmalıdır, ancak RRT müdahalesinin optimal zamanlaması ve yöntemi net değildir. SA-AKI hastaları hayatta kalırsa, çoğu hastanın böbrek fonksiyonu iyileşecek olsa da, böbrek onarım mekanizmaları veya böbrek fonksiyon onarımının başarısızlığı hakkında çok az şey bilinmektedir ve yaşam boyu KBH ve SDBY'ye ilerleme riski daha yüksektir. Şu ana kadar AKI tedavisi için kesin ve güvenilir bir ilaç bulunmamaktadır. Geleneksel klinik tedavi önlemleri temel olarak böbrek replasmanı ve semptomatik kapsamlı tedavidir. Böbrek fonksiyonunun onarımı, böbreğin kendisinin bir bütün olarak vücutta güvenilir bir şekilde desteklenmesine bağlıdır. Bu nedenle, SA-AKI'yi erken ve zamanında etkili bir şekilde önleyebilecek veya tedavi edebilecek, kronik böbrek hastalığının ortaya çıkmasını önleyebilecek veya böbrek onarımını teşvik edebilecek ilaçların veya önlemlerin araştırılması, sepsis hastalarının ölüm oranını azaltmak ve hayatta kalan hastaların yaşam kalitesini iyileştirmek için önemli klinik değere sahiptir.
Emodin, ravent ve Polygonum cuspidatum gibi Çin bitkilerinden elde edilen, anti-enflamatuar, antiviral ve anti-tümör gibi çeşitli farmakolojik etkileri olan doğal bir bileşiktir. Önceki çalışmalar emodinin sepsis hastaları üzerinde koruyucu bir etkiye sahip olduğunu doğrulamış; son çalışmalar ise emodinin oksidatif stres, inflamasyon ve hücre apoptozunun neden olduğu hasara karşı koruyucu bir etkiye sahip olduğunu göstermiştir. Bununla birlikte, emodinin SA-AKI hastalarının prognozunu iyileştirip iyileştiremeyeceği hala belirsizdir. Bu çalışma, yaşam bilimleri ile ilgili veri tabanları aracılığıyla SA-AKI patogenezinde yer alan anahtar genleri araştıracak ve bu anahtar genlerde yer alan enflamatuar sinyal yollarını analiz edecektir; Ayrıca, emodinin SA-AKI'nin enflamatuar yolunu ve SA-AKI sıçanları üzerindeki koruyucu etkisini ve mekanizmasını etkileyip etkilemediğini araştırmak için hayvan deneyleri yapılmış, önlenmesi ve tedavisi için yeni fikirler sağlanmıştır.

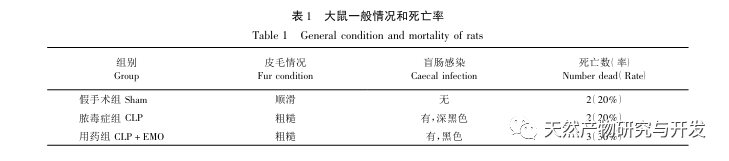


Araştırmalar SA-AKI patogenezinin çok faktörlü ve karmaşık olduğunu, inflamasyon, mikro dolaşım disfonksiyonu ve metabolik yeniden programlama arasındaki etkileşimi içerdiğini göstermiştir. Patofizyolojisi, birden fazla hücre tipinin hasar görmesini ve işlev bozukluğunu içerir. Sepsis sürecinde bakteriler endotoksin veya endotoksin benzeri maddeler salarak vücuttaki nötrofiller, monositler ve endotel hücreleri gibi enflamatuar hücreleri aktive eder ve kan dolaşımına büyük miktarda endojen enflamatuar mediatör salgılar. Bu durum bir yandan böbrekler de dahil olmak üzere birçok organda hasara yol açarken, diğer yandan da daha fazla iltihap hücresinin hastalığa katılmasını sağlayarak kötü huylu bir bağışıklık ağı yanıtı oluşturur. Lipopolisakkarit (LPS) ile indüklenen SA-AKI'nin SD sıçan modelinde nerolidol, NF - κ B ve Toll benzeri reseptör 4 (TLR4) sinyal yolaklarını inhibe ederek SA-AKI'yi hafifletir. TLR4/NF - κ B yolağının renal enflamasyon yanıtı sürecine dahil olduğu doğrulanmıştır ve TLR4/NF - κ B aracılı enflamatuar yanıtın inhibe edilmesi LPS kaynaklı AKI üzerinde koruyucu bir etkiye sahiptir. İnflamatuar yanıtın SA-AKI patogenezinde önemli bir mekanizma olduğu ve inflamatuar yanıt yolunun inhibe edilmesinin sepsis için önemli bir tedavi seçeneği olduğu ve SA-AKI hastalarının klinik tedavisi için yeni fikirler sağladığı görülebilir.
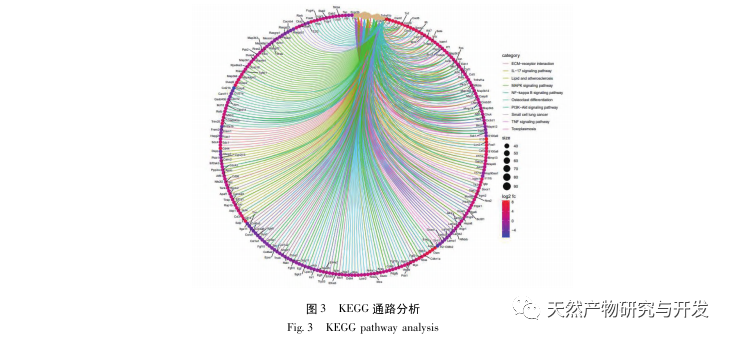
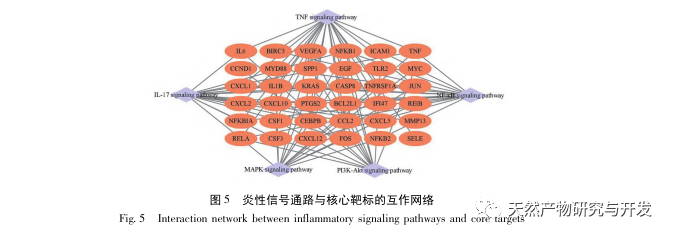
Bu çalışmada SA-AKI patogenezinde yer alan 2801 anahtar hedefi analiz etmek için biyolojik bir veri tabanı kullanılmıştır. Bu hedeflerin KEGG analizi, TNF sinyal yolu ve IL-17 sinyal yolunun üst sıralarda yer aldığı ve NF - κ B sinyal yolunun her iki yolun da SA-AKI patogenezine katılması için bir merkez görevi gördüğü toplam 5 temel enflamatuar yanıt sinyal yolunu ortaya çıkarmıştır. TNF sinyal yolunda, TNF - α sadece NF - κ B sinyalinin anahtar yukarı yönlü aktivatörü değil, aynı zamanda NF - κ B sinyal yolunun aşağı yönlü yanıt veren bir molekülü olarak hizmet eder, bu da NF - κ B sinyal yolunu pozitif geri besleme yoluyla desteklediğini ve ikisinin birbirini tamamladığını gösterir. IL-17 sinyal yolunda, IL-17A, IL-17 ailesindeki ana başlatıcı faktördür ve Th17 hücreleri ana salgılayan hücrelerdir. CLP ile indüklenen modelde, IL-17A'nın karın boşluğunda yüksek oranda eksprese edildiği ve şiddetli sepsis sonrası inflamatuar yanıtta kilit rol oynadığı bulunmuştur. Karın boşluğunda IL-17A'nın nötralize edilmesi, pro-enflamatuar sitokinlerin üretimini azaltabilir. Bu arada, çalışmalar dendritik hücrelerdeki (DC'ler) Toll benzeri reseptör 9'un (TLR9) gama delta T hücreleri tarafından IL-17A üretimine aracılık ederek SA-AKI gelişiminde kilit bir rol oynayabileceğini göstermiştir; Diğer çalışmalar IL-17A'nın devre dışı bırakılmasının SA-AKI'yi önleyebileceğini göstermiştir. Yukarıdakiler, TNF - α ve IL-17A'nın sepsiste pro-enflamatuar faktörler olduğunu ve TNF sinyal yolağı ile IL-17 sinyal yolağının sepsisin oluşumu ve gelişiminde yaygın olarak yer aldığını göstermektedir ki bu da veri analizi sonuçlarıyla tutarlıdır.
Sepsisin emodin ile tedavisi üzerine, özellikle beyin, kan, kalp, bağırsak ve akciğer dokularına odaklanan birçok çalışma yapılmıştır. Sepsis ilişkili ensefalopatide (SAE), emodin bilişsel bozukluğu ve patolojik hasarı iyileştirebilir ve BDNF / TrkB sinyalini yukarı doğru düzenleyerek farelerde CLP kaynaklı inflamasyonu inhibe edebilir. Kan sisteminde, emodin P-selektini aşağı regüle eder, sepsisin geç evresinde trombosit sayısını ve agregasyon yeteneğini artırır ve endojen pıhtılaşma faktörü aktivitesini ve fibrinojen fonksiyonunu artırarak anti-enflamatuar etkiler gösterir. Septik kardiyomiyopatide, emodinin septik sıçanlarda kardiyak disfonksiyonu tersine çevirebildiği ve miyokardiyal durumu iyileştirebildiği bulunmuştur, bu da inflamazom aktivasyonunu inhibe etmesiyle ilgili olabilir. Sepsisin neden olduğu bağırsak hasarında emodin, enflamatuar faktörlerin ve oksidatif stres belirteçlerinin seviyelerini azaltarak bağırsak mukozal hasarını iyileştirebilir ve etki mekanizması VDR/Nrf2/HO-1 yolağı ile ilişkili olabilir; Ve sıkı bağlantı (TJ) proteininin ekspresyon seviyesini artırarak bağırsak bariyerinin bütünlüğünü korur ve bağırsak bariyeri geçirgenliğini inhibe eder. Emodin, bağırsağın enflamatuar tepkisini ve bariyer işlevini iyileştirmenin yanı sıra, Escherichia coli'nin yer değiştirmesini önleyebilir, bakterilerin yayılmasını ve transferini önleyebilir ve bakterilerin neden olduğu ikincil zararı azaltabilir. Sepsise bağlı akut akciğer hasarında, emodin NF - κ B ve yüksek hareketlilik grubu kutusu 1 (HMGB1) yolaklarını inhibe edebilir, böylece pulmoner oksidatif stresi ve enflamatuar yanıtı azaltabilir. Akciğerler üzerinde yapılan bir başka çalışma da otofaji yolağına dayanmaktadır ve emodin müdahalesi akut akciğer hasarının ilerlemesini etkili bir şekilde önleyebilir. Ayrıca, diğer çalışmalar emodinin sepsis kaynaklı akut akciğer hasarında akuaporin (AQP), TJ, enflamatuar faktörler ve akciğer hücresi apoptozunu düzenleyerek pulmoner doku ödemini etkili bir şekilde hafifletebileceğini göstermiştir. Emodinin SA-AKI üzerindeki çalışması henüz rapor edilmemiştir. Bu çalışma sayesinde, emodin ile tedavi edilen CLP modeli sıçanların ELISA sonuçlarında TNF - α, IL-17 ve IFN - γ ekspresyonunda azalma gösterdiği bulunmuştur ki bu da emodinin sepsis inflamasyonu üzerindeki inhibitör etkisiyle tutarlıdır.
Emodinin Th17/Treg enflamatuar ekseni üzerindeki aynı etkisi de aydınlatılmıştır. Akut pankreatit çalışmasında, emodinin IFN - γ/IL-17 oranını düzenleyerek şiddetli akut pankreatitte immün yanıtı inhibe ettiği ve böylece bağırsak bariyeri işlev bozukluğunu hafiflettiği bulunmuştur. Bu çalışmada da SA-AKI'de emodinin IL-17A ekspresyonunu azaltabildiği ve enflamatuar yanıtı iyileştirebildiği bulunmuştur.
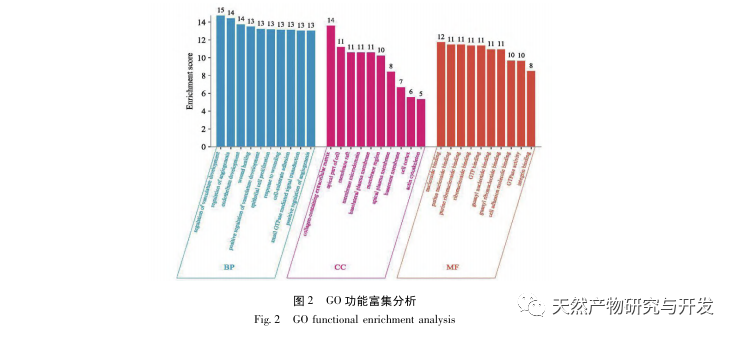
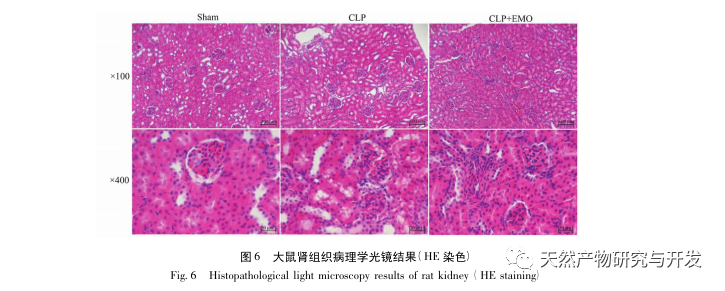
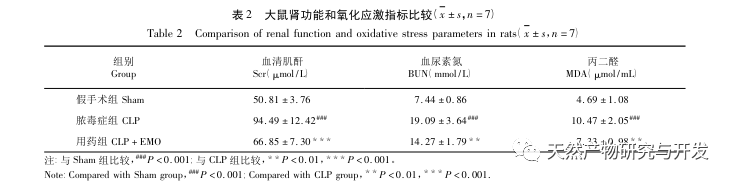
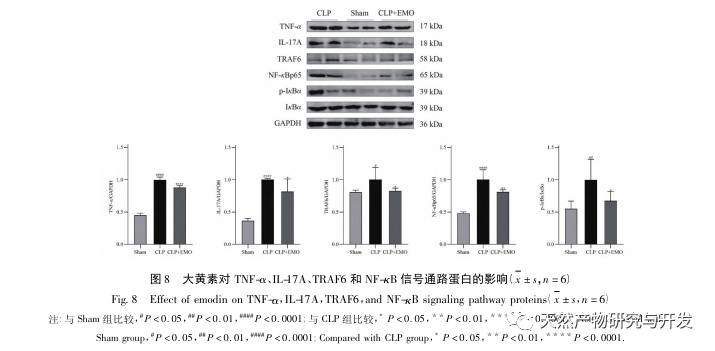
Özetle, bu çalışma veri madenciliği yoluyla emodin patogenezinde yer alan 2801 anahtar gen tanımlamıştır. GO biyolojik süreç analizi, bu hedeflerin biyolojik işlevlerinin esas olarak membran sinyal iletimi, vasküler düzenleme ve yara iyileşmesini içerdiğini göstermektedir. KEGG yolak zenginleştirme analizi TNF, IL-17, PI3K Akt, NF - κ B ve MAPK sinyal yolaklarının inflamasyonla ilgili sinyal yolaklarında zenginleştiğini göstermiştir. Deneysel doğrulama, emodin tedavisinin SA-AKI'de böbrek fonksiyonunu iyileştirdiğini ve oksidatif stres (MDA) ve inflamatuar sitokin (TNF - α, IL-17 ve IFN - γ) seviyelerinin azaldığını göstermiştir. IL-17A, TNF - α, TRAF6, NF - κ Bp65'in protein ekspresyonu ve I κ B α'nın fosforilasyon seviyesi, veri analizi sonuçlarıyla tutarlı olarak CLP grubuna kıyasla önemli ölçüde azalmıştır. Emodinin sıçanlarda SA-AKI'yi iyileştirebileceği ve bunun da IL-17/NF - κ B ve TNF/NF - κ B sinyal yolaklarıyla ilişkili olabileceği düşünülmektedir.
