Ишемическая цереброваскулярная болезнь включает в себя два типа: транзиторный ишемический инсульт и церебральный инфаркт. Среди них инфаркт головного мозга в традиционной китайской медицине называется ишемическим инсультом (ИИ) - это заболевание, вызванное различными причинами, приводящими к локальным нарушениям кровоснабжения участков мозговой ткани, в результате чего возникают ишемические и гипоксические поражения и некроз тканей мозга, а в дальнейшем - ряд неврологических функциональных нарушений. Высокие показатели смертности и инвалидизации, а также сложные патологические механизмы ежегодно ложатся тяжелым экономическим бременем на весь мир. Кислородно-глюкозная депривация (КГД) в клетках мозга - наиболее распространенная модель ишемического инсульта in vitro, широко используемая в фундаментальных и доклинических исследованиях инсульта.
Аутофагия широко распространена в эукариотических клетках и играет важную роль в регуляции процессов выживания и гибели клеток. Большое количество исследований указывает на то, что аутофагия тесно связана с возникновением и развитием ишемического повреждения мозга. Некоторые исследования показали, что аутофагия нейронов может облегчить ишемическое повреждение мозга, в то время как другие сообщили, что аутофагия нейронов может усугубить ишемическое повреждение мозга, но конкретный механизм до сих пор не ясен.
β - никотинамид мононуклеотид (NMN) присутствует в различных продуктах питания и играет важнейшую роль в регуляции клеточного старения и поддержании нормальных функций организма. Он участвует в трансдукции многих важных внутриклеточных сигнальных путей. Существуют исследования, согласно которым введение NMN in vitro может быстро превратить его в NAD+ для регулирования клеточного старения и поддержания нормальных функций организма. NMN может компенсировать снижение NAD+, вызванное ИБС, и улучшать повреждение нейронов при ишемии головного мозга. Это позволяет предположить, что NMN играет определенную роль в ИБ. Исследования показали, что NMN может способствовать регенерации нейрососудов, улучшать эндотелиальную функцию микрососудов мозга, оказывать противовоспалительное и антиапоптотическое действие. Есть также несколько исследований, предполагающих, что NMN может оказывать противоишемическое действие при повреждении мозга путем регуляции аутофагии, но конкретный механизм, с помощью которого NMN регулирует аутофагию и противодействует ИБС, пока не ясен.
Целью данного исследования является создание модели клеток PC12, лишенных кислорода и глюкозы. Выживаемость клеток измеряли методом МТТ in vitro, аутофагосомы и аутолизосомы обнаруживали с помощью просвечивающей электронной микроскопии, интенсивность флуоресценции аутофагосом наблюдали с помощью МДК, а экспрессию связанных с аутофагией белков LC3-II/LC3-I, Beclin1, p62 и P-mTOR/mTOR определяли с помощью Вестерн-блота. Цель исследования - выяснить влияние NMN на индуцированное ОГД аутофагическое повреждение в клетках PC12.




Исследование Lancet 2017 года показало, что инсульт является основным заболеванием, приводящим к многолетней потере жизни в Китае, с быстрым прогрессированием болезни, высокими показателями смертности и инвалидности. Среди них на долю ИБ приходится от 60% до 70% всех инсультов, причиной которых является закупорка сосудов, приводящая к снижению кровоснабжения определенного участка мозга. После церебральной ишемии и гипоксии может начаться ряд патологических и физиологических реакций, таких как аутофагия, апоптоз, окислительный стресс и перегрузка внутриклеточным кальцием. Длительный цикл восстановления выживших после ИБС увеличивает глобальное экономическое бремя. В настоящее время существует множество противопоказаний к препаратам, используемым на рынке для профилактики и лечения ИБС. Поэтому необходимо постоянно искать препараты для профилактики и лечения ИБС. ОГД - классическая модель для изучения ИБ in vitro. Клеточная линия PC12 - одна из наиболее распространенных клеточных линий для изучения повреждения нейронов, часто используемая в исследованиях повреждения при ишемии и гипоксии. Поэтому в данном эксперименте использовалась модель клеток OGD PC12 для исследований in vitro.
NMN - это естественное вещество, встречающееся в организме человека, а также присутствующее во многих продуктах питания, с молекулярной массой 334,22. Он является продуктом реакции никотинамидфосфорибозилтрансферазы, а также одним из ключевых предшественников NAD+. Исследования показали, что регулирование уровня NMN в организме оказывает хороший терапевтический и репаративный эффект при сердечно-сосудистых и цереброваскулярных заболеваниях, нейродегенеративных заболеваниях и возрастных дегенеративных заболеваниях. Также есть данные о том, что введение NMN может уменьшить размер инфаркта и неврологические повреждения в модели MCAO у крыс. В этом эксперименте был использован МТТ-тест, чтобы продемонстрировать, что OGD может снизить выживаемость клеток PC12. NMN может увеличить выживаемость клеток PC12 при ОГД в концентрациях 400, 800 и 1600 мк моль/л, при этом наибольшая выживаемость наблюдается при концентрации 800 мк моль/л. Однако не было обнаружено существенной разницы в выживаемости клеток между концентрациями NMN200 и 3200 мк моль/л, что указывает на то, что концентрация 200 мк моль/л еще не достигла эффективной концентрации для улучшения выживаемости клеток PC12, вызванной ОГД, а концентрация 3200 мк моль/л могла вызвать определенный ущерб для клеток из-за чрезмерной концентрации.
Аутофагия, также известная как программируемая клеточная смерть II типа, представляет собой процесс, в котором клетки под контролем генов, связанных с аутофагией, используют лизосомы для деградации поврежденных, денатурированных или стареющих макромолекул и органелл для поддержания их выживания, дифференциации, роста и стабильности. Исследования показывают, что аутофагия индуцируется после ИБС, а также возникает и развивается вместе с патологическим процессом ИБС, играя различные регуляторные роли в острой, подострой, восстановительной и последующей стадиях ИБС.
MTOR - это атипичная серин/треониновая протеинкиназа с относительной молекулярной массой 289 кДа. При связывании с различными белками может образовывать два различных комплекса, а именно mTORCl и mTORC2. MTORCl чувствителен к рапамицину и отвечает за интеграцию факторов роста и питательных сигналов, в основном регулируя клеточную аутофагию, биогенез рибосом, трансляцию белков и синтез липидов. MTORT считается клапаном для аутофагии. Исследования показали, что фосфорилированный mTOR может облегчать окислительное повреждение при лишении глюкозы и играть защитную роль в клетках. 3-MA - широко используемый ингибитор аутофагии. RAPA - это ингибитор mTOR, который может вызывать аутофагию путем ингибирования mTORC1, также известного как активатор аутофагии. В этом эксперименте были созданы группы 3-MA и RAPA для вмешательства и регулирования OGD-индуцированной аутофагии в клетках PC12; в то же время были созданы группы 3-MA, RAPA и комбинации препаратов для наблюдения за тем, может ли NMN противодействовать эффектам 3-MA или RAPA на OGD-индуцированную аутофагию в клетках PC12.
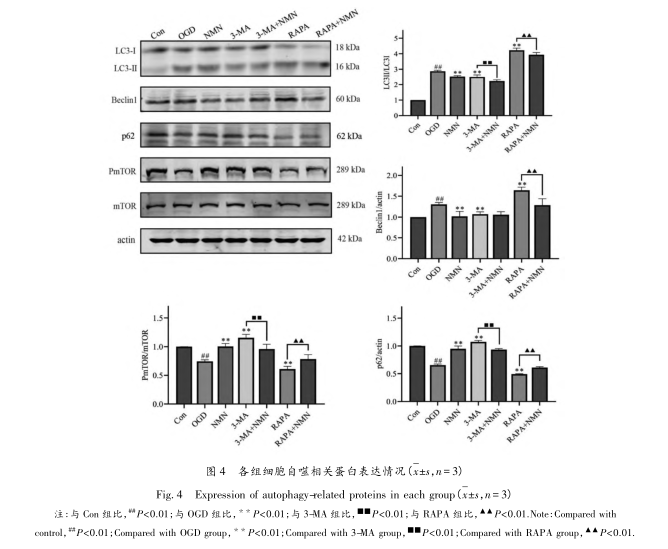
Уровни белков Beclin-1, LC3 и p62 могут служить важными индикаторами аутофагии. Беклин-1 является зрелым регулятором аутофагии, который положительно коррелирует с аутофагией. Beclin1 взаимодействует с такими белками, как VPS15, VPS34, ATG14, выполняя функции аутофагии и мембранного транспорта. LC3 является гомологом убиквитин-подобного модификатора ATG8 у дрожжей, который, как считается, играет роль в аутофагии. После обработки ATG4 LC3 теряет свой С-концевой остаток и превращается в LC3-I. LC3-I подвергается каскаду убиквитинирующих ферментативных реакций, ковалентно связывается с липидной молекулой фосфатидилэтаноламина на мембране аутофагосомы, превращаясь в LC3-II. Увеличение соотношения LC3-II/LC3-I указывает на повышение уровня аутофагии. P62 - маркерный белок, отражающий активность аутофагии, и уровень его белка отрицательно коррелирует с аутофагией. То есть, когда происходит аутофагия, белок p62 постоянно деградирует в цитоплазме; когда активность аутофагии ослаблена и функция аутофагии нарушена, белок p62 будет постоянно накапливаться в цитоплазме. Этот эксперимент подтвердил с помощью технологии Вестерн-блот, что NMN может снижать относительные уровни экспрессии белков Beclin1 и LC3-II/LC3-I, а также повышать уровни экспрессии белков P-mTOR/mTOR и p62. Кроме того, трансмиссионная электронная микроскопия и метод MDC подтвердили, что NMN может уменьшать количество и интенсивность аутофагосом и аутолизосом в клетках OGD PC12. Вышеизложенное свидетельствует о том, что NMN может ингибировать OGD-индуцированную аутофагию в клетках PC12.
Таким образом, можно предположить, что определенная доза NMN может противодействовать индуцированному OGD аутофагическому повреждению в клетках PC12, тем самым оказывая защитный эффект на клетки, и этот защитный эффект может быть связан с mTOR-путями. Это исследование может дать определенный целевой ориентир для профилактики и лечения NMN индуцированного OGD аутофагического повреждения, а также накопить лабораторные данные для разработки натурального соединения NMN.
