Az iszkémiás agyi érbetegségnek két típusa van: a tranziens iszkémiás stroke és az agyi infarktus. Közülük az agyi infarktust a hagyományos kínai orvoslás diagnózisában iszkémiás stroke-nak (IS) nevezik, amely különböző okok által okozott betegség, amely helyi vérellátási zavarokhoz vezet az agyszöveti régiókban, ami az agyszövet iszkémiás és hipoxiás elváltozásait és nekrózisát eredményezi, és ezt követően egy sor neurológiai működési zavart okoz. A magas halálozási és rokkantsági arány, valamint az összetett patológiai mechanizmusok minden évben jelentős gazdasági terhet rónak a világra. Az oxigén-glükózmegvonás (OGD) agysejtekben az ischaemiás stroke leggyakrabban használt in vitro modellje, amelyet széles körben alkalmaznak az alap- és preklinikai stroke-kutatásban.
Az autofágia széles körben jelen van az eukarióta sejtekben, és fontos szerepet játszik a sejtek túlélési és halálozási folyamatainak szabályozásában. Számos tanulmány utal arra, hogy az autofágia szorosan összefügg az iszkémiás agykárosodás kialakulásával és fejlődésével. Egyes tanulmányok kimutatták, hogy a neuronális autofágia enyhítheti az ischaemiás agykárosodást, míg mások arról számoltak be, hogy a neuronális autofágia súlyosbíthatja az ischaemiás agykárosodást, de a konkrét mechanizmus még mindig nem világos.
A β - nikotinamid-mononukleotid (NMN) jelen van különböző élelmiszerekben, és létfontosságú a sejtek öregedésének szabályozásában és a normál testi funkciók fenntartásában. Számos fontos intracelluláris jelátviteli útvonal átvitelében vesz részt. Vannak kutatási jelentések arról, hogy az NMN in vitro adagolása gyorsan NAD+ -dá alakítható a sejtek öregedésének szabályozása és a normál testi funkciók fenntartása érdekében. Az NMN kompenzálhatja az IS által okozott NAD+-csökkenést, és javíthatja az agyi iszkémia során bekövetkező neuronális károsodást. Ez arra utal, hogy az NMN bizonyos szerepet játszik az IS-ben. Tanulmányok kimutatták, hogy az NMN elősegítheti a neurovaszkuláris regenerációt, javíthatja az agyi mikrovaszkuláris endotélfunkciót, gyulladáscsökkentő és apoptózisellenes hatásokat fejt ki. Néhány tanulmány arra is utal, hogy az NMN az autofágia szabályozásával iszkémiás agykárosodás elleni hatást fejthet ki, de még nem tisztázott az a specifikus mechanizmus, amellyel az NMN szabályozza az autofágiát és az IS elleni hatást.
E tanulmány célja egy oxigén-glükózmegvonásos PC12 sejtmodell létrehozása. A sejtek túlélési arányát MTT-teszttel mértük in vitro, az autofagoszómákat és autoliszoszómákat transzmissziós elektronmikroszkópiával detektáltuk, az autofagoszómák fluoreszcenciájának intenzitását MDC-vel figyeltük meg, és az LC3-II/LC3-I, Beclin1, p62 és P-mTOR/mTOR autofágiával kapcsolatos fehérjeexpresszióját Western blot segítségével detektáltuk. A cél az NMN hatásának tisztázása az OGD által indukált autofágikus károsodásra a PC12 sejtekben.




A 2017-es Lancet-tanulmány kimutatta, hogy a stroke a fő betegség, amely Kínában éveken át tartó életveszteséget okoz, a betegség gyors lefolyásával, magas halálozási és rokkantsági rátával. Ezek közül az IS az összes stroke 60% - 70%-ért felelős, amelyet az agy egy bizonyos területének vérellátásának csökkenéséhez vezető érelzáródás okoz. Az agyi iszkémia és hipoxia után egy sor patológiai és fiziológiai reakciót indíthat el, mint például az autofágia, az apoptózis, az oxidatív stressz és az intracelluláris kalcium-túlterhelés. Az IS túlélőinek hosszú felépülési ciklusa megnövelte a globális gazdasági terheket. Jelenleg számos ellenjavallata van a piacon az IS megelőzésére és kezelésére használt gyógyszereknek. Ezért folyamatosan fel kell kutatni az IS megelőzésére és kezelésére szolgáló gyógyszereket. Az OGD klasszikus modell az IS in vitro tanulmányozására. A PC12 sejtvonal az egyik leggyakrabban használt sejtvonal a neuronális sérülések tanulmányozására, amelyet gyakran használnak az iszkémia és a hipoxia okozta sérülések kutatásában. Ezért ez a kísérlet az OGD PC12 sejtmodellt használta in vitro kutatáshoz.
Az NMN az emberi szervezetben természetesen előforduló, 334,22-es molekulatömegű anyag, amely számos élelmiszerben is jelen van. A nikotinamid-foszforibozil-transzferáz reakció terméke és egyben a NAD+ egyik legfontosabb prekurzora. Vizsgálatok szerint az NMN szintjének szabályozása a szervezetben jó terápiás és reparatív hatással van a szív- és érrendszeri és agyi érrendszeri betegségekre, a neurodegeneratív betegségekre és az életkorral összefüggő degeneratív betegségekre. Vannak kutatási jelentések arról is, hogy az NMN adagolása csökkentheti az infarktus méretét és a neurológiai károsodást patkány MCAO modellekben. Ebben a kísérletben MTT-tesztet alkalmaztak annak kimutatására, hogy az OGD csökkentheti a PC12 sejtek túlélési arányát. Az NMN 400, 800 és 1600 μ mol/L koncentrációban növelheti az OGD PC12 sejtek túlélési arányát, a legmagasabb túlélési arányt 800 μ mol/L koncentrációban figyelték meg; azonban nem volt jelentős különbség a sejtek túlélési arányában az NMN200 és 3200 μ mol/L koncentrációk között, ami azt jelzi, hogy a 200 μ mol/L koncentráció még nem érte el a hatékony koncentrációt az OGD indukálta PC12 sejtek túlélési arányának javítására, míg a 3200 μ mol/L koncentráció a túlzott koncentráció miatt bizonyos károsodást okozhatott a sejtekben.
Az autofágia, más néven II. típusú programozott sejthalál, arra a folyamatra utal, amelyben a sejtek az autofágiával kapcsolatos gének szabályozása alatt a lizoszómákat használják a sérült, denaturált vagy öregedő makromolekulák és organellák lebontására, hogy megőrizzék túlélésüket, differenciálódásukat, növekedésüket és stabilitásukat. A kutatások azt mutatják, hogy az autofágia az IS után indukálódik, és az autofágia az IS patológiai folyamatával együtt is előfordul és fejlődik, különböző szabályozó szerepet játszva az IS akut, szubakut, gyógyulási és következményes szakaszaiban.
Az MTOR egy atipikus szerin/treonin fehérje kináz, amelynek relatív molekulatömege 289 kDa. A különböző fehérjékhez való kötődése két különböző komplexet, nevezetesen az mTORCl és az mTORC2 komplexet képezhet. Az MTORCl érzékeny a rapamicinre, és felelős a növekedési faktorok és tápanyagjelek integrálásáért, főként a sejtek autofágiájának, a riboszóma biogenezisének, a fehérjetranszlációnak és a lipidszintézisnek a szabályozásáért. Az MTORT az autofágia szelepének tekinthető. Kutatások kimutatták, hogy a foszforilált mTOR enyhítheti az oxidatív glükózmegvonás okozta károsodást, és védő szerepet játszik a sejtekben. A 3-MA egy általánosan használt autofágia-gátló. A RAPA egy mTOR-gátló, amely az mTORC1 gátlásával képes autofágiát indukálni, amely autofágia-aktivátorként is ismert. Ebben a kísérletben 3-MA és RAPA csoportokat állítottunk fel, hogy beavatkozzunk és szabályozzuk az OGD által indukált autofágiát a PC12 sejtekben. Ugyanakkor 3-MA, RAPA és gyógyszer-kombinációs csoportokat is létrehoztunk, hogy megfigyeljük, hogy az NMN ellensúlyozni tudja-e a 3-MA vagy a RAPA hatását az OGD által indukált autofágiára a PC12 sejtekben.
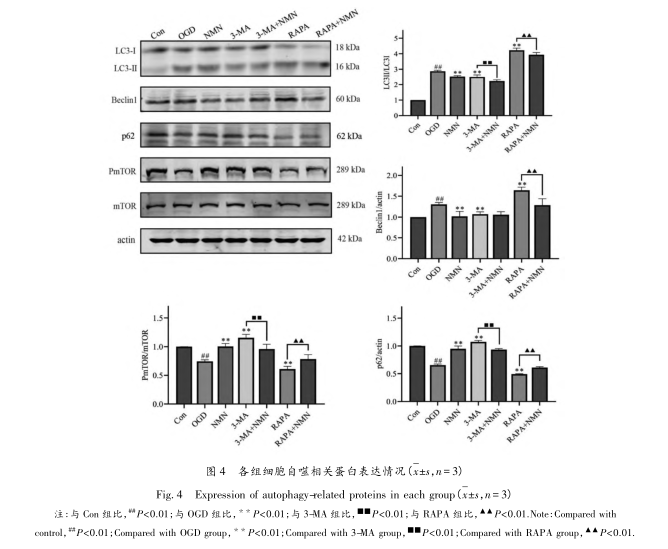
A Beclin-1, az LC3 és a p62 fehérjék szintje az autofágia fontos kimutatási indikátora lehet. A Beclin1 egy érett autofágia szabályozó, amely pozitívan korrelál az autofágiával. A Beclin1 kölcsönhatásba lép olyan fehérjékkel, mint a VPS15, VPS34, ATG14 az autofágia és a membrántranszport funkciók ellátása érdekében. Az LC3 az élesztőben az ATG8 ubikvitinszerű módosító homológja, amelyről úgy gondolják, hogy szerepet játszik az autofágiában. Az ATG4-gyel történő kezelés után az LC3 elveszíti C-terminális maradékát, és LC3-I-vé alakul át. Az LC3-I ubikvitinációhoz hasonló enzimatikus reakciók kaszkádján megy keresztül, kovalensen kapcsolódik az autofágoszóma membránján lévő lipidmolekulához, a foszfatidil-etanolaminhoz, és átalakul LC3-II-vé. Az LC3-II/LC3-I arány növekedése az autofágia szintjének növekedését jelzi. A P62 az autofágia aktivitását tükröző markerfehérje, és fehérjeszintje negatívan korrelál az autofágiával. Azaz, amikor autofágia történik, a p62 fehérje folyamatosan lebomlik a citoplazmában; Amikor az autofágia aktivitása gyengül és az autofágia funkciója károsodik, a p62 fehérje folyamatosan felhalmozódik a citoplazmában. Ez a kísérlet Western blot technológiával megerősítette, hogy az NMN képes lefelé szabályozni a Beclin1 és az LC3-II/LC3-I fehérjék relatív expressziós szintjét, és felfelé szabályozni a P-mTOR/mTOR és a p62 fehérjék expressziós szintjét. Ezenkívül transzmissziós elektronmikroszkópiával és MDC-módszerrel megerősítették, hogy az NMN képes csökkenteni az autofágoszómák és autoliszoszómák számát és intenzitását az OGD PC12 sejtekben. A fentiek azt jelzik, hogy az NMN képes gátolni az OGD által indukált autofágiát a PC12 sejtekben.
Összefoglalva, ez arra utal, hogy egy bizonyos dózisú NMN ellensúlyozni tudja az OGD által indukált autofágikus károsodást a PC12 sejtekben, ezáltal sejtvédő hatást fejt ki, és ez a védőhatás az mTOR-ral kapcsolatos útvonalakhoz kapcsolódhat. Ez a tanulmány bizonyos célreferenciát nyújthat az OGD által indukált autofágikus károsodás NMN általi megelőzéséhez és kezeléséhez, és laboratóriumi adatokat halmozhat fel a természetes vegyület NMN fejlesztéséhez.
