Con el desarrollo de la ciencia y la tecnología y los cambios en la demanda del mercado, el desarrollo y la aplicación de nuevos ingredientes alimentarios son cada vez más frecuentes. Las "Medidas administrativas para la revisión de la seguridad de los nuevos ingredientes alimentarios" de China dejan claro que los nuevos ingredientes alimentarios se refieren a los siguientes artículos que no tienen hábitos de consumo tradicionales en China:
(i) Animales, plantas y microorganismos;
(ii) Componentes aislados de animales, plantas y microorganismos;
(iii) Ingredientes alimentarios cuya estructura original ha sido modificada;
(iv) Otros ingredientes alimentarios de nuevo desarrollo, la evaluación de la seguridad y los procedimientos de aprobación de los cuales deberán seguir estrictamente las disposiciones de las Medidas Administrativas para la Revisión de la Seguridad de Nuevos Ingredientes Alimentarios. Entre ellos, la "terminación de la revisión" como una de las conclusiones de la revisión de nuevos ingredientes alimentarios, que implica una variedad de circunstancias específicas, la red de socios de alimentos de acuerdo con la Comisión Nacional de Salud emitió la terminación de la revisión de nuevos ingredientes alimentarios resume la "terminación de la revisión" de las diferentes circunstancias que pueden estar involucrados, para los negocios Para referencia de las empresas.
Circunstancias clasificadas como gestión común de los alimentos (33 tipos)
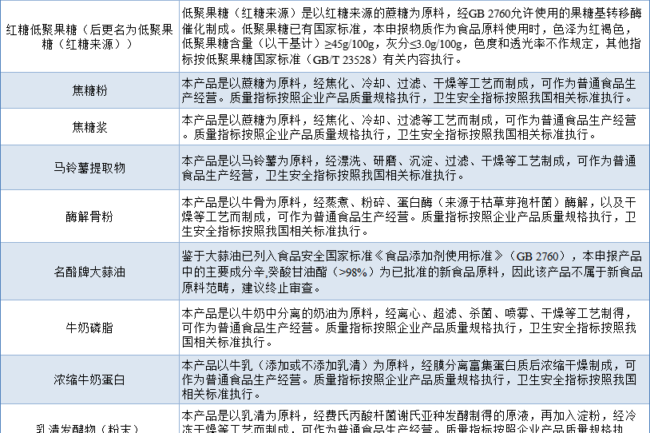
Uno de los casos de finalización de la revisión para las sustancias que deben declararse como nuevos ingredientes alimentarios se categoriza como gestión de alimentos comunes, que incluye principalmente que las materias primas puedan verificarse como alimentos comunes, o tengan una equivalencia sustancial con alimentos comunes existentes, y puedan tener ya normas nacionales relevantes, o productos con un largo historial de consumo. Estos ingredientes pueden producirse y venderse legalmente como alimentos comunes, o pueden utilizarse como ingredientes alimentarios en una amplia gama de productos alimenticios.
Equivalencia sustancial con nuevos ingredientes alimentarios aprobados (24 casos)
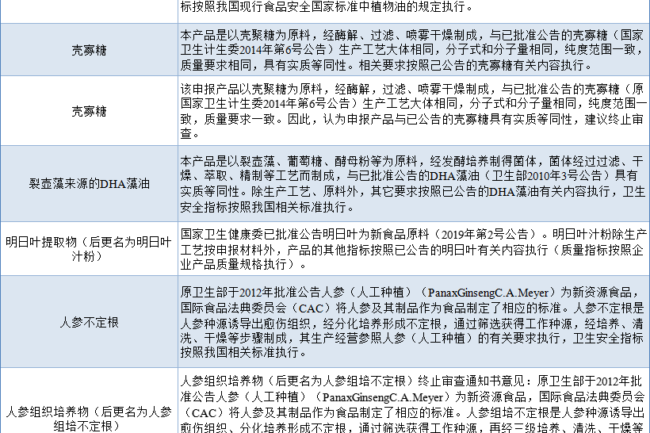
La sustancia que se va a declarar como nuevo ingrediente alimentario coincide con el nuevo ingrediente alimentario anunciado en cuanto al origen de la especie, las propiedades biológicas, los componentes principales, las partes comestibles, la cantidad de uso, el ámbito de aplicación y la población de aplicación, etc. El proceso y los requisitos de calidad adoptados son básicamente los mismos, lo que indica que ambos son sustancialmente equivalentes en términos de seguridad. En este caso, la materia prima se aplicará de acuerdo con las normas de gestión de los nuevos ingredientes alimentarios aprobados, y su uso deberá ajustarse estrictamente al contenido del anuncio y a las normas pertinentes.
Circunstancias que deben gestionarse como especialidad alimentaria local (11 tipos)
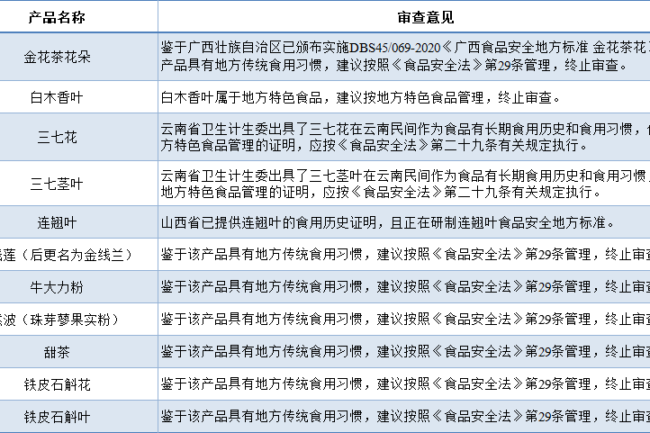
Para algunos ingredientes alimentarios con hábitos de consumo tradicionales distintivos dentro de regiones específicas y reconocidos por las autoridades locales reguladoras de la seguridad alimentaria, incluso si no se consumen comúnmente en todo el país, pueden incluirse en la terminación del catálogo de revisión debido a sus características locales únicas y transferirse a la gestión especial de alimentos con características locales. Esto significa que estos ingredientes pueden utilizarse directamente como ingredientes alimentarios legítimos dentro de la provincia, y los fabricantes de alimentos provinciales deben fabricar sus productos cumpliendo estrictamente las normas locales provinciales de seguridad alimentaria. Si las empresas de otras provincias planean utilizar tales características locales de las materias primas, puede haber adaptabilidad reglamentaria y los riesgos de seguridad, se recomienda comunicarse activamente con las autoridades reguladoras locales de seguridad alimentaria para obtener orientación profesional y la aprobación, para garantizar que el proceso de aplicación transregional de las leyes y reglamentos nacionales y las normas de seguridad alimentaria, para proteger los derechos e intereses de los consumidores y el desarrollo normalizado del mercado.
Gestión como sustancias homólogas medicinales y alimentarias (4 tipos)
En China, los medicamentos y alimentos con el mismo origen se refieren a aquellas sustancias tradicionales que son tanto hierbas chinas como alimentos. Si la sustancia que se va a declarar como nuevo ingrediente alimentario posee el atributo de ser homóloga a la medicina y al alimento, o es sustancialmente equivalente a la sustancia de la lista publicada de sustancias homólogas, el departamento revisor puede poner fin a la revisión del nuevo ingrediente alimentario de acuerdo con las regulaciones pertinentes y gestionarlo directamente como sustancia de origen homólogo a la medicina y al alimento.

Otros casos de cese de revisión (1 tipo)
Además, existen algunas otras circunstancias especiales para poner fin a la revisión de las sustancias que deben declararse como nuevos ingredientes alimentarios, como haber sido incluidas en la Farmacopea con una clara actividad farmacológica, lo que puede dejar claro que la sustancia no es un ingrediente alimentario.

En el proceso de aprobación de nuevos ingredientes alimentarios, la "terminación de la revisión" no significa el final, sino que es una vía indirecta para que las empresas obtengan la aprobación. Aunque no esté "recomendada para aprobación", si la materia prima declarada es sustancialmente equivalente a ingredientes alimentarios existentes, o tiene un largo historial de consumo y es adecuada para ser incluida en la gestión de alimentos generales o alimentos locales especializados, etc., puede pasar el procedimiento de "terminación de examen" y ser clasificada en las categorías correspondientes, como sustancialmente equivalente a nuevos ingredientes alimentarios existentes, o con un largo historial de consumo y adecuada para ser incluida en la gestión de alimentos generales o alimentos locales especializados. Todos ellos pueden pasar el procedimiento de "terminación de examen" y ser clasificados en las categorías correspondientes, tales como sustancialmente equivalentes a nuevos materiales alimentarios existentes, gestionados como alimentos generales, gestionados como alimentos de especialidad local o alimentos con origen medicinal, etc., y entrar legalmente en la circulación del mercado.
Por lo tanto, no importa a través de la "recomendación de aprobación" regular o a través del mecanismo de "finalización de la revisión", las empresas pueden obtener la calificación de acceso al mercado de nuevos ingredientes alimentarios, lo que proporciona a las empresas más opciones y flexibilidad en el desarrollo de productos y la expansión del mercado.
