Erforschung des Wirkmechanismus von Emodin bei der Behandlung von sepsisbedingter akuter Nierenschädigung auf der Grundlage von Data Mining und experimenteller Überprüfung
Sepsis ist eine lebensbedrohliche Organfunktionsstörung, die durch ein Ungleichgewicht in der Reaktion des Wirts auf eine Infektion verursacht wird. Die Nieren sind eines der am häufigsten betroffenen Organe bei einer Sepsis, und die sepsisassoziierte akute Nierenschädigung (SA-AKI) ist oft die direkte Todesursache bei Sepsispatienten, mit einer hohen Sterblichkeitsrate, die die klinischen Ärzte vor nie dagewesene Herausforderungen stellt. Die AKI bleibt bestehen und erhöht das potenzielle Risiko einer chronischen Nierenerkrankung (CKD). Bei überlebenden Patienten kommt es oft unweigerlich zu einer Nierenerkrankung im Endstadium (ESRD), was eine ernsthafte Bedrohung für ihre Lebensqualität und Sicherheit darstellt.
Leider sind die derzeitigen Möglichkeiten zur Vorbeugung und Behandlung der SA-AKI sehr begrenzt. Für eine aktive, auf Flüssigkeit basierende Therapie gibt es keine zuverlässige evidenzbasierte Medizin, und sie kann sogar schädlich sein. Der Einsatz vasoaktiver Medikamente zur Aufrechterhaltung des Blutdrucks erfordert ein Gleichgewicht zwischen dem großen Kreislauf und der Mikrozirkulation, und es gibt keinen Konsens darüber, wie hoch der Zielblutdruck sein sollte, um das Auftreten einer AKI zu verhindern. Wenn die renale Prävention versagt, muss eine Nierenersatztherapie (RRT) zur Behandlung eingesetzt werden, aber der optimale Zeitpunkt und die Methode der RRT-Intervention sind nicht klar. Wenn SA-AKI-Patienten überleben, erholt sich zwar die Nierenfunktion der meisten Patienten, aber es ist wenig über die Mechanismen der Nierenreparatur oder des Versagens der Nierenfunktionsreparatur bekannt, und das lebenslange Risiko einer Progression zu CKD und ESRD ist höher. Bislang gibt es kein eindeutiges und zuverlässiges Medikament zur Behandlung der AKI. Die konventionellen klinischen Behandlungsmaßnahmen bestehen hauptsächlich aus Nierenersatz und einer umfassenden symptomatischen Behandlung. Die Wiederherstellung der Nierenfunktion hängt von der zuverlässigen Unterstützung der Niere selbst im Körper als Ganzes ab. Die Erforschung von Medikamenten oder Maßnahmen, die eine SA-AKI frühzeitig und wirksam verhindern oder behandeln, das Auftreten einer chronischen Nierenerkrankung vermeiden oder die Nierenreparatur fördern können, ist daher von großem klinischen Wert für die Senkung der Sterblichkeitsrate von Sepsispatienten und die Verbesserung der Lebensqualität der überlebenden Patienten.
Emodin ist eine natürliche Verbindung, die aus chinesischen Kräutern wie Rhabarber und Polygonum cuspidatum extrahiert wird und verschiedene pharmakologische Wirkungen wie entzündungshemmende, antivirale und tumorhemmende Eigenschaften hat. Frühere Studien haben bestätigt, dass Emodin eine schützende Wirkung auf Sepsis-Patienten hat. Neuere Studien haben gezeigt, dass Emodin eine schützende Wirkung gegen Schäden hat, die durch oxidativen Stress, Entzündungen und Zellapoptose verursacht werden. Es ist jedoch noch unklar, ob Emodin die Prognose von SA-AKI-Patienten verbessern kann. In dieser Studie werden die Schlüsselgene, die an der Pathogenese von SA-AKI beteiligt sind, mit Hilfe von biowissenschaftlichen Datenbanken erforscht und die entzündlichen Signalwege, die an diesen Schlüsselgenen beteiligt sind, analysiert. Darüber hinaus wurden Tierversuche durchgeführt, um zu untersuchen, ob Emodin den Entzündungsweg von SA-AKI sowie seine schützende Wirkung und den Mechanismus bei SA-AKI-Ratten beeinflusst, was neue Ideen für die Prävention und Behandlung liefert.

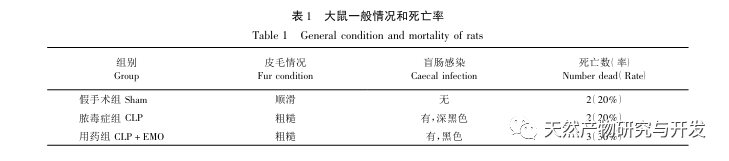
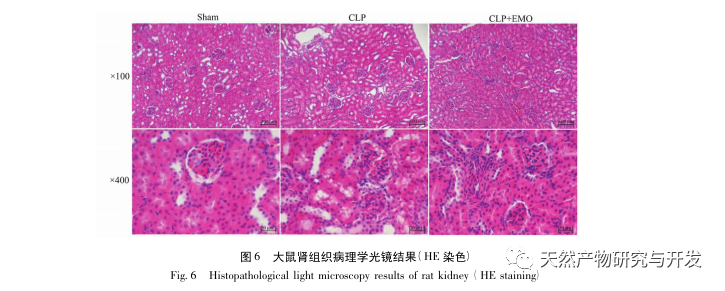


Die Forschung hat gezeigt, dass die Pathogenese der SA-AKI multifaktoriell und komplex ist und eine Wechselwirkung zwischen Entzündung, Mikrozirkulationsstörung und metabolischer Reprogrammierung beinhaltet. Die Pathophysiologie umfasst die Schädigung und Funktionsstörung verschiedener Zelltypen. Bei der Sepsis setzen Bakterien Endotoxine oder endotoxinähnliche Substanzen frei, die Entzündungszellen wie Neutrophile, Monozyten und Endothelzellen im Körper aktivieren und eine große Menge an körpereigenen Entzündungsmediatoren in den Blutkreislauf freisetzen. Dies führt einerseits zu einer Schädigung mehrerer Organe, einschließlich der Nieren, und aktiviert andererseits weitere Entzündungszellen, die sich an der Krankheit beteiligen und eine bösartige Reaktion des Immunsystems auslösen. Im SD-Rattenmodell der durch Lipopolysaccharid (LPS) induzierten SA-AKI lindert Nerolidol die SA-AKI durch Hemmung der NF-κ B- und Toll like receptor 4 (TLR4)-Signalwege. Es wurde bestätigt, dass der TLR4/NF-κ B-Signalweg am Prozess der Entzündungsreaktion der Nieren beteiligt ist, und die Hemmung der TLR4/NF-κ B-vermittelten Entzündungsreaktion hat eine schützende Wirkung auf die LPS-induzierte AKI. Es zeigt sich, dass die Entzündungsreaktion ein wichtiger Mechanismus in der Pathogenese der SA-AKI ist, und die Hemmung des Entzündungsreaktionsweges ist eine wichtige Behandlungsoption für Sepsis, die neue Ideen für die klinische Behandlung von SA-AKI-Patienten liefert.
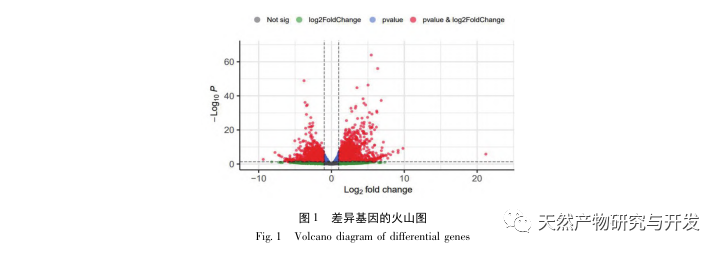
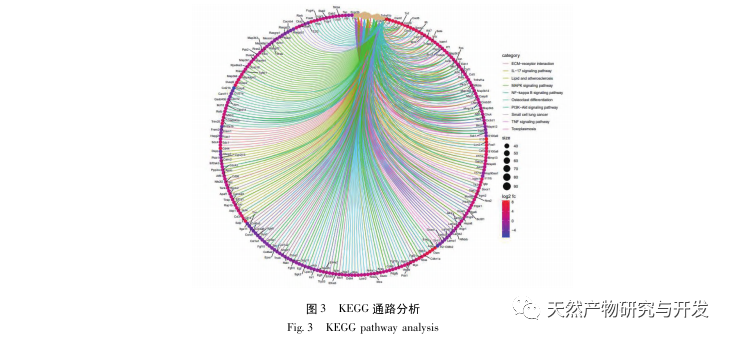
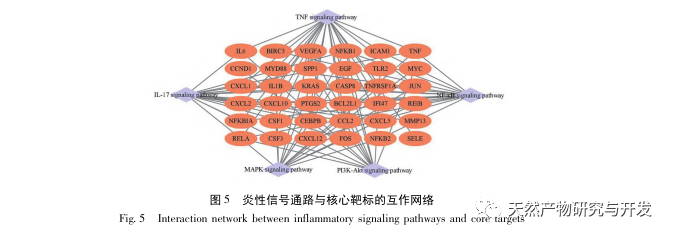
In dieser Studie wurde eine biologische Datenbank verwendet, um 2801 Schlüsselziele zu analysieren, die an der Pathogenese von SA-AKI beteiligt sind. Die KEGG-Analyse dieser Targets ergab insgesamt 5 wichtige Entzündungsreaktions-Signalwege, unter denen der TNF-Signalweg und der IL-17-Signalweg einen hohen Stellenwert einnahmen, und der NF-κ B-Signalweg diente als Drehscheibe für beide Signalwege, die an der Pathogenese der SA-AKI beteiligt sind. Im TNF-Signalweg ist TNF-α nicht nur der wichtigste Upstream-Aktivator des NF-κ B-Signalwegs, sondern dient auch als Downstream-Reaktionsmolekül des NF-κ B-Signalwegs, was darauf hindeutet, dass es den NF-κ B-Signalweg durch positive Rückkopplung fördert und die beiden sich gegenseitig ergänzen. Im IL-17-Signalweg ist IL-17A der wichtigste initiierende Faktor der IL-17-Familie, und Th17-Zellen sind die wichtigsten sezernierenden Zellen. Im CLP-induzierten Modell wurde festgestellt, dass IL-17A in der Bauchhöhle stark exprimiert wird und eine Schlüsselrolle bei der Entzündungsreaktion nach schwerer Sepsis spielt. Die Neutralisierung von IL-17A in der Bauchhöhle kann die Produktion von pro-inflammatorischen Zytokinen reduzieren. In der Zwischenzeit haben Studien gezeigt, dass der Toll-like-Rezeptor 9 (TLR9) in dendritischen Zellen (DCs) eine Schlüsselrolle bei der Entwicklung von SA-AKI spielen kann, indem er die Produktion von IL-17A durch Gamma-Delta-T-Zellen vermittelt; andere Studien haben gezeigt, dass das Ausschalten von IL-17A SA-AKI verhindern kann. Die obigen Ausführungen deuten darauf hin, dass TNF-α und IL-17A pro-inflammatorische Faktoren bei der Sepsis sind, und dass der TNF-Signalweg und der IL-17-Signalweg weitgehend an der Entstehung und Entwicklung der Sepsis beteiligt sind, was mit den Ergebnissen der Datenanalyse übereinstimmt.
Es wurden zahlreiche Studien zur Behandlung von Sepsis mit Emodin durchgeführt, die sich hauptsächlich auf Gehirn, Blut, Herz, Darm und Lungengewebe konzentrierten. Bei der Sepsis-assoziierten Enzephalopathie (SAE) kann Emodin die kognitiven Beeinträchtigungen und pathologischen Schäden verbessern und die CLP-induzierte Entzündung bei Mäusen durch eine Hochregulierung der BDNF/TrkB-Signalisierung hemmen. Im Blutsystem reguliert Emodin das P-Selektin, verbessert die Thrombozytenzahl und die Aggregationsfähigkeit im Spätstadium der Sepsis und steigert die Aktivität der endogenen Gerinnungsfaktoren und die Fibrinogenfunktion, wodurch es entzündungshemmende Wirkungen entfaltet. Bei septischer Kardiomyopathie wurde festgestellt, dass Emodin die kardiale Dysfunktion rückgängig machen und den Zustand des Herzmuskels bei septischen Ratten verbessern kann, was möglicherweise mit seiner Hemmung der Inflammasom-Aktivierung zusammenhängt. Bei durch Sepsis verursachten Darmverletzungen kann Emodin die Schädigung der Darmschleimhaut verbessern, indem es den Gehalt an Entzündungsfaktoren und Markern für oxidativen Stress senkt, und sein Wirkmechanismus könnte mit dem VDR/Nrf2/HO-1-Signalweg zusammenhängen; durch die Erhöhung der Expression des Tight-Junction-Proteins (TJ) schützt es die Integrität der Darmbarriere und hemmt die Durchlässigkeit der Darmbarriere. Neben der Verbesserung der Entzündungsreaktion und der Barrierefunktion des Darms kann Emodin auch die Verdrängung von Escherichia coli verhindern, die Ausbreitung und Übertragung von Bakterien verhindern und die durch Bakterien verursachten Sekundärschäden reduzieren. Bei sepsisbedingten akuten Lungenverletzungen kann Emodin die NF-κ-B- und HMGB1-Signalwege hemmen und dadurch den oxidativen Stress und die Entzündungsreaktion in der Lunge verringern. Eine andere Studie über die Lunge basiert auf dem Autophagie-Stoffwechselweg, und die Intervention von Emodin kann das Fortschreiten der akuten Lungenschädigung wirksam verhindern. Darüber hinaus haben andere Studien gezeigt, dass Emodin das Lungengewebeödem bei einer durch Sepsis verursachten akuten Lungenverletzung wirksam lindern kann, indem es Aquaporin (AQP), TJ, Entzündungsfaktoren und die Apoptose der Lungenzellen reguliert. Über die Wirkung von Emodin auf SA-AKI wurde bisher noch nicht berichtet. In dieser Studie wurde festgestellt, dass mit Emodin behandelte CLP-Modell-Ratten eine verringerte Expression von TNF-α, IL-17 und IFN-γ in ELISA-Ergebnissen aufwiesen, was mit der hemmenden Wirkung von Emodin auf Sepsis-Entzündungen übereinstimmt.
Die gleiche Wirkung von Emodin auf die Th17/Treg-Entzündungsachse wurde auch aufgeklärt. In der Studie über akute Pankreatitis wurde festgestellt, dass Emodin die Immunreaktion bei schwerer akuter Pankreatitis hemmt, indem es das Verhältnis von IFN-γ/IL-17 reguliert und dadurch die Dysfunktion der Darmbarriere lindert. Und diese Studie ergab, dass Emodin bei SA-AKI auch die Expression von IL-17A verringern und die Entzündungsreaktion verbessern kann.
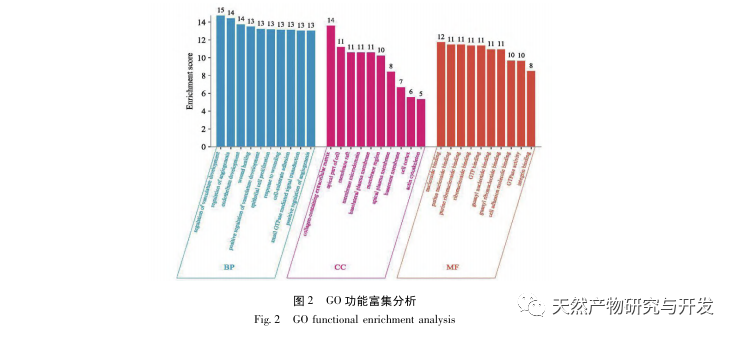
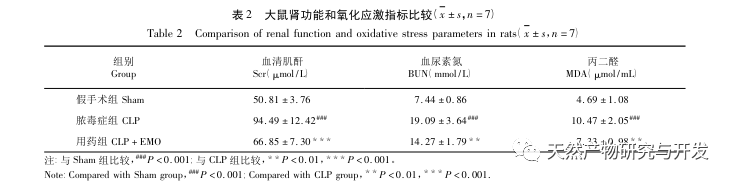
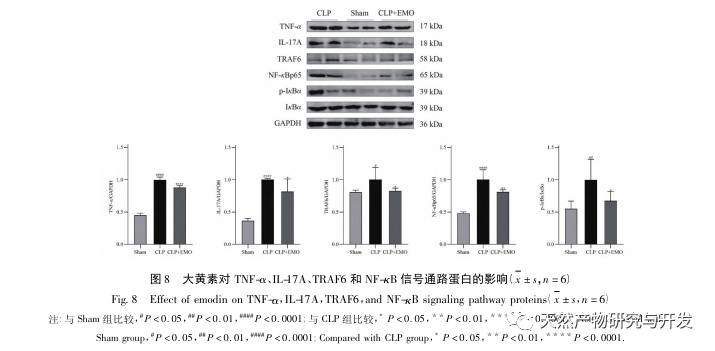
Zusammenfassend wurden in dieser Studie durch Data-Mining 2801 Schlüsselgene identifiziert, die an der Pathogenese von Emodin beteiligt sind. Die GO-Analyse der biologischen Prozesse deutet darauf hin, dass die biologischen Funktionen dieser Ziele hauptsächlich die Membransignaltransduktion, die Gefäßregulierung und die Wundheilung betreffen. Die Analyse der Anreicherung von KEGG-Signalwegen zeigte, dass TNF, IL-17, PI3K Akt, NF-κ B und MAPK-Signalwege in entzündungsbezogenen Signalwegen angereichert waren. Die experimentelle Überprüfung zeigte, dass die Behandlung mit Emodin die Nierenfunktion bei SA-AKI verbesserte und die Werte von oxidativem Stress (MDA) und entzündlichen Zytokinen (TNF-α, IL-17 und IFN-γ) sanken. Die Proteinexpression von IL-17A, TNF-α, TRAF6, NF-κ Bp65 und das Phosphorylierungsniveau von I-κ B-α waren im Vergleich zur CLP-Gruppe deutlich reduziert, was mit den Ergebnissen der Datenanalyse übereinstimmt. Es wird vorgeschlagen, dass Emodin SA-AKI bei Ratten verbessern kann, was mit den IL-17/NF - κ B und TNF/NF - κ B Signalwegen zusammenhängen kann.
