Undersøgelse af den regulerende effekt af honokiol på HIF-1 α - VEGF-stien i PC12-celler baseret på netværksfarmakologi og celleeksperimenter
Magnolia officinalis, som er en Qi-regulerende medicin, der kan tørre fugt, fjerne slim og lindre overskydende Qi, er blevet grundigt undersøgt både nationalt og internationalt i de senere år. Hovedkomponenterne i Magnolia officinalis og magnolol er en klasse af meget bioaktive fenolforbindelser med minimal toksicitet og farmakologiske virkninger som antiinflammatorisk, smertestillende, antitumor og antipatogene mikroorganismer. Houpo phenol kan trænge ind i centralnervesystemet gennem blod-hjerne-barrieren og have en direkte indvirkning på nervevæv, hvilket gør det til et lovende lægemiddel mod neurologiske sygdomme; På den anden side har honokiol også terapeutiske virkninger på en række kræftformer, såsom mavekræft, lungekræft, leverkræft og kræft i bugspytkirtlen.
Aktivering af udtrykket af HIF-1 α kan fremme angiogenese, neurobeskyttelse og neural reparation og derved behandle cerebrale iskæmiske rotter. Derudover er HIF-1 også en nøglefaktor til regulering af tumorangiogenese, og magnolol hæmmer udtrykket af HIF-vej og hypoxi-medierede proangiogene gener i de fleste tumorer og iskæmiske sygdomme i nethinden. Ovenstående undersøgelser indikerer, at regulering af HIF-1 α med magnolol i forskellige tilstande er den vigtigste mekanisme for dets farmakologiske virkninger. Denne undersøgelse tager udgangspunkt i "HIF-1 α" og bruger netværksfarmakologi og eksperimentel verifikation til at udforske de regulatoriske virkninger af honokiol på HIF-1 α - VEGF-vejen i PC12-celler under normoxiske og hypoxiske forhold.
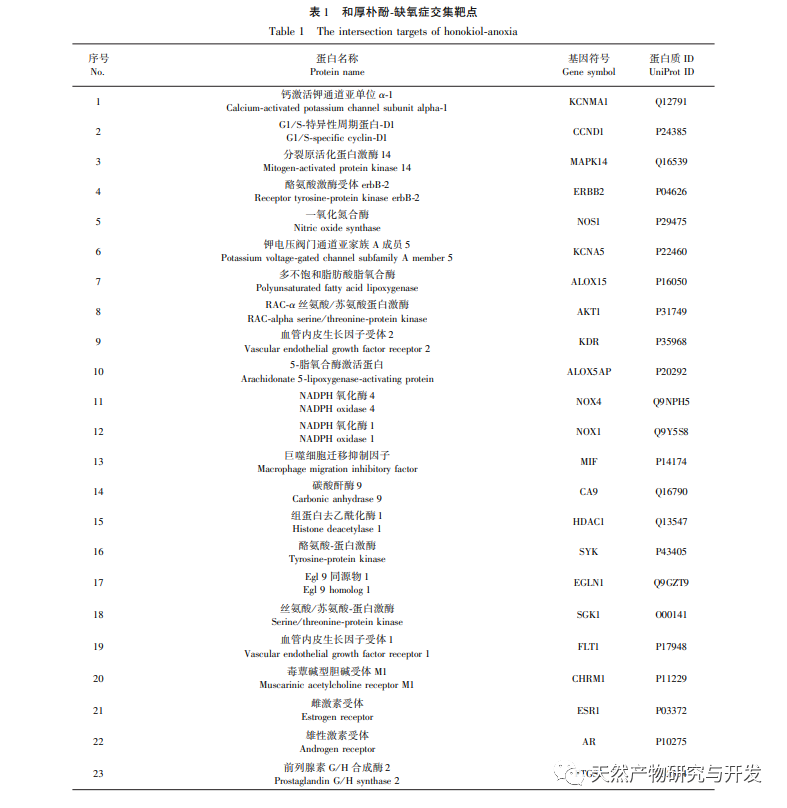
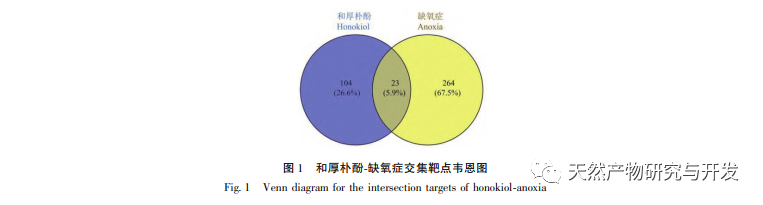
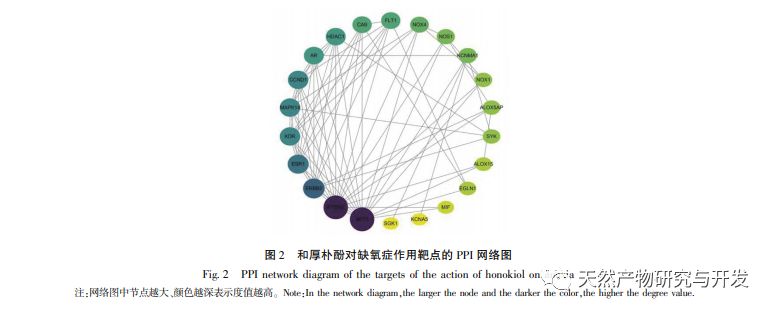
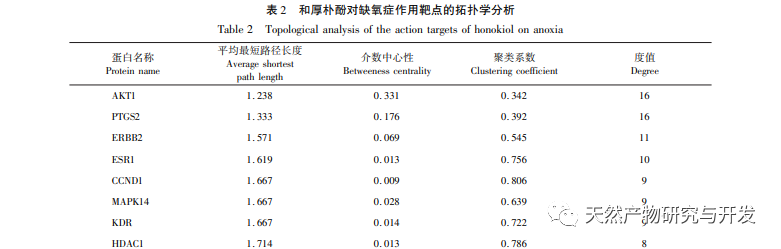
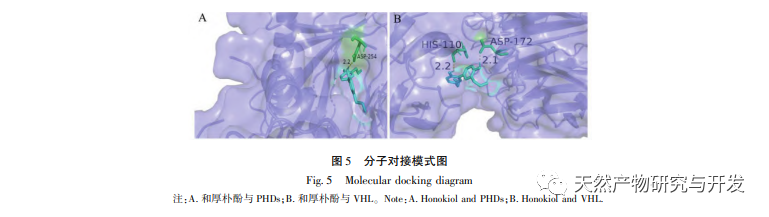
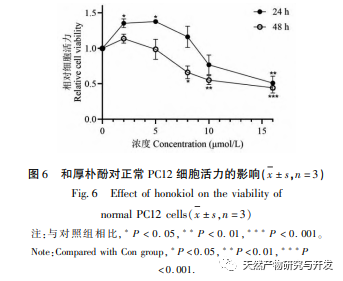
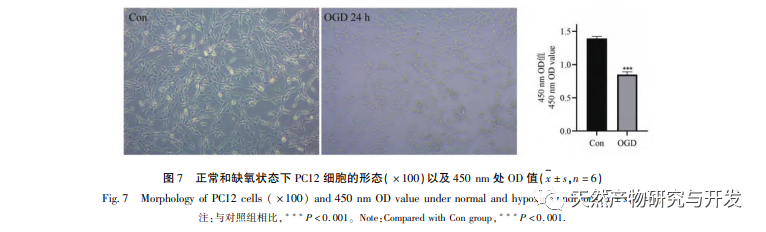
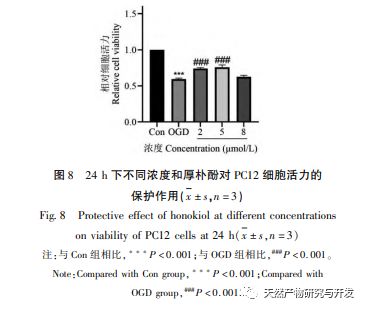
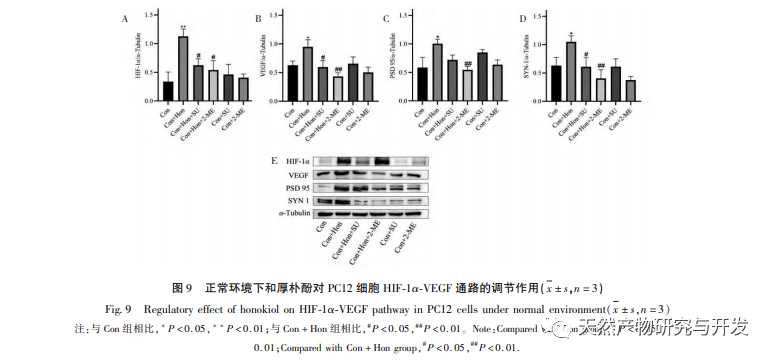
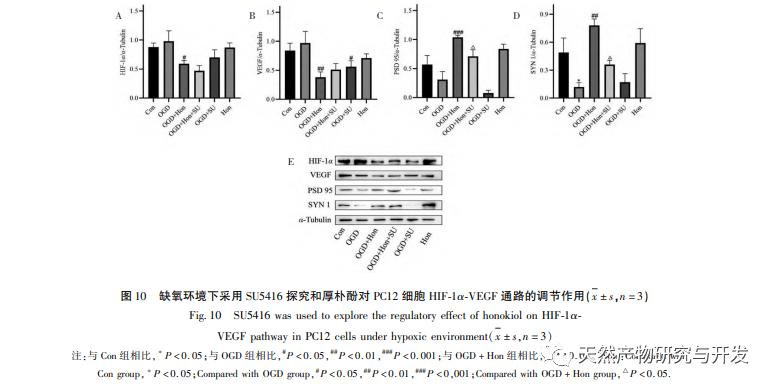
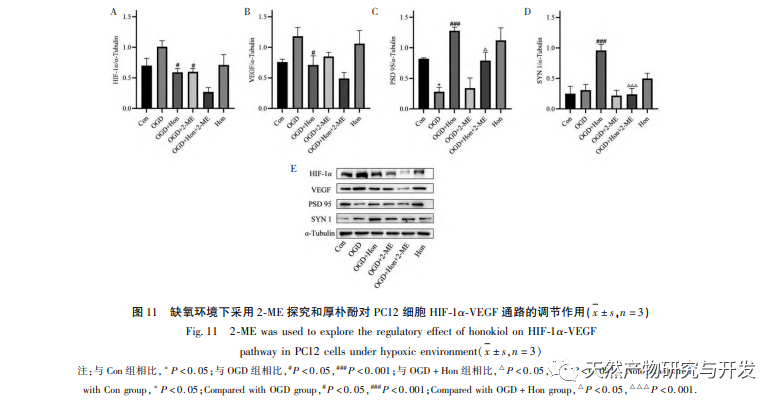 Under normoxiske forhold er udtrykket af HIF-1 α og VEGF lavt, men administration af magnolol fremmer signifikant udtrykket af HIF-1 α og VEGF-proteiner; Under hypoxiske forhold er HIF-1 α og VEGF stærkt udtrykt, og administration af honokiol hæmmer signifikant udtrykket af HIF-1 α og VEGF. Houpo phenol udviser forskellige regulatoriske virkninger på HIF-1 α og VEGF i forskellige tilstande, hvilket er af stor betydning for at studere dets farmakologiske mekanisme og udvikle dets anvendelse. Med hensyn til hvordan honokiol påvirker dannelsen og nedbrydningen af HIF-1 α, viste de molekylære dockingresultater i denne undersøgelse, at honokiol har god bindingsaktivitet med to nedbrydningsenzymer, PHD'er og VHL. Vi kan dog stadig ikke afklare, om det specifikke nedbrydningsenzym aktiveres eller hæmmes, hvilket også er en retning, der skal undersøges i fremtiden.
Under normoxiske forhold er udtrykket af HIF-1 α og VEGF lavt, men administration af magnolol fremmer signifikant udtrykket af HIF-1 α og VEGF-proteiner; Under hypoxiske forhold er HIF-1 α og VEGF stærkt udtrykt, og administration af honokiol hæmmer signifikant udtrykket af HIF-1 α og VEGF. Houpo phenol udviser forskellige regulatoriske virkninger på HIF-1 α og VEGF i forskellige tilstande, hvilket er af stor betydning for at studere dets farmakologiske mekanisme og udvikle dets anvendelse. Med hensyn til hvordan honokiol påvirker dannelsen og nedbrydningen af HIF-1 α, viste de molekylære dockingresultater i denne undersøgelse, at honokiol har god bindingsaktivitet med to nedbrydningsenzymer, PHD'er og VHL. Vi kan dog stadig ikke afklare, om det specifikke nedbrydningsenzym aktiveres eller hæmmes, hvilket også er en retning, der skal undersøges i fremtiden.
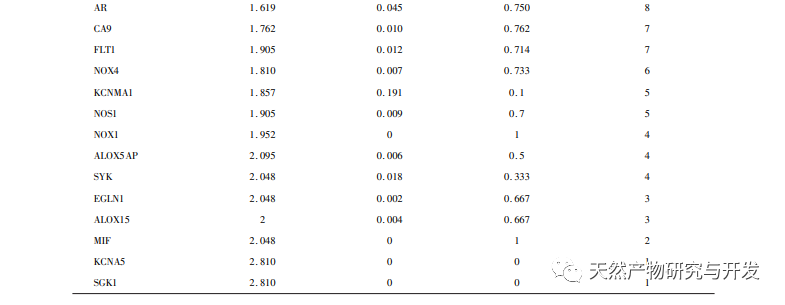
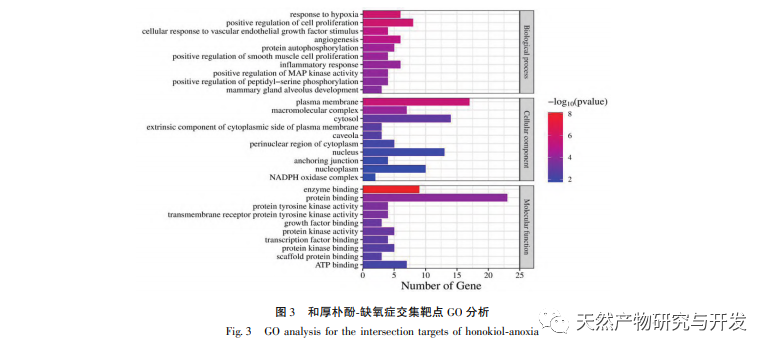
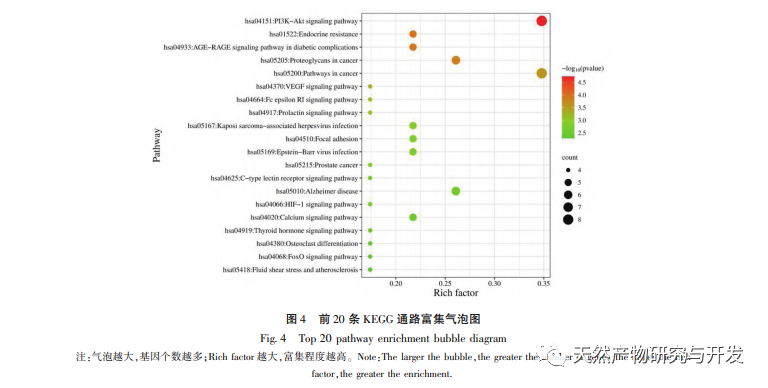
Netværksfarmakologi er en undersøgelse, der udføres ved hjælp af systembiologiske metoder, der kan lette identifikationen af lægemiddelmål og er blevet anvendt i vid udstrækning til forudsigelse af aktive ingredienser og virkningsmekanismer i traditionel kinesisk medicin. For eksempel har forskning opsummeret netværksreguleringsmekanismen for traditionel kinesisk medicin i antidepressiv behandling, og resultaterne viser, at traditionel kinesisk medicin udøver antidepressive virkninger gennem "multi-target multi pathway", regulering af "neuroendokrin immunnetværk" og PI3K Akt-signalvej. I netværksfarmakologiforskningen af traditionel kinesisk medicin anti-tumor er det blevet rapporteret, at traditionel kinesisk medicin udøver anti-tumoreffekter gennem antiinflammatorisk, antiimmunsystem, antiangiogenese, energimetabolisme og andre mekanismer. Derudover har nogle forskere fundet ud af, at traditionel kinesisk medicin fremmer vækst og spredning af nerveceller og hæmmer celleapoptose ved at regulere PI3K Akt-vejen, HIF-1-vejen og TNF-vejen og derved spiller en vis regulerende rolle i hypoxi. Resultaterne af GO-berigelsesanalysen omfatter reaktioner på hypoxi, cellulære reaktioner på vaskulær endotelvækstfaktorstimulering, inflammatoriske reaktioner og andre biologiske processer, som kan være relateret til den komplekse patogenese af hypoxi. Dette indikerer, at honokiol kan gribe ind i forekomsten og udviklingen af sygdomme fra flere niveauer og veje. Resultaterne af KEGG-berigelsesanalysen omfatter HIF-1 pathway, VEGF pathway, PI3K Akt pathway osv. PI3K Akt-stien kan regulere beslægtede proteiner gennem fosforylering og derved fremme cellevækst og hæmme apoptose. HIF-1-vejen kan ændre genekspressionen for at forbedre kroppens iltforsyningskapacitet og øge blodforsyningen for at tilpasse sig iskæmiske og hypoksiske miljøer. VEGF er et downstream-målgen for HIF-1 α. Under hypoksiske forhold kan det stimulere produktionen og stabiliseringen af HIF-1 α og igangsætte transkriptionen af VEGF, hvilket resulterer i øget ekspression af VEGF. Nedenfor vil vi fokusere på at diskutere depression, cerebral iskæmi og tumorsygdomme.
Aktivering af HIF-1 α - VEGF-signalvejen spiller en vigtig rolle i at fremme synaptisk plasticitet og effektivt vende depressionslignende adfærd og hukommelsessvigt i CUMS. Blandt dem er hypoxia inducible factor-1 (HIF-1) en transkriptionsfaktor, der reagerer på hypoxi. Som en cellulær iltreceptor er det en heterodimer, der består af ustabile alfa- og beta-underenheder, som er vidt udbredt i menneskeceller. Undersøgelser har vist, at hypoksisk prækonditionering (HP) kan øge udtrykket af HIF-1 α i hippocampus, den paraventrikulære kerne i hypothalamus og neocortex hos rotter. Der er rapporter om, at intermitterende hypoxi (IH) kan stimulere hippocampus angiogenese og neurogenese og forbedre hjernens hukommelsessvigt. Derfor er HIF-1 α-signalvejen et lovende potentielt mål for behandling af depression. Vascular endothelial growth factor (VEGF) har høj specificitet for endotelceller og har potentiale for neurotrofiske og neurobeskyttende effekter i centralnervesystemet. Forskning har vist, at VEGF påvirker synaptisk plasticitet i neuroner og kan fremme axonal vækst og neurogenese. VEGFR-2 (KDR) er en celleoverfladereceptor for VEGF, som spiller en rolle i indlæring og hukommelse ved at formidle langtidsforbedring, plasticitetsforbedring og kognitiv funktionsforbedring gennem sin receptor VEGFR-2. Sammenfattende er aktivering af HIF-1 α - VEGF-signalvejen en meget undersøgt strategi til forbedring af depressiv adfærd. Derudover kan PI3K Akt-vejen i nerveceller regulere spredning og differentiering af nerveceller og også deltage i regulering af cerebral blodgennemstrømning og fremme neuronal overlevelse, hvilket er tæt forbundet med forekomsten og udviklingen af depression. Patogenesen af depression er relateret til synaptisk plasticitetsforstyrrelse. Ændringer i synaptisk plasticitet er tæt forbundet med udtrykket af synaptiske proteiner. PSD95 er en type postsynaptisk tæt materiale (PSD) proteinfamilie, der kan regulere synaptisk transmission og synaptisk funktion. SYN1 er et specifikt markørprotein for synaptiske vesikler, som kan afspejle antallet, tætheden og fordelingen af synapser. PSD95 og SYN1 spiller en afgørende rolle for at fremme signaltransduktion og synaptisk plasticitet, og nogle antidepressive lægemidler kan forbedre den synaptiske plasticitet betydeligt. Dette stemmer overens med resultaterne i 2.8 og 2.9, hvor honokiol kan øge niveauerne af PSD95- og SYN1-proteiner for at forbedre den synaptiske plasticitet i PC12-celler.
Forbedring af den neurologiske funktion hos rotter med fokal cerebral iskæmi kan være relateret til fremme af udtrykket af HIF-1 α - VEGF-signalvejen og dannelsen af synaptisk plasticitet efter cerebral iskæmi. Forskere har fundet ud af, at mekanismen for hjernebeskyttelse er relateret til den øgede ekspression af HIF-1 α og dens downstream-målgener VEGF og EPO. Mekanismen til forbedring af cerebral iskæmi forårsaget af hypoxi i stor højde er også relateret til opregulering af HIF-1 α-vejen. Aktiveringen af PI3K Akt-vejen kan også forbedre neurologiske underskud og have en neurobeskyttende effekt på rotter med cerebral iskæmi-reperfusionsskade. Derudover spiller HIF-1 α - VEGF-signalvejen en vigtig rolle i forekomsten og udviklingen af tumorer, især i tumorer i centralnervesystemet. Forskning har vist, at honokiol hæmmer spredningen af gliomceller ved at reducere udtrykket af HIF-1 α og dets målgener VEGF og GLUT1. I dyreforsøg har nogle forskere brugt nøgne mus til at etablere en solid tumormodel af humane tyktarmskræftceller. Efter oral administration af magnolol hæmmer det signifikant tumorvækst, og dets mekanisme er relateret til hæmning af HIF-1 α - VEGF-stien og PI3K Akt-stien.
Sammenfattende har magnolol forskellige regulerende virkninger på HIF-1 α - VEGF-signalvejen under normale og hypoksiske miljøer. Houpo phenol kan behandle depression, cerebral iskæmi og tumorsygdomme gennem flere veje og mål, hvilket giver retning for yderligere forskning i mekanismen for Houpo phenol til behandling af disse sygdomme. Derudover blev den forudsagte molekylære dockingvinkel og den gode docking mellem honokiol og HIF-1 α-nedbrydende enzym observeret. Denne undersøgelse vil fortsætte med at udforske, hvordan honokiol påvirker HIF-1 α ved hjælp af molekylærbiologi og andre metoder.
