Virkningerne af polysaccharider fra Atractylodes macrocephala og n-butanol på mitokondrie-autofagi i rotter med miltmangel
Miltmangel er en almindelig syndromtype i differentieringen af organer og indvolde, der normalt manifesteres som afmagring, appetitløshed, epigastrisk smerte, oppustethed, træthed, bleg hudfarve, løs afføring osv. Miltmangel indikerer, at kroppen er i en metabolisk tilstand med lavt energiindhold, især relateret til gastrointestinal dysfunktion. Det er værd at bemærke, at mitokondrier er en vigtig energikilde til gastrointestinal peristaltik i kroppen, idet de producerer energi i form af ATP gennem oxidativ fosforylering og er et vigtigt led i den "miltmedierede transport". Oxidativ skade, næringsstofmangel og andre eksterne stimuli kan let føre til mitokondriel skade. Som reaktion herpå kan værtsceller aktivere autofagi for at fjerne beskadigede mitokondrier og opretholde den cellulære homeostase. Hvis autofagi-funktionen er nedsat, og beskadigede mitokondrier ikke kan fjernes i tide, kan det medføre celledød. Forskning har vist, at der er observeret abnormiteter i mitokondriel autofagi i celler som skeletmuskler, nerver, lever og myokardium hos dyr med miltmangel.
Atractylodes lancea (Thunb.) DC er en flerårig urteagtig plante i Asteraceae-familien, som har den virkning, at den udtørrer fugt og styrker milten. Ifølge den kinesiske farmakopé er kilden rhizomet fra Asteraceae-planten Atractylodes macrocephala eller Atractylodes macrocephala. De vilde ressourcer af Atractylodes macrocephala er hovedsageligt fordelt i Hubei, Xuancheng, Anhui, Wuning, Jiangxi og Hanzhong, Shaanxi, mens de vilde ressourcer af Atractylodes macrocephala hovedsageligt er fordelt i det nordøstlige Kina, Indre Mongoliet, Hebei og andre regioner. Traditionelt mener man, at Atractylodes macrocephala i Maoshan-området i Jiangsu-provinsen har den bedste kvalitet og er en ægte lægeurt. I mange lande som Thailand og Japan bruges Atractylodes macrocephala også ofte til at behandle sygdomme i fordøjelsessystemet. Moderne farmakologiske undersøgelser har vist, at Atractylodes macrocephala kan regulere niveauerne af gastrointestinale hormoner i rotteserum; Atractylodes macrocephala-ekstrakt har en hæmmende effekt på væksten af mavekræftceller (BGC-823 og SGC-7901) og Helicobacter pylori. Atractylodes macrocephala indeholder forskellige typer af kemiske komponenter, herunder flygtige olier, polysaccharider, glykosider og ikke-flygtige stoffer med lav polaritet. Forskerteamet har tidligere fundet ud af, at polysaccharider fra Atractylodes macrocephala og dets n-butanolkomponenter (glykosider) har terapeutiske virkninger på miltmangel. Baseret på dette er dette eksperiment det første, der undersøger mekanismen for Atractylodes macrocephalas effektive komponenter, der regulerer miltmangel ud fra mitokondrie-autofagi, med det formål at lægge grunden til en rationel anvendelse af Atractylodes macrocephala.




 Den kliniske diagnose af miltmangel er generelt baseret på symptomer. Patienter med miltmangel udviser ofte symptomer som nedsat appetit, kedelige mavesmerter, træthed og kolde lemmer. Appetitløshed viser sig som vægttab hos dyr med miltmangel, mavesmerter viser sig som pukkelryg, træthed og svaghed viser sig som sløvhed og let træthed, og frygt for kulde viser sig som sammenklumpning og sammenkrølling. I dette eksperiment viste rotterne tegn på afmagring, pukkelryggethed, slaphed og sammenkrøllethed efter modellering, hvilket bekræftede succesen med den etablerede rotte-model for miltmangel.
Den kliniske diagnose af miltmangel er generelt baseret på symptomer. Patienter med miltmangel udviser ofte symptomer som nedsat appetit, kedelige mavesmerter, træthed og kolde lemmer. Appetitløshed viser sig som vægttab hos dyr med miltmangel, mavesmerter viser sig som pukkelryg, træthed og svaghed viser sig som sløvhed og let træthed, og frygt for kulde viser sig som sammenklumpning og sammenkrølling. I dette eksperiment viste rotterne tegn på afmagring, pukkelryggethed, slaphed og sammenkrøllethed efter modellering, hvilket bekræftede succesen med den etablerede rotte-model for miltmangel.
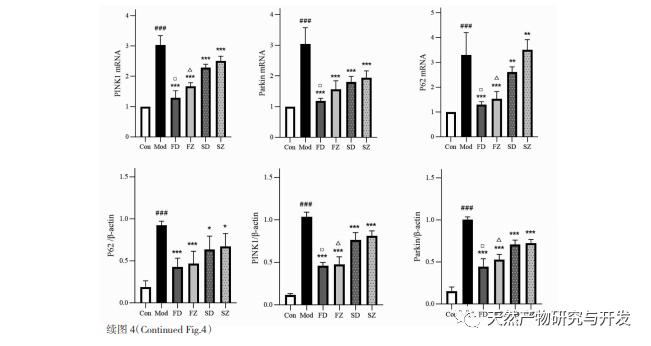
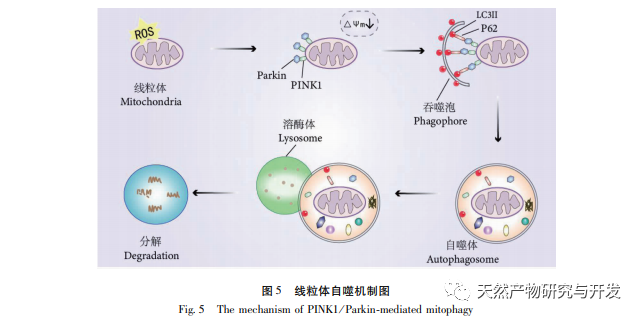
Reguleringsmekanismen for mitokondriel autofagi er kompleks, og flere signalveje kan formidle forskellige typer af autofagiprocesser. PINK1/Parkin-signalvejen er den mest almindelige og velundersøgte signalvej for autofagi i mitokondrier. PINK1 kan normalt ikke påvises i sunde mitokondrier, fordi det spaltes af intramembranale hydrolaser (Parl), når det er kommet ind i mitokondrierne, og derefter fjernes. Som vist i figur 5 blokeres PINK1's adgang til mitokondrierne, når mitokondrierne er beskadigede, på grund af et fald i det indre membranpotentiale, og det ophobes kontinuerligt på mitokondriernes ydre membran og rekrutterer parkin til de beskadigede mitokondrier. Parkin er en E3 ubiquitin-proteinligase, der kan ubiquitinere beskadigede mitokondriemembranproteiner, når den aktiveres af PINK1. Det genkendes af det selektive autofagi-adaptorprotein p62 og forbindes derefter med det autofagi-relaterede protein mikrotubuli-associeret protein 1 let kæde 3 (LC3) på autofagosom-membranen, hvilket igangsætter autofagi og i sidste ende nedbryder beskadigede mitokondrier. Denne undersøgelse viste, at mRNA- og proteinniveauerne af PINK1 og Parkin steg markant i modelgruppen, hvilket indikerer tilstedeværelsen af beskadigede mitokondrier. PINK1/Parkin-stien er blevet aktiveret, men beskadigede mitokondrier er muligvis ikke blevet nedbrudt af autofagi på grund af dysfunktion. Efter behandling med polysaccharider fra Atractylodes macrocephala og n-butanol faldt mRNA- og proteinniveauerne af PINK1 og Parkin i hver gruppe af rotter, hvilket indikerer, at nogle beskadigede mitokondrier er blevet nedbrudt og fjernet ved autofagi.
Mitokondriel autofagi er tæt reguleret af mange autofagirelaterede proteiner, så udtrykket af visse nøgleproteiner bruges ofte til at bestemme styrken af autofagi, hvoraf LC3 og p62 er mere kritiske. Når der ikke forekommer autofagi, findes det meste LC3 i cytoplasmaet i form af LC3I. Når autofagi opstår, gennemgår LC3 ubiquitinationsmodifikation og binder sig til phosphatidylethanolamin på overfladen af autofagosomer for at danne LC3II, der ligger på membranoverfladen af autofagosomer. Derfor er forekomsten af LC3II ofte en vigtig markør for autofagi. Som et vigtigt selektivt autofagi-adapterprotein kan p62 binde sig til LC3II og fungere som et substrat for selektiv autofagi. Når lysosomer og autofagosomer er i bindingsfasen, kan p62 fungere som en donor for lysosomer og lede autofagosomer til at binde sig til dem og danne autolysosomer. Til sidst nedbrydes substraterne af proteolytiske enzymer i lysosomerne, og p62 nedbrydes efterfølgende sammen med dem. Autofagi sker normalt med et fald i p62. Denne undersøgelse observerede, at udtrykket af LC3II-protein og LC3II/I-forholdet i modelgruppen var signifikant lavere end i den blanke gruppe, hvilket indikerer, at autofagosomdannelse i gastriske antrale vævsceller er begrænset under miltmangel. Stigningen i mRNA- og proteinniveauet for p62 indikerer en hæmning af autofagiaktiviteten. Efter indgivelse af polysaccharider fra Atractylodes macrocephala, Atractylodes macrocephala og n-butanol blev omdannelsen af LC3 Ⅰ til LC3II i hver gruppe af rotter forbedret, og niveauerne af p62 mRNA og protein faldt, hvilket indikerer en stigning i autofagi-niveauerne. I overensstemmelse med resultaterne af transmissionselektronmikroskopien var mitokondriestrukturen hos rotterne i modelgruppen alvorligt beskadiget, og der blev ikke observeret nogen autofagisk struktur, hvilket indikerer, at nedsat autofagifunktion kan have ført til ophobning af beskadigede mitokondrier. Efter administrationen blev den strukturelle mitokondrieskade i hver gruppe af rotter reduceret, og antallet af autofagiske lysosomer steg. Derfor mener vi, at miltmangel fører til nedsat mitokondriel autofagi-funktion i rotternes gastriske antralvæv, mens indgift af polysaccharider fra Atractylodes macrocephala og Atractylodes macrocephala med n-butanol fremmer autofagi.
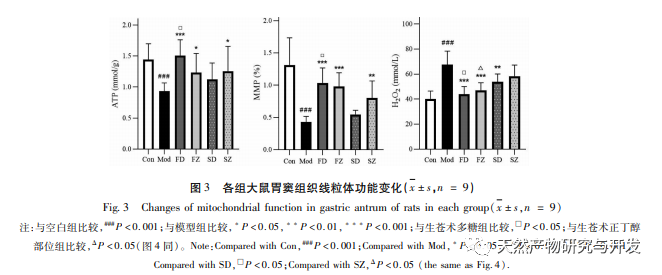
Obstruktion af mitokondriel autofagi ledsages normalt af produktion af reaktive iltarter (ROS), og en stigning i intracellulære ROS-niveauer vil fremkalde oxidativ stress. Oxidativt stress angriber mitokondriemembranen, hvilket fører til et fald i membranpotentialet, mitokondriebeskadigelse og funktionsnedsættelse, som igen udløser energigenereringsdefekter og en stigning i ROS, hvilket skaber en ond cirkel. Beskadigede og dysfunktionelle mitokondrier ryddes selektivt af mitokondriel autofagi, som hjælper med at reducere ROS-produktionen og forhindre oxidativ skade på normale celler. H2O2 er den vigtigste endogene ROS i celler, som kan produceres af næsten alle oxidative stressfaktorer og frit kan diffundere ind og ud af celler, hvilket forårsager en ubalance i det oxidative antioxidantsystem. Derfor evaluerer dette eksperiment indirekte ROS-niveauer ved at detektere H2O2-indhold. Forskningsresultaterne viste, at niveauerne af H2O2, membranpotentiale og ATP i rotter med miltmangel faldt, hvilket indikerer nedsat mitokondriefunktion. Behandlingen med polysaccharider fra Atractylodes macrocephala og n-butanol forbedrede mitokondriefunktionen betydeligt, hvilket kan opnås ved at fremme mitokondriel autofagi og øge clearingen af beskadigede mitokondrier.
Sammenfattende spekulerer vi i, at polysacchariderne og n-butanolkomponenterne i Atractylodes macrocephala kan regulere miltmangel ved at forbedre autofagi-forstyrrelser i mave-tarmvævet og genoprette mitokondriefunktionen. Desuden er polysacchariderne og n-butanolkomponenterne efter omrøring med klid betydeligt mere effektive end det rå produkt.
