Udforskning af Morinda officinalis' mekanisme mod aterosklerose baseret på netværksfarmakologi og eksperimentel verifikation
Aterosklerose (AS) er en almindelig kronisk hjerte-kar-sygdom, der er karakteriseret ved dannelsen af aterosklerotisk plak eller fibrøst plak i intima af store og midterste arterier. Infiltration af lipider i arterieintima er blevet den vigtigste patogenese ved aterosklerose. Makrofager samlet i intima og medier opsluger en stor mængde oxideret lipoprotein med lav densitet (ox LDL) gennem scavenger-receptorer på cellemembranen for at danne skumceller, som får cellerne til at frigive et stort antal proinflammatoriske faktorer og matrixmetalloproteinaser i det intercellulære rum, fremmer ophobning af plak i arterievæggen for at øge, derefter blive til ustabil plak og til sidst udvikle sig til myokardieinfarkt. Men at forsinke udviklingen af AS effektivt har altid været en af de udfordringer, der bekymrer det akademiske samfund. I de senere år har det populære nye lægemiddel og spiselige produkt, Morinda officinalis, vist sig at have gode effekter i forhold til at regulere blodlipider og forbedre aterosklerose.
Morinda citrifolia, også kendt som noni, er en plante af Euphorbia-slægten i Rubiaceae-familien. Den har farmakologiske virkninger som antiinflammatorisk, antioxidant og lipidsænkende. Ifølge traditionel kinesisk medicin har Morinda officinalis en sur og sød smag, en afbalanceret medicinsk egenskab og har den virkning, at den nærer nyreessensen, afbalancerer yin og yang og forsinker aldring. Det kan effektivt forebygge kardiovaskulære og cerebrovaskulære sygdomme. Den specifikke mekanisme bag Hai Ba Ji i behandlingen af AS er dog stadig uklar. I betragtning af den komplekse kemiske sammensætning af Morinda officinalis, som hovedsageligt består af anthraquinoner, flavonoider, phenylpropanoider, phenolsyrer og andre komponenter, i overensstemmelse med multikomponent- og multimålkarakteristika for traditionel kinesisk medicin, kan netværksfarmakologi bruges til klart at belyse den molekylære mekanisme for de farmakologiske virkninger af Morinda officinalis. I de senere år er netværksfarmakologi blevet en ny disciplin, der integrerer computervidenskab, bioinformatik og datamining. Den konstruerer et "lægemiddelaktiv ingrediens sygdomsmål sygdom"-netværk og forklarer dets biologiske funktioner, hvilket gør det muligt for folk at få en klarere forståelse af mekanismerne og mekanismerne for lægemiddelbehandling af sygdomme. Denne undersøgelse er baseret på de forskellige aktive ingredienser og rige mål for Morinda officinalis og har til hensigt at bruge netværksfarmakologimetoder til at forudsige og analysere mål, biologiske processer og signalveje for Morinda officinalis i behandlingen af AS. Samtidig vil in vitro-eksperimenter blive brugt til verifikation for at skabe et farmakologisk grundlag for lægemiddeludvikling og behandling af AS.
 åreforkalkning
åreforkalkning



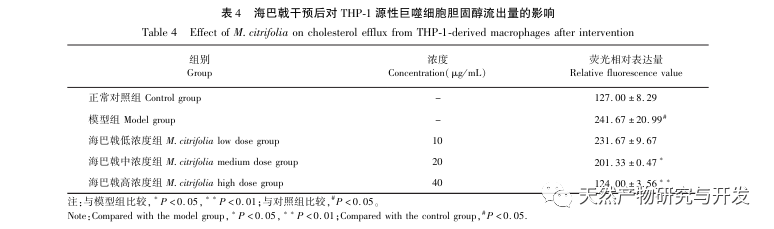
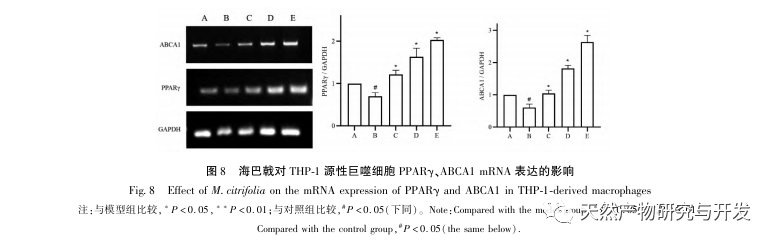
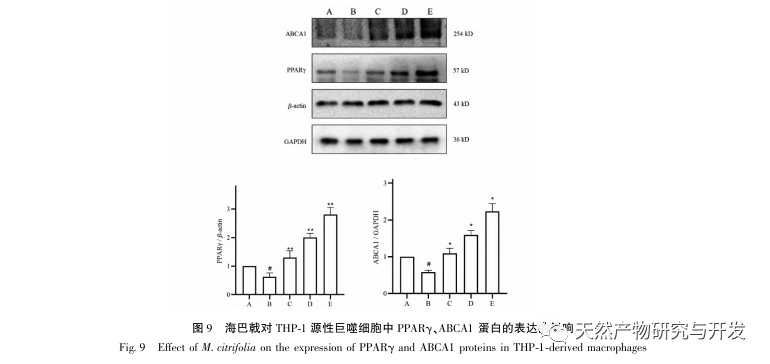
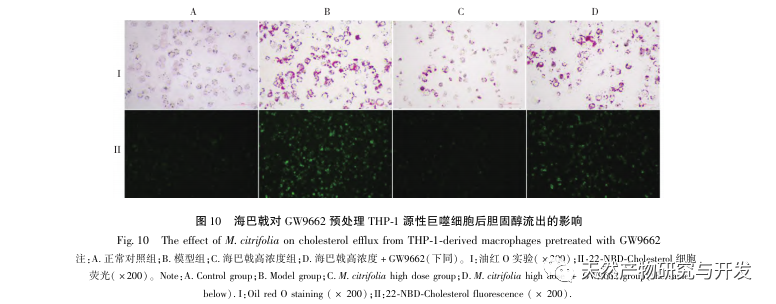
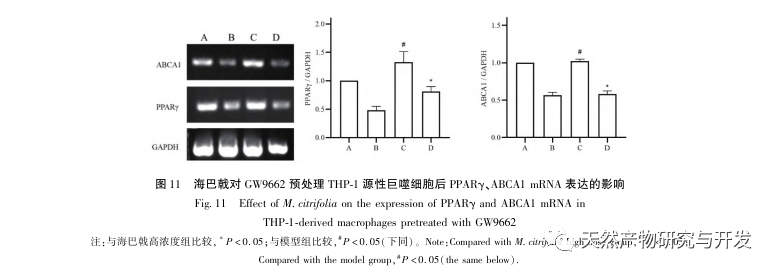
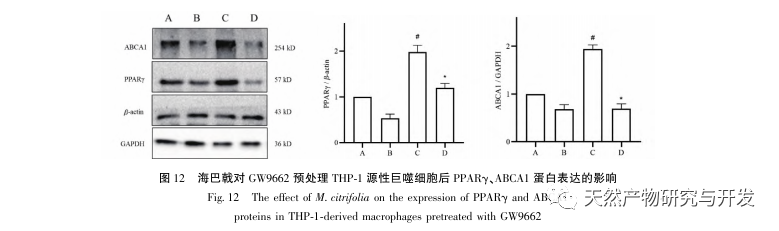
AS er en almindelig hjerte-kar-sygdom, og dens hurtige udvikling kan direkte føre til ondartede kardiovaskulære hændelser hos patienter, såsom myokardieinfarkt. Moderne medicin mener, at lipidteorien stadig er den vigtigste mekanisme for AS-forekomst. Statiner, PCSK9-hæmmere og andre lipidsænkende lægemidler bruges ofte i klinisk praksis til at bremse udviklingen af aterosklerose. Men på grund af de bivirkninger som muskelømhed og leverfunktionsskader, der stadig forekommer ved terapeutiske doser, kan mange patienter ikke tåle disse lægemidler. Derfor har jagten på nye, sikrere og mindre giftige lægemidler til behandling af AS en positiv betydning. Som et nyt lægemiddel og spiseligt produkt har Morinda officinalis en bred vifte af aktive ingredienser og farmakologiske virkninger, hvilket er i tråd med de typiske egenskaber ved traditionel kinesisk medicins multi-mål- og multi-vej-behandling af sygdomme. Denne undersøgelse brugte netværksfarmakologi til at forudsige de effektive ingredienser og mål for Morinda officinalis i behandlingen af AS og konstruerede en THP-1-afledt makrofagmodel for at verificere, at Morinda officinalis fremmer intracellulær kolesteroludstrømning gennem PPAR γ-signalvejen.
Ved at screene forskellige databaser fandt man ud af, at 59 forbindelser, herunder flavonoider, phenylpropanoider og fenolsyrer, hovedsageligt spiller en terapeutisk rolle i behandlingen af AS. I de senere år har flere forskningsrapporter vist, at flavonoider spiller en nøglerolle i behandlingen af SA og er de vigtigste aktive steder i plantemedicin. Sahib et al. fandt, at indholdet af catechiner, quercetin og kaempferol i frugten af Morinda officinalis var henholdsvis 53,68 mg/g, 7,4 mg/g og 6,4 mg/g, hvilket rangerer blandt de tre mest kendte aktive flavonoider. Disse tre komponenter spiller en vigtig rolle i reguleringen af abnormiteter i blodlipiderne og forsinker åreforkalkning. Forskning har vist, at hovedkomponenten i Yixin Tongmai-granulat, catechiner, direkte kan aktivere PPAR γ-vejen og forbedre AS gennem molekylær docking og in vitro- og in vivo-eksperimenter. Quercetin er almindeligt forekommende i forskellige planter med en betydelig andel i Morinda officinalis. Jia et al. og Li et al. rapporterede, at quercetin kan reducere plakindholdet i thoraxaorta i Apoe -/- musens AS-model induceret af fedtfattig kost betydeligt. Mekanismen er relateret til den øgede ekspression af ATP-bindende kassettetransportør A1 (ABCA1). Forskning har bekræftet, at kaempferol har en stærk antiinflammatorisk aktivitet og kan forsinke udviklingen af aterosklerose ved at aktivere PI3K/AKT/Nrf2-stien.
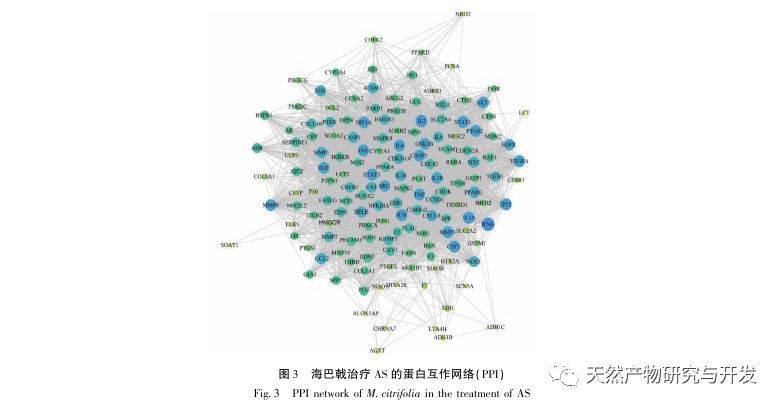
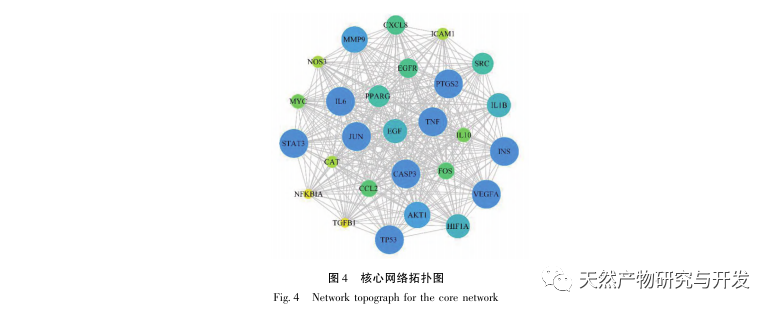
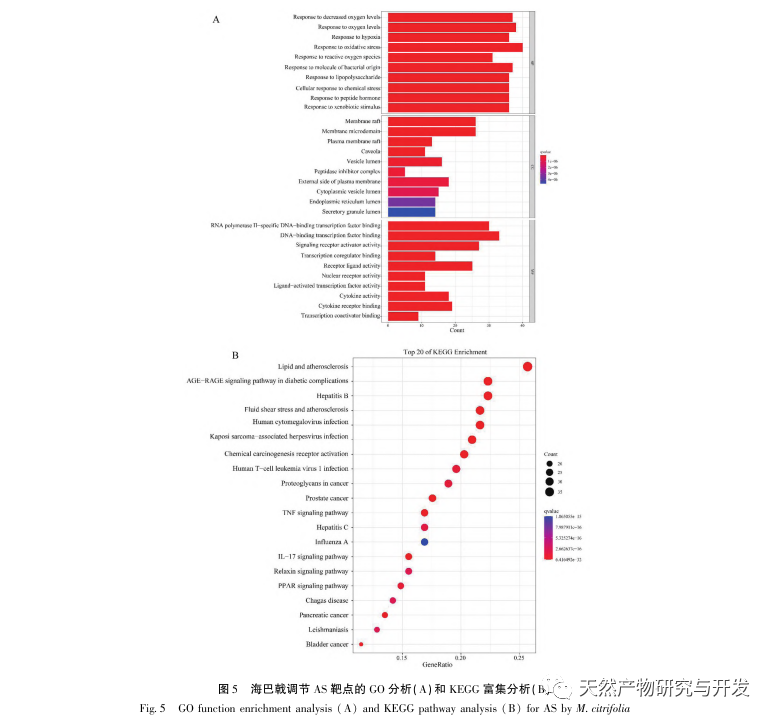
Efterfølgende afslørede GO-berigelsesanalysen, at Morinda officinalis hovedsageligt regulerer biologiske funktioner såsom membranreceptorer og nukleare receptorer i celler; Berigelsesanalyse af KEGG-signalveje afslørede, at behandlingen af AS med Morinda officinalis er forbundet med lipidmetabolisme-relaterede signalveje, hvor PPAR-signalvejen er en af dem. Forskning har vist, at lipidmetabolisme-relaterede signalveje, især PPAR-signalvejen, er tæt forbundet med lipidtransportører på cellemembranen og receptorer i kernen. Som vi alle ved, er PPAR klassiske nukleare receptorer placeret i kernen. Efter at have modtaget signalet fra second messenger øger PPAR udtrykket af kolesteroltransportører på cellemembranen ved at aktivere nedstrøms transkriptionsfaktorer, hvorved ophobningen af kolesterol i cellerne reduceres, og makrofager forhindres i at udvikle sig til skumceller. Derfor spiller PPAR-signalvejen en vigtig rolle i at reducere dannelsen af skumceller i lipidkerner og forsinke AS. Desuden er PPARG-genet også et vigtigt knudepunkt i kernenetværket i komponentmålnetværket i denne undersøgelse.
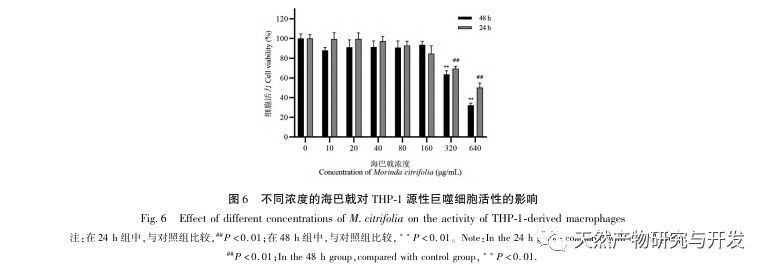
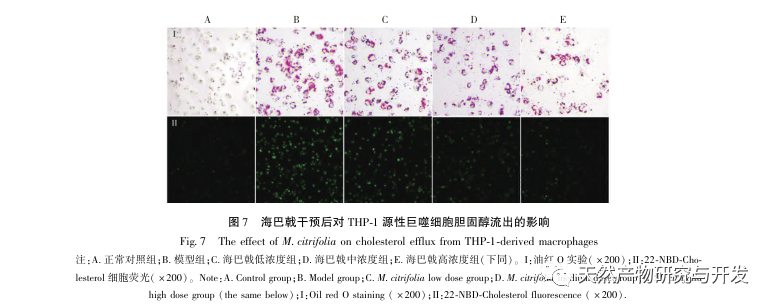
Baseret på ovenstående netværksfarmakologiske analyse konstruerede denne undersøgelse THP-1-afledte makrofager til at simulere skumceller i aterosklerotiske plaques in vitro. Efter at Morinda officinalis havde interveneret med THP-1-afledte makrofager, viste det sig, at det intracellulære kolesterolindhold blev reduceret betydeligt, og at udtrykket af PPAR γ i cellerne blev opreguleret betydeligt. Inada et al. og Nerurkar et al. bekræftede henholdsvis den lipidsænkende effekt af Morinda officinalis gennem dyreforsøg. I en klinisk undersøgelse blev det konstateret, at Morinda officinalis kan reducere LDL-niveauerne i serum betydeligt og øge niveauerne af lipoprotein med høj densitet (HDL) hos storrygende personer. For nylig bekræftede Chong et al., at Morinda officinalis kan reducere lipidplaques i aorta betydeligt i en termisk oxideret palmeolie-diæt induceret AS-rotte-model, men den specifikke mekanisme er ikke blevet belyst. Tidligere har Lee et al. udvundet tørret pulver af Morinda officinalis-frugt med 70% methanol og fundet ud af, at det kunne ophidse PPAR γ-receptorer i C2C12-skeletmuskelceller. Denne eksperimentelle rapport er i overensstemmelse med vores resultater. Denne undersøgelse viste for første gang, at Morinda officinalis kan fremme kolesteroludstrømning fra THP-1-afledte makrofager, og kombineret med netværksfarmakologi forudsagde den dens omvendte kolesteroltransport (RCT)-effekt ved at aktivere PPAR γ-signalvejen. En af de vigtige mekanismer, hvormed RCT regulerer lipidabnormiteter og forbedrer AS in vivo, er overførslen af kolesterol fra celler gennem scavenger-receptorer på cellemembranen, som derefter binder sig til apolipoprotein A, apoE og andre proteiner i plasmaet og transporteres til leveren for at blive metaboliseret. Det omdannes derefter til galdesyrer og udskilles fra kroppen, hvorved abnormiteter i lipidmetabolismen forbedres. ABCA1, som er en vigtig scavenger-receptor på makrofagmembranen, reguleres fint af den opstrøms nukleare transkriptionsfaktor PPAR γ og er ansvarlig for at transportere intracellulært kolesterol til det ekstracellulære rum gennem RCT-processen. I denne undersøgelse blev ekspressionsniveauet for ABCA1 opreguleret med aktiveringen af PPAR γ. Når PPAR γ-hæmmeren GW9662 blev brugt, blev opreguleringstendensen for ABCA1-receptorekspression i THP-1-afledte makrofager hæmmet, og der var ikke noget signifikant fald i det intracellulære kolesterolindhold, hvilket indikerer, at ABCA1 medieret af PPAR γ er den vigtigste bærer af intracellulær kolesteroltransport. På samme måde kan quercetin, baicalin og dihydromyricetin alle fremme RCT og udøve anti-AS-effekter ved at aktivere PPAR γ/ABCA1-signalvejen. Derfor kan Morinda officinalis fremme kolesteroludstrømning fra THP-1-afledte makrofager ved at aktivere PPAR γ-signalvejen.
Kort sagt har Morinda officinalis en sød og sur smag med afbalancerede medicinske egenskaber. Det kan give næring til nyreessensen, afbalancere yin og yang og forebygge kardiovaskulære og cerebrovaskulære sygdomme. Denne undersøgelse brugte netværksfarmakologi kombineret med in vitro-eksperimenter til at afsløre mekanismen for Morinda officinalis til behandling af AS og viste for første gang, at Morinda officinalis kan fremme kolesteroludstrømning fra THP-1-afledte makrofager og fremme RCT ved at aktivere PPAR γ-signalvejen. Derfor giver denne undersøgelse en ny farmakologisk mekanisme til effektiv forebyggelse og behandling af AS med Morinda officinalis. Der er dog stadig nogle begrænsninger i denne undersøgelse: (1) Da TCMSP-databasen ikke omfattede plantemedicinen Morinda officinalis, blev CAMUP-databasen og SwissADME-databasen brugt til at hjælpe med at screene dens aktive ingredienser. Selv om der har været undersøgelser, hvor man har brugt flere databaser til at screene ingredienser i traditionel kinesisk medicin i fællesskab, er screeningskriterierne for aktive ingredienser i forskellige databaser forskellige, så der er behov for yderligere verificering med hensyn til screeningens pålidelighed; (2) Denne undersøgelse screenede 5 sygdomsrelaterede databaser, og resultaterne viste, at der var betydelige forskelle i antallet af AS-mål i hver database, hvilket kan være relateret til forskelle i de sygdomstyper, der er inkluderet i hver database; (3) Baseret på resultaterne af in vitro-eksperimenter vil vores forskningsgruppe yderligere konstruere en AS-dyremodel for at give et mere komplet eksperimentelt grundlag for fremme af RCT og forsinkelse af AS ved Morinda officinalis ud fra perspektivet med in vivo-eksperimenter.
